Clear Sky Science · zh
溶酶体内的动态磁机械力诱导持久的巨噬细胞极化以实现抗肿瘤免疫
用温和的力唤醒免疫系统
癌症常常通过使机体防御陷入沉睡来存活。这项研究探索了一种出人意料的唤醒方式:用磁控纳米颗粒对免疫细胞内的微小隔室施加物理牵引。研究者并非仅依赖药物,而是在细胞内部利用精心调控的机械力,将称为巨噬细胞的免疫细胞重编程为持久的抗肿瘤战士。
为什么实体肿瘤难以治疗
现代癌症免疫疗法,如检查点抑制抗体和工程化免疫细胞,已改变了某些血液瘤的治疗。但对许多实体肿瘤患者(如肺癌)而言,这些方法仅对少数人有效。一个主要原因是肿瘤微环境:肿瘤被充满抑制性信号和细胞的保护性生态位所包围,从而削弱免疫反应。巨噬细胞可以处于攻击肿瘤的M1样状态或支持肿瘤的M2样状态,通常被推动进入有利于肿瘤的M2模式。用传统生化药物持久地逆转这种“不良”编程一直很困难。
把纳米颗粒变成微小的机械马达
研究团队设计了磁性纳米马达——由锌掺杂氧化铁构成、包覆正电荷聚合物的纳米级颗粒——这些颗粒很容易被巨噬细胞吞噬并在溶酶体(细胞的回收与信号中枢)中积聚。进入溶酶体后,外加旋转磁场使这些颗粒排列成杆状链并旋转,搅动溶酶体内黏稠的流体,产生微小涡流。计算机模拟和模型膜实验表明,通过精细调节旋转频率,可将溶酶体膜所受的剪切应力设定在一个“甜点”区间:强到足以使膜短暂渗漏,但又不足以导致永久性破坏。
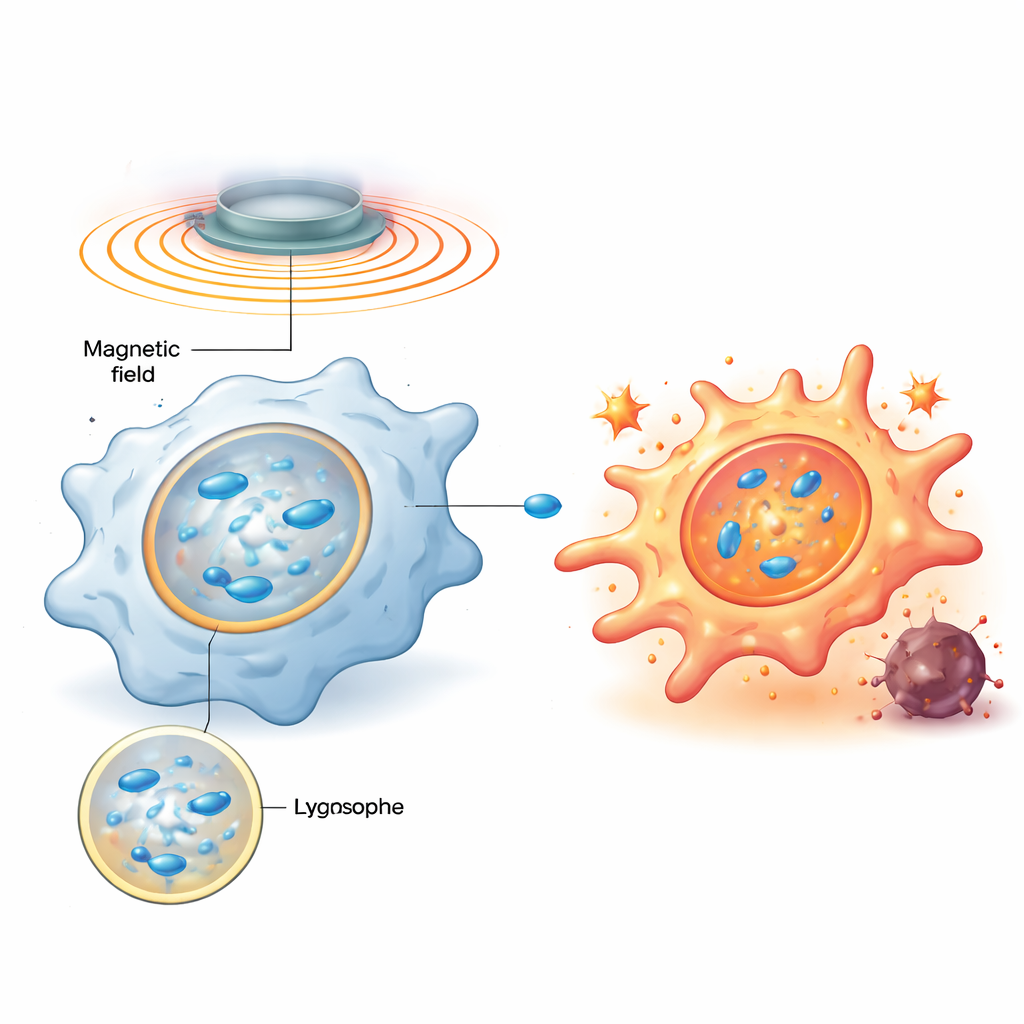
机械触发引发生化警报
当溶酶体膜短暂受扰时,一种结合糖分子的蛋白质——半乳糖凝集素‑9(galectin‑9)迅速聚集到受损部位,充当这一机械应力的感受器。研究显示,这会进而激活一个关键的能量感应酶AMPK,随后提升驱动炎症和抗菌反应的NF‑κB信号通路。上述信号共同将巨噬细胞的代谢从安静且节能的状态重塑为快速糖酵解的模式,这与具有敌对性的M1样行为相关。重要的是,当磁场关闭时,溶酶体可以修复并且信号减弱;当稍后重新开启磁场时,同一路径会被再次激活。这种可编程的开‑关循环允许研究者在不杀死细胞的情况下反复“敲击”同一机械开关。
重新教育巨噬细胞以对抗肿瘤
在细胞培养中,这种由磁力诱导的溶酶体通透性增加——称为MagLMP——能将被推向促肿瘤M2样状态的巨噬细胞重新转回促炎的M1样状态。被重编程的细胞产生更多炎性细胞因子,并在数天内保持其M1样谱系,即便在通常会促使其向M2转变的肿瘤来源培养基中也是如此。在小鼠肿瘤模型中,将磁性纳米马达植入肿瘤并施加每日旋转磁场循环,减缓了多种癌症的生长。当实验性去除巨噬细胞时,这一益处大多消失,表明这些细胞对疗效至关重要。对肿瘤组织进行单细胞RNA测序进一步显示,MagLMP增加了M1样巨噬细胞的比例、增强了抗肿瘤性中性粒细胞和效应CD8 T细胞,并在巨噬细胞内上调了与NF‑κB及糖酵解相关的基因。
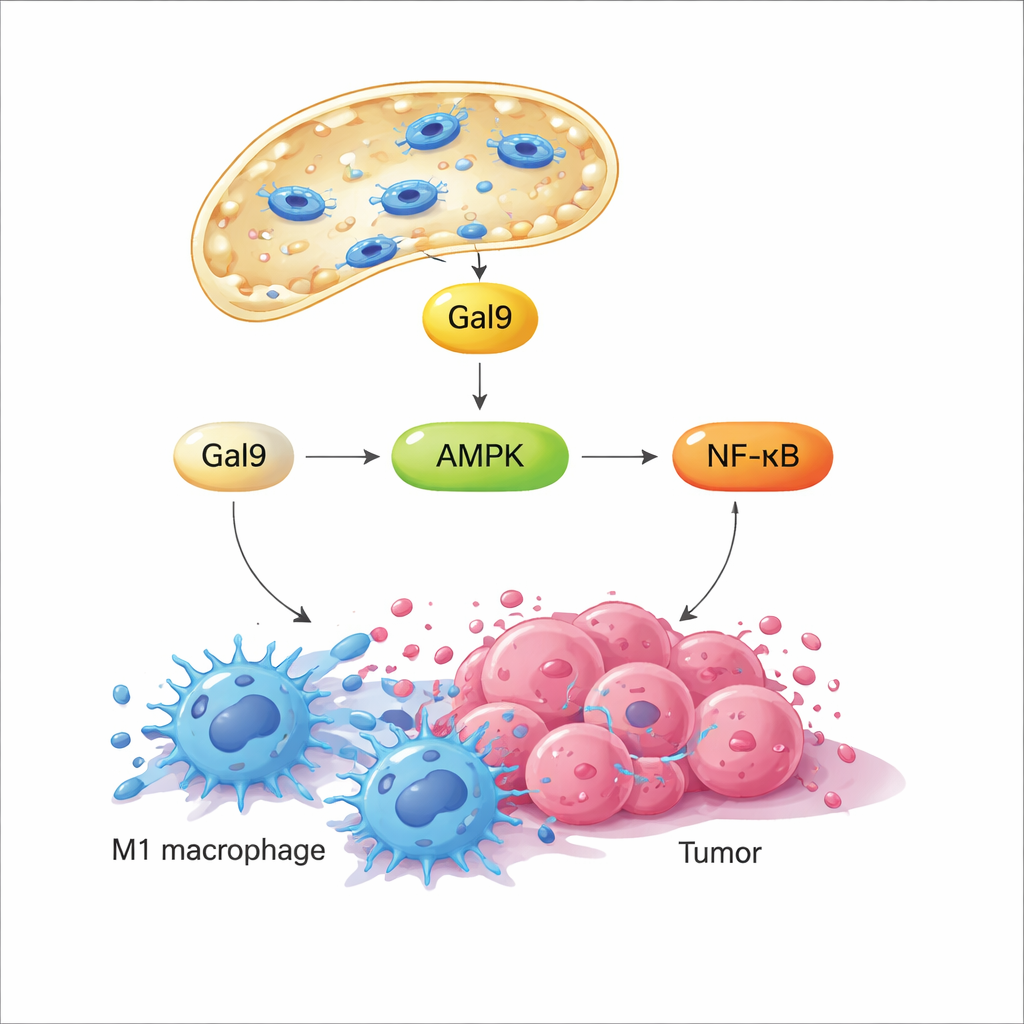
从局部控制到全身疗法
研究者接着探问这种方法是否能更像现实世界的治疗那样通过血液循环递送。他们将纳米马达静脉注射,并使用外部简单磁体将其集中到肿瘤内,证明了肿瘤床中巨噬细胞的高效摄取。随后的MagLMP处理再次将巨噬细胞转向M1样状态并抑制肿瘤生长。在一个肿瘤原位生长于肺部的早期肺癌小鼠模型中,结合磁性引导与周期性MagLMP显著延长了生存期:约三分之一的受治小鼠存活超过300天,而对照组仅存数周。在难治模型中,将MagLMP与PD‑1检查点抑制剂联合使用进一步增强了肿瘤控制。
一种从内到外控制免疫的新方式
这项工作表明,针对特定细胞器施加微小且精确可控的机械力,可用于调控活体免疫行为。通过反复且可逆地“戳动”溶酶体,MagLMP激活了galectin‑9–AMPK–NF‑κB轴,将巨噬细胞重编程为持久的抗肿瘤战士而不对细胞造成广泛损伤。对非专业读者而言,关键思想是:由磁驱纳米马达传递的物理信号可以像免疫系统的调节旋钮,为未来与药物互补的癌症免疫疗法提供新型工具。
引用: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
关键词: 癌症免疫治疗, 巨噬细胞重编程, 磁性纳米颗粒, 机械信号传导, 溶酶体信号