Clear Sky Science · zh
暂时性机械激活Piezo1通道促进体外扩增造血干细胞
制造更多救命的血液干细胞
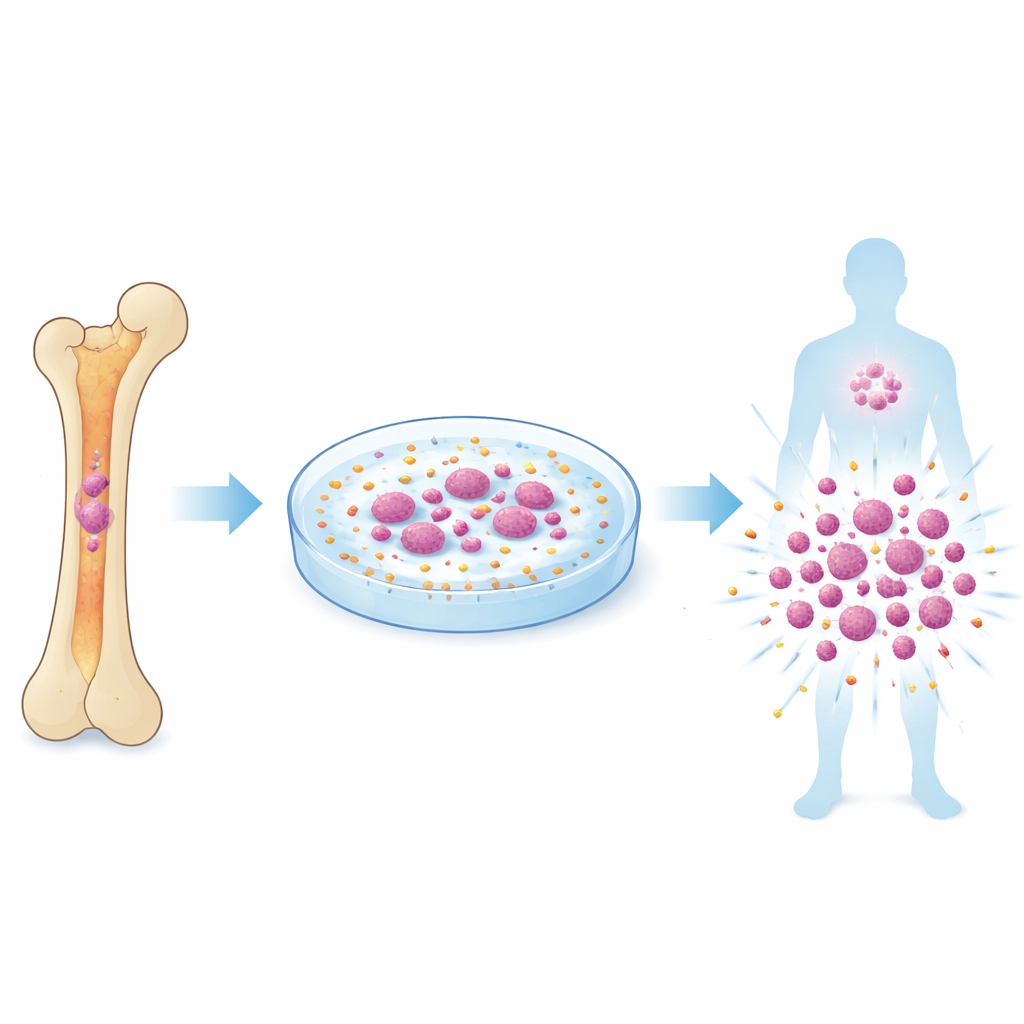
骨髓移植可以治愈某些血液癌症和遗传性疾病,但医生常受限于从供体获得的真正造血干细胞数量太少。本研究揭示了一种令人意外的方法,通过用微小的塑料微珠轻轻“触碰”细胞以刺激其表面的机械传感器,在体外扩增这些稀有细胞。该工作提示了一条新的、可能更安全的途径,以生成足够的干细胞,使更多患者能从移植中受益。
为什么扩增造血干细胞如此困难
造血干细胞位于骨髓深处,终生默默供给我们的红细胞、白细胞和血小板。移植这些细胞可以重置受损的血液系统,例如在白血病治疗中,但前提是有足够健康的干细胞且它们保持完全功能。在培养皿中扩增它们的努力常常不尽如人意:细胞往往要么停止自我更新,要么失去长期重建血液系统的能力。目前大多数方法依赖生长因子混合物和基因改造,但它们无法完全重现骨髓中复杂的物理环境,那里干细胞持续感受到推、拉与压力。
干细胞上隐藏的机械开关
研究人员把注意力集中在一种称为Piezo1的蛋白上,这是一种位于细胞膜上的微小阀门样通道,当膜被弯曲或拉伸时会打开,让钙离子涌入并启动细胞内信号。通过检查多种血细胞类型,他们发现Piezo1在真正的造血干细胞中尤其丰富。当他们用遗传手段删除Piezo1或用药物阻断它时,在培养皿中生长的干细胞就无法良好扩增,移植到小鼠后也不能有效重建血液。有趣的是,持续用化学激活剂刺激Piezo1也有害:细胞积累过多钙,产生有害的活性分子,且移植能力下降。这些结果表明,干细胞需要短暂且时机恰当的机械激活Piezo1,而不是持续的化学刺激。
利用微小珠子触动传感器
为了提供恰到好处的机械推动,团队转而使用微观高分子球体,本质上是光滑的塑料微珠,它们可以在培养中与干细胞发生轻微碰撞。他们测试了不同尺寸和刚度的微珠,发现直径500纳米的聚苯乙烯球——称为PS500——效果显著。当小鼠骨髓细胞与这些微珠共同培养时,干细胞数量显著增加,并且这些细胞在多代小鼠的连续移植中保持强劲的长期重建能力。精细的成像和力学测量显示,微珠反复以极小的力在干细胞膜上形成凹陷,足以短时打开Piezo1通道而不至于压垮细胞。
从机械触碰到生长信号
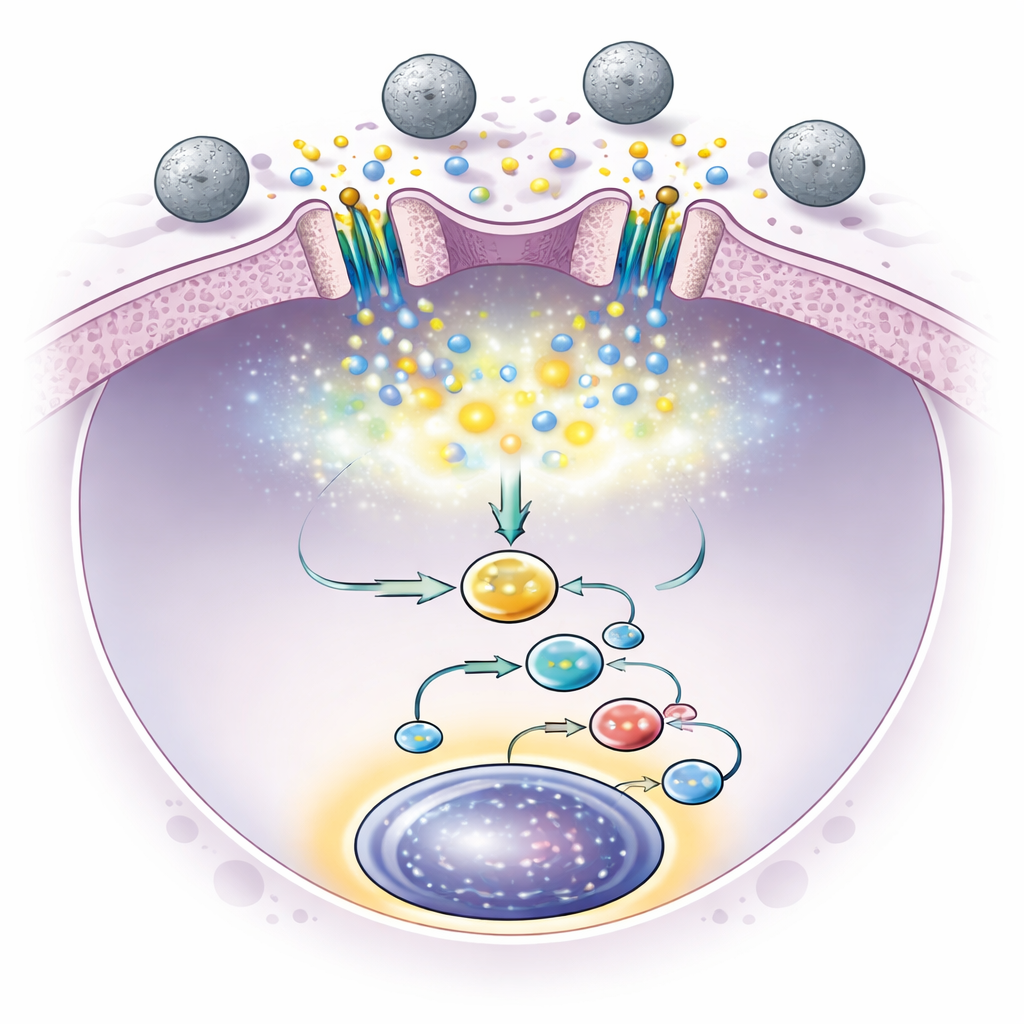
Piezo1通道的短暂开启会触发干细胞内钙离子的小脉冲流入。继而,这激活了内部通路,使细胞产生某些信号蛋白,尤其是生长因子白介素-6。白介素-6随后反馈作用于干细胞并在其细胞核中激活名为Stat3的蛋白,已知该蛋白有助于干细胞生存和自我更新。当研究人员阻断Stat3通路时,微珠的有益效果消失,证实了这一连锁事件——机械触碰、钙脉冲、白介素-6释放与Stat3激活——对扩增至关重要。重要的是,在仅短暂暴露于微珠之后,这些信号保持活跃且干细胞数量持续上升,表明不需要持续刺激。
对人类移植的前景
团队随后将同样的方法应用于从脐带血收集的人类造血干细胞——脐带血是常见但常受限的移植来源。使用PS500微珠,这些人细胞的扩增量比仅用领先的小分子方法多出数倍,同时保留了在免疫缺陷小鼠体内长期重建血液的能力。在小鼠中的安全性研究表明,微珠不会进入干细胞,可通过简单离心或过滤有效去除,且在测试剂量下未见明显器官损伤或血液异常。这使基于微珠的系统成为血库和移植中心实用且潜在可扩展的技术选择。
这对患者意味着什么
本质上,这项研究表明,一种温和的机械提示——由漂浮的纳米级微珠传递——可以在保持干细胞效力的同时促使其增殖,方法是短暂激活内在的压力传感器而非过度刺激它。如果能转化到临床,这种方法可能使从小量脐带血或部分供体生成足够高质量干细胞变得更容易,从而扩大可接受治愈性移植的患者范围。研究还强调,不仅要关注细胞周围的化学“汤”,也要关注它们所经历的物理感受,这可以开启控制细胞命运的新途径。
引用: Wang, Q., Zeng, X., Yang, H. et al. Transient mechanical activation of the Piezo1 channel facilitates ex vivo expansion of hematopoietic stem cells. Cell Res 36, 272–285 (2026). https://doi.org/10.1038/s41422-025-01209-1
关键词: 造血干细胞, 机械敏感离子通道, Piezo1, 聚苯乙烯微球, 干细胞移植