Clear Sky Science · zh
肌苷通过2,3‑BPG‑PNP轴促进红细胞代谢重编程并恢复氧气释放以实现回春
这为何与健康老龄化相关
随着年龄增长,器官常常无法获得足够的氧气,这是一种隐性压力,会促成心脏病、记忆力衰退、肌肉无力和其他与年龄相关的问题。本研究提出了一个简单却重要的问题:问题的一部分是否源自携氧的红细胞内部?一种常见的天然分子肌苷能否帮助恢复它们的活力?
红细胞随年龄的变化
研究者跟踪了300多名年龄在20至85岁的成人,仔细测量了他们红细胞释放氧气的能力。他们发现随着寿命延长这一能力稳步下降:年长者的红细胞更紧地结合氧气,向组织释放的氧减少。这一变化与其他器官的警示信号并存,包括血压升高以及肾脏和肝脏功能的轻微下降。在小鼠中也出现相同的模式:年老动物的红细胞释放氧气更少,并显示出更多的氧化应激——一种与衰老相关的化学磨损。
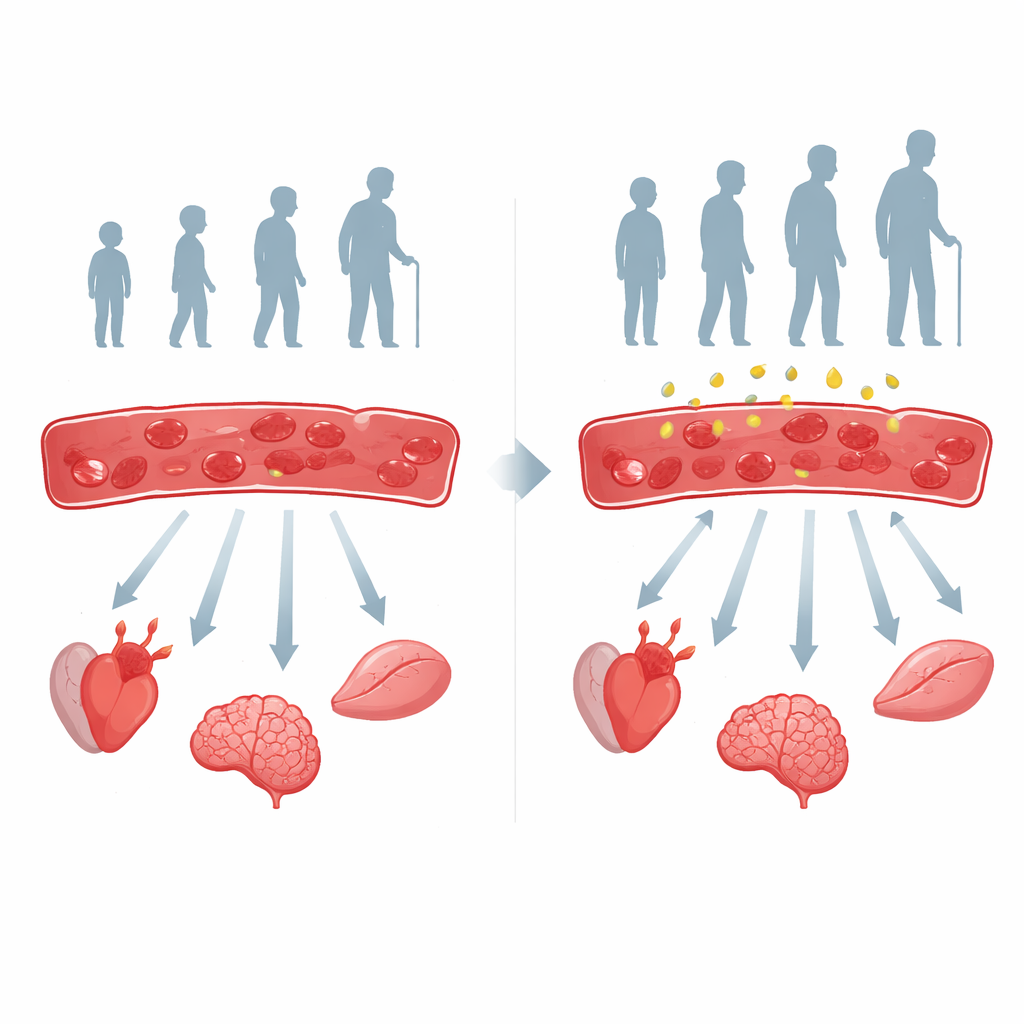
血细胞内的隐性燃料开关
红细胞缺乏细胞核和线粒体,因此依赖简化的内部化学反应来产生能量并微调氧气释放。一种名为2,3‑BPG的小分子通常帮助血红蛋白在需要处释放氧气。团队发现2,3‑BPG随年龄下降,因为合成它的酶BPGM活性减弱。在人类和小鼠中,较低的2,3‑BPG与更差的氧释放密切相关。当科学家构建无法合成2,3‑BPG的红细胞小鼠时,这些动物出现了更早的组织缺氧、更多的氧化应激、肌力减弱、记忆力下降和血糖控制变差——本质上是由红细胞变化单独驱动的加速衰老表型。
肌苷作为备用能量来源
代谢谱分析显示,衰老的红细胞不仅减速,它们还重接线。随着葡萄糖处理功能的减退,它们逐渐增加对肌苷的利用,肌苷是一种来自核苷酸的天然化合物。在年长的人和小鼠中,分解肌苷为称为核糖‑1‑磷酸的糖片段的酶PNP活性增强。使用标记的肌苷,研究者显示该核糖片段流入支持能量产生的关键内部通路,并且重要的是,有助于重建2,3‑BPG。在体外实验中,将人或小鼠红细胞置于肌苷溶液中可以迅速增强其释放氧气的能力并降低有害的活性氧——前提是细胞能通过称为ENT1的转运蛋白摄取肌苷并通过PNP将其消化。
基因测试与动物试验
为证实该备用燃料系统的重要性,团队构建了缺乏肌苷入口ENT1的红细胞小鼠。这些动物无法从肌苷中获益,氧释放能力较差,氧化应激更高,且随着年龄增长在认知、肌力和血糖控制方面衰退更快。随后,科学家进行了预临床试验:他们对中年小鼠连续一个月每天注射肌苷。经处理的动物显示红细胞释放更多氧气、产生更少有害的氧化物。小鼠在转杆测试中跑得更好、握力更强、记忆测试表现更优,并且心脏、肾脏、肌肉及涉及学习与记忆的关键脑区中缺氧损伤的证据更少。
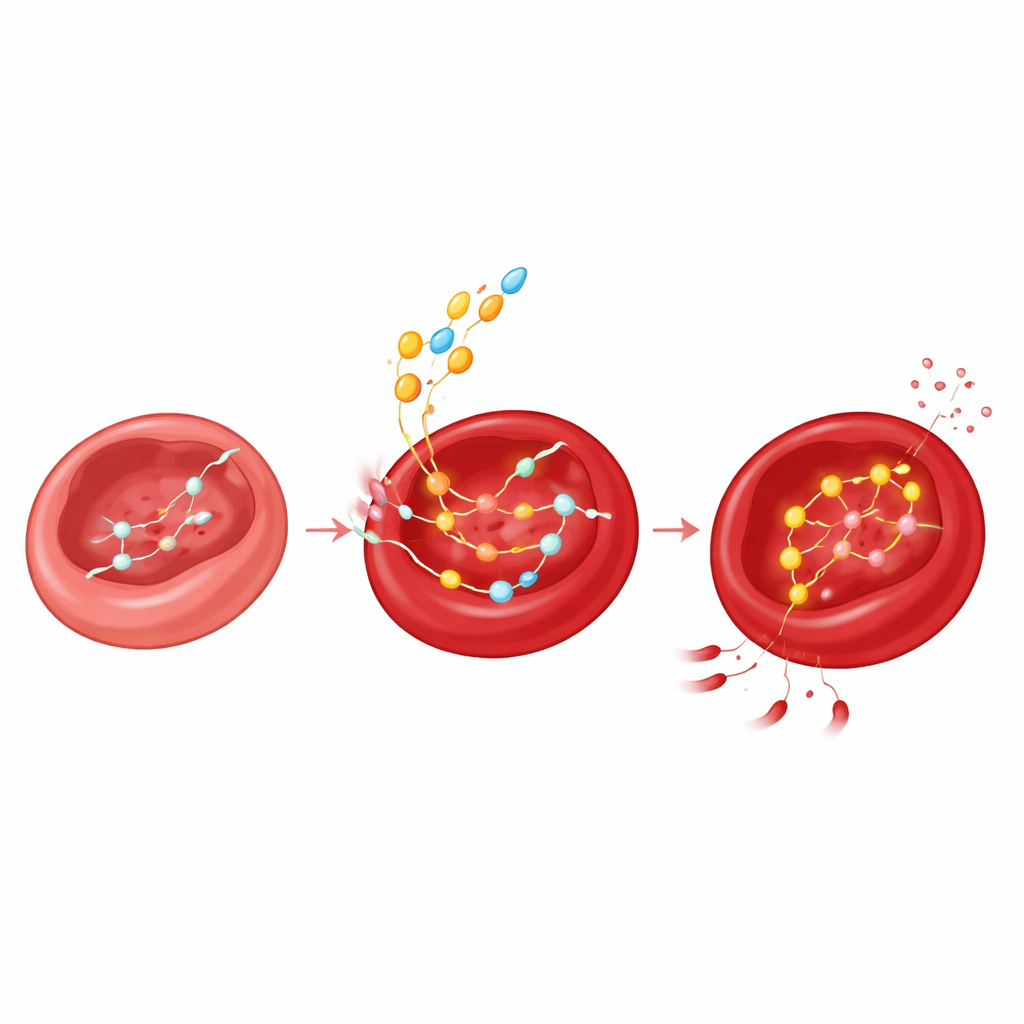
随年龄放松的分子刹车
研究还揭示了一个精巧的反馈回路。通过分子建模、酶学测定和定点突变,作者表明2,3‑BPG本身能与PNP结合并通过在酶的特定位点与磷酸竞争来抑制其活性。在年轻时,充足的2,3‑BPG因此抑制了肌苷的分解。随着2,3‑BPG水平随年龄下降,这个刹车被解除:PNP变得更活跃,肌苷被更快消耗,其核糖片段被转入产生能量的通路,以补偿迟缓的葡萄糖代谢。换句话说,既帮助血红蛋白释放氧气的分子,也在悄然控制红细胞如何利用应急燃料储备。
这对衰老与回春意味着什么
综合来看,这项工作提出衰老不仅关乎器官功能衰退,也关乎输送氧气的红细胞老化导致的氧气供应减弱。BPGM活性和2,3‑BPG的下降标志着一个新的“衰老特征”,而肌苷–PNP–ENT1轴则作为一套内建的救援系统,部分恢复能量流和氧释放。通过外源补充额外肌苷(至少在小鼠中),研究者能够加强这套救援系统、改善红细胞功能、缓解组织缺氧并减缓力量与记忆的下降。尽管在人类中仍有大量工作需验证,该研究提出了一个有趣的可能性:通过微调红细胞代谢——或许用肌苷或相关策略——可能成为促进更健康老龄化的一条新途径。
引用: Liu, W., Yang, Z., Chen, C. et al. Inosine promotes erythrocyte metabolic reprogramming and restores oxygen release for rejuvenation via 2,3-BPG-PNP axis. Cell Discov 12, 19 (2026). https://doi.org/10.1038/s41421-026-00877-6
关键词: 红细胞, 衰老, 氧气输送, 肌苷, 代谢