Clear Sky Science · zh
胆红素直接激活RIPK3以诱导非经典坏死性凋亡
当一种有益分子变为有害
胆红素最为人所知的是它导致新生儿黄疸的黄色素,以及瘀伤常见的颜色。在低水平时,它实际上有助于保护我们的细胞免受损伤。但当胆红素在体内积聚并渗入大脑时,尤其是在新生儿和重度肝病患者中,它可能造成持久损伤。本研究揭示了过量胆红素可直接翻转脑细胞内的一个分子“杀开关”的令人意外的机制,驱动一种破坏性的细胞死亡形式,并为未来治疗提供了新的靶点。
从血液色素到大脑威胁
胆红素是在机体回收红细胞时产生的。通常,肝脏会对其进行修饰和清除,使水平保持低且相对安全。在某些情况下——如新生儿黄疸、严重感染或肝衰竭——未被处理的胆红素会积累。由于其易溶于脂质,这种“游离”形式能穿过血脑屏障,尤其是在疾病或炎症削弱该屏障时。一旦进入大脑,胆红素已知具有毒性,但其损伤神经细胞的确切步骤一直不清楚。
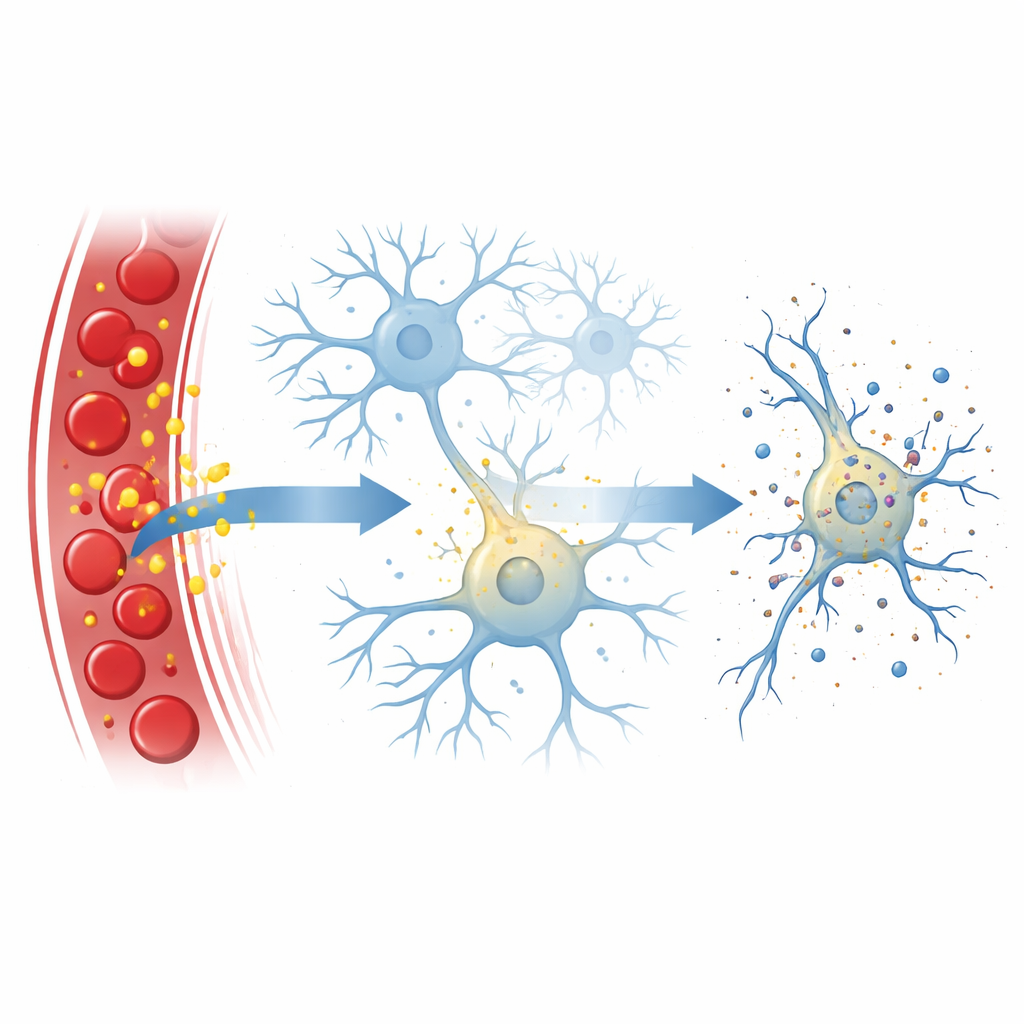
受控的细胞爆裂
研究人员将注意力集中在坏死性凋亡上,这是一种受调控的细胞死亡形式,类似于微小的爆炸:细胞肿胀,外膜破裂,细胞内容物泄出,常常触发炎症。这个过程通常由一系列蛋白驱动,其中称为RIPK3的蛋白起着中心枢纽作用,另一个蛋白MLKL则在细胞膜上打孔。在教科书式的经典通路中,RIPK3由识别炎性分子或病毒遗传物质等危险信号的伙伴蛋白激活。而在这里,团队发现胆红素可以绕过这些常规伙伴,仍然在神经细胞中驱动坏死性凋亡。
胆红素抓住了细胞的“杀开关”
通过培养的神经元、脑切片和小鼠模型,科学家们证明胆红素选择性地激活神经细胞中的RIPK3及其下游伙伴MLKL,而常规的上游蛋白基本保持不变。遗传学实验证明,当去除RIPK3或MLKL时,胆红素不再能有效地杀死神经元。生化测试进一步显示:胆红素在RIPK3活性核心的两个特定位点上直接结合,促进RIPK3分子聚集,并增强其激酶活性——即开启死亡通路的化学功能。这种对RIPK3的直接作用不依赖于蛋白的典型相互作用面(RHIM结构域)或其他适配蛋白,标志着进入坏死性凋亡的非经典途径。
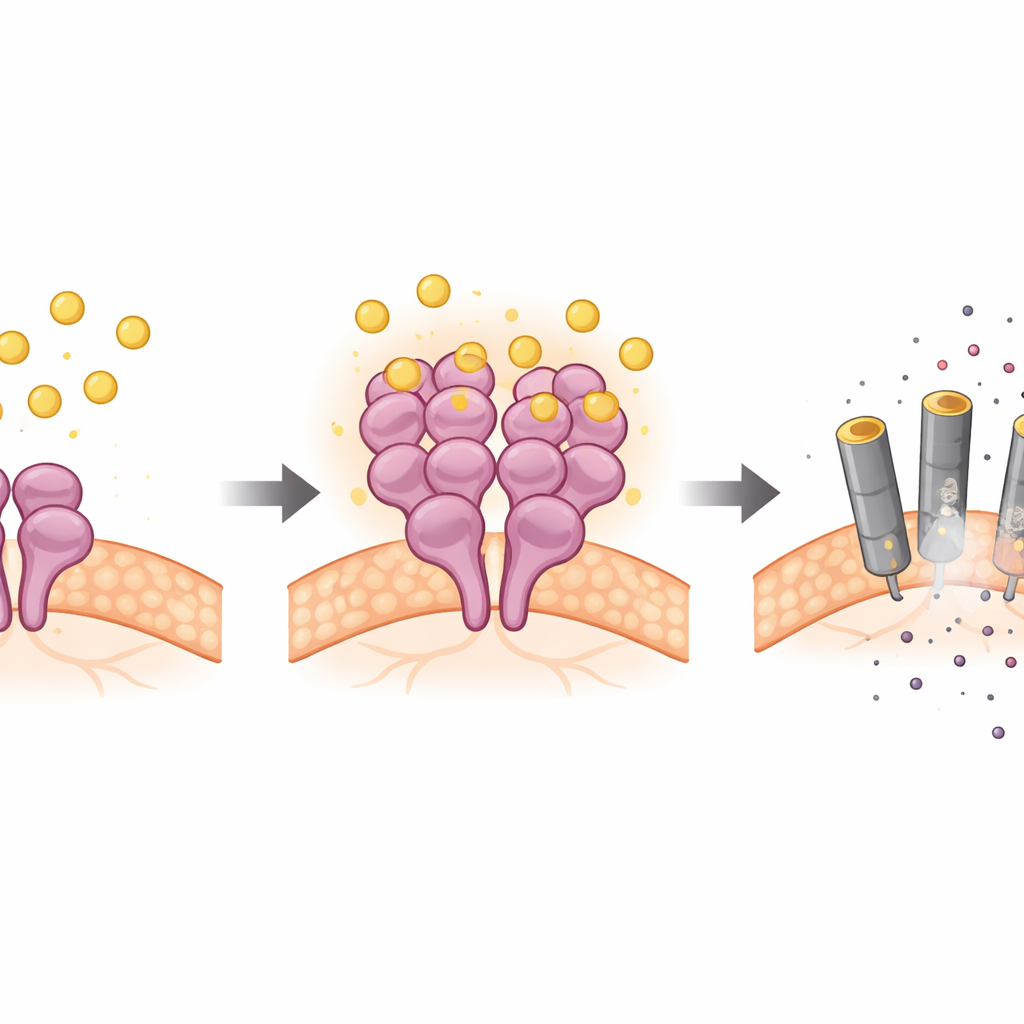
来自活体大脑的证据
为检验该机制在整只动物中的重要性,团队通过向小鼠脑内注射胆红素或诱导肝损伤和炎症使胆红素自然进入大脑来提高小鼠体内的胆红素水平。在正常小鼠中,这导致易感脑区中RIPK3和MLKL强烈激活,细胞死亡标志物增加,健康神经元明显减少。缺失RIPK3的转基因小鼠则受到保护:其神经元显示出明显更少的损伤、更少的死亡信号和降低的炎性反应,尽管胆红素水平同样很高。重要的是,通常被视为无害的经处理后水溶性胆红素既不激活RIPK3也未引起类似脑损伤,进一步强调未经修饰的脂溶性胆红素才是真正的罪魁祸首。
对患者意味着什么
这项工作表明,过量的未结合胆红素可以直接激活RIPK3,触发通过坏死性凋亡导致的受控但毁灭性的大脑细胞破裂。胆红素不仅仅作为一种广泛的毒物或氧化应激来源,而是像一种小分子激活剂,激活神经元和脑内免疫细胞中特定的死亡程序。对于重度黄疸或肝衰竭患者,这表明阻断RIPK3或MLKL——尤其是能进入大脑的药物——有一天可能有助于限制神经损伤。简言之,该研究展示了一个通常有益的色素如何变成精确的分子刺客,并指向在不破坏其日常保护作用的情况下解除其致命作用的新途径。
引用: Xue, Q., Ma, X., Chen, Z. et al. Bilirubin directly activates RIPK3 to induce non-classical necroptosis. Cell Discov 12, 21 (2026). https://doi.org/10.1038/s41421-026-00876-7
关键词: 胆红素神经毒性, 坏死性凋亡, RIPK3, 肝功能衰竭与脑损伤, 细胞死亡通路