Clear Sky Science · zh
ODAD1 功能缺失变体破坏 ODA 对接并在原发性纤毛运动障碍中诱导肌动蛋白细胞骨架重塑
当身体的显微刷子出错时
你的每一次呼吸都依赖于成千上万条微小的、毛发状的结构——纤毛,它们将黏液、病原体和尘埃扫出气道。在一种罕见的遗传病——原发性纤毛运动障碍(PCD)中,这些显微刷子无法正常工作,导致顽固咳嗽、肺部感染,有时还会出现脏器左右反位。本文研究揭示了单一基因 ODAD1 的破坏性改变如何不仅使纤毛内部的驱动马达失效,还意外地重塑了承载这些纤毛的细胞支架——暴露出该疾病一个新的、可能可药物干预的薄弱环节。
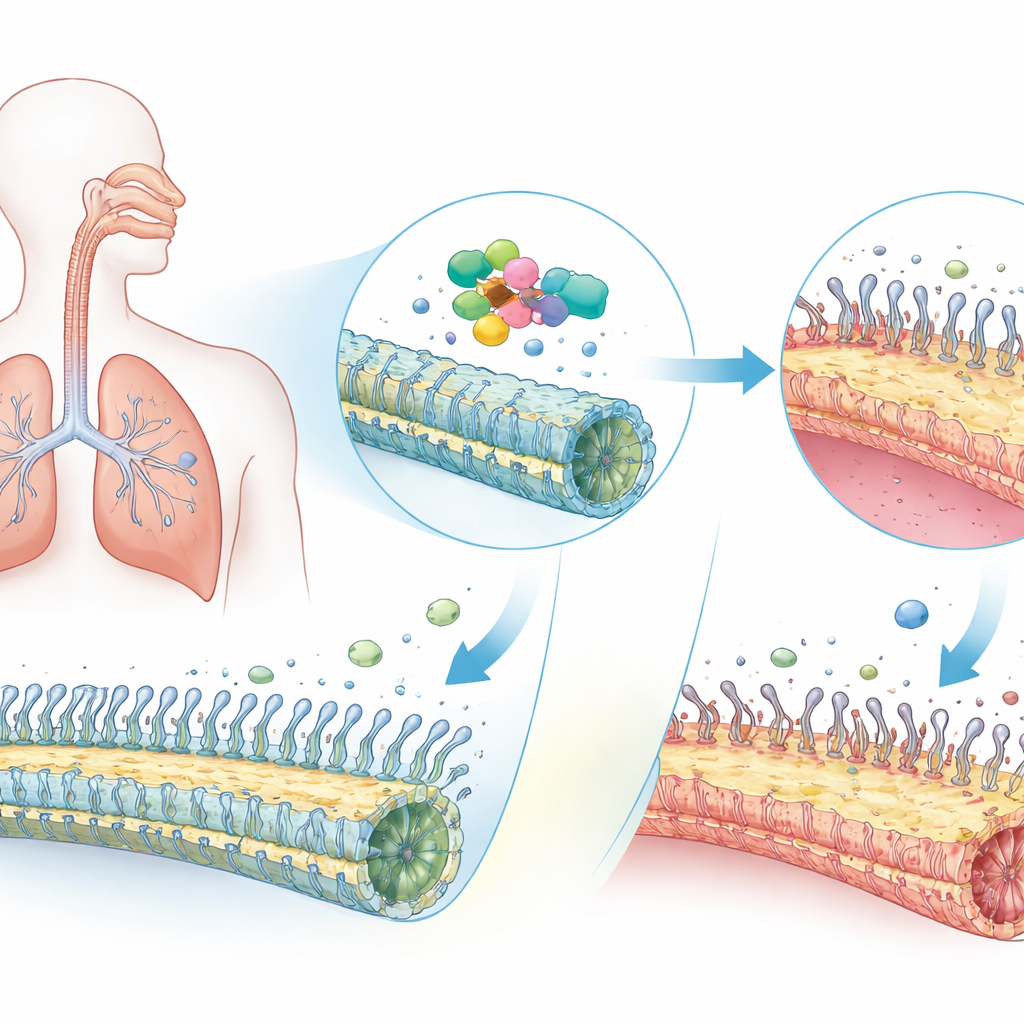
一种罕见但后果严重的肺部疾病
PCD 在全球大约每几千人中有一例,常在儿童期显现。由于鼻腔和肺部上皮的纤毛不能有效摆动,黏液和被困的微生物滞留,导致慢性鼻窦问题、中耳感染和进行性肺损伤。许多患者还出现“左右反位”(situs inversus),即心脏和其他器官左右位置颠倒,这是胚胎期纤毛未能引导早期体轴布局的标志。医生已知数十种不同基因的缺陷可致 PCD。ODAD1 是这些基因之一,负责将为纤毛摆动提供动力的分子马达固定到位。但科学家尚未完全弄清 ODAD1 缺陷在人体气道组织内如何发挥作用。
在患者细胞中追踪有缺陷的基因
研究人员研究了来自七个汉族家庭的九名个体,这些人表现出典型的 PCD 症状:新生儿期呼吸困难、终生湿咳、频繁肺部感染,以及呼气一氧化氮水平异常低下,这是一项临床特征。基因检测发现了四种有害的 ODAD1 变体,其中一种此前未曾报道。所有有缺陷的变体都严重降低或消除了鼻腔上皮细胞中的正常 ODAD1 蛋白。团队以高速摄影记录患者样本中的纤毛时发现,平滑、波状的正常摆动被微弱、无序的闪动所取代。从这些细胞培养的实验室模型——在气液界面重建的薄层有纤毛的气道上皮——也显示出相同的迟缓且不协调的运动。
破损的微型机械内部
为查明物理性损伤,科学家使用了强大的成像技术。常规电子显微镜和尖端冷冻电镜显示,患者纤毛的外侧驱动单元及其对接位点完全缺失。在某些病例中,纤毛轴心的其他关键结构也错位或畸形。这些缺陷解释了纤毛无法产生足够力量来搬运黏液的原因。然而,损害并不限于纤毛本身。来自患者来源培养的气道表面包含的多纤毛细胞明显减少,剩余的细胞排列异常、体积增大,且其纤毛方向混乱。令人意外的是,每个细胞内作为纤毛发芽起点的“基体”数量正常,提示问题出在这些细胞在组织表面的组织方式,而不是它们试图构建的纤毛数量。
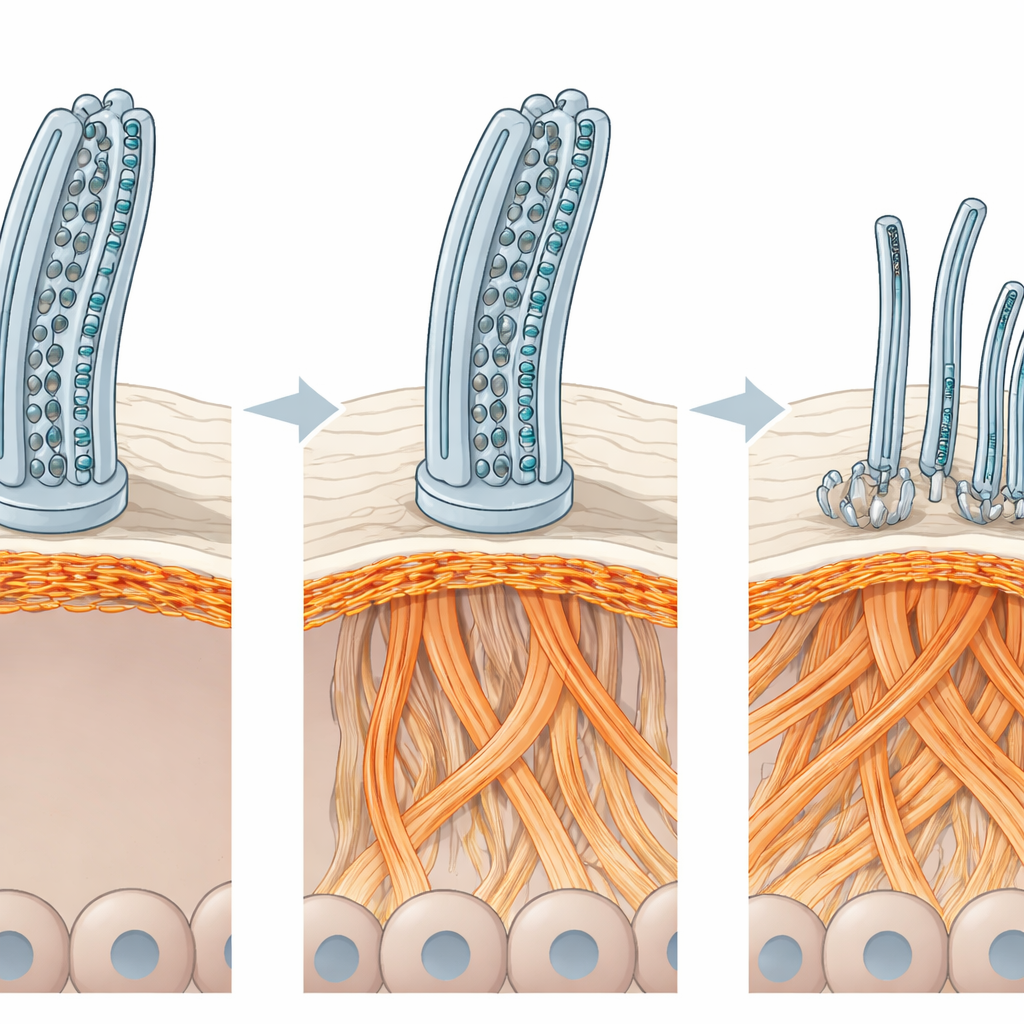
细胞内部支架被重接线
为确定破坏组织排列的原因,团队在患者来源的气道培养物中测量了数千种蛋白质。尽管许多与纤毛相关的蛋白减少,但若干与肌动蛋白相关的蛋白反而增多。对肌动蛋白丝的成像证实了这一支架的显著重塑:多纤毛细胞顶部出现增粗的肌动蛋白束,细胞边界处的网络被压缩,组织更深处形成凝聚的斑块。这些变化并非患者遗传背景独有:在健康细胞中敲除 ODAD1 会产生相同的肌动蛋白重接线和多纤毛细胞减少。当研究者使用小分子药物温和扰动肌动蛋白组装时,多纤毛细胞的数量及其表面排列部分恢复,纤毛数量增多且组织得更好——尽管在没有 ODAD1 介导的马达对接作用下,纤毛仍无法完全恢复正常摆动。
恢复缺失部件并展望未来
最后,研究者测试了替换 ODAD1 是否能恢复纤毛运动。他们用患者细胞培养出“顶端朝外”的气道类器官——带纤毛向外的微型空心气道组织球体,并使用慢病毒载体递送一份功能性 ODAD1 拷贝。导入的蛋白正确定位到纤毛中,恢复了缺失的马达对接位点,并使纤毛的摆动速度与模式接近正常。综合来看,这些结果表明 ODAD1 丧失通过两条路径损害气道:直接使纤毛的马达系统失能,间接扰乱塑造有纤毛表面的肌动蛋白支架。对于患者而言,这一双重认识提示了双管齐下的治疗前景——通过基因疗法纠正主要的马达缺陷,同时采用更安全的肌动蛋白调节策略,帮助重建健康的纤毛“地毯”,从而恢复清除肺部的功能。
引用: Huo, C., Luo, T., Yang, S. et al. Loss-of-function variants in ODAD1 disrupt ODA docking and induce actin cytoskeletal remodeling in primary ciliary dyskinesia. Cell Discov 12, 25 (2026). https://doi.org/10.1038/s41421-026-00875-8
关键词: 原发性纤毛运动障碍, ODAD1, 运动纤毛, 肌动蛋白细胞骨架, 基因治疗