Clear Sky Science · zh
使用 CmTSA 超复合技术在归档临床标本中确定肿瘤微环境结构的综合空间分析流程
为什么肿瘤周围的隐秘格局很重要
癌症不会孤立生长。它们被一个繁忙的“邻里”环绕——包括免疫细胞、支持细胞、血管和类瘢痕组织,这些共同组成了肿瘤的“微环境”。本文介绍了一种在常规医院组织样本上详尽绘制这一隐秘格局的实用方法。通过揭示哪些类型的细胞相互邻近,以及它们如何组织成有益或有害的微社区,该方法有助于医生更好地预测患者肿瘤的行为并判断哪些治疗最有可能有效。
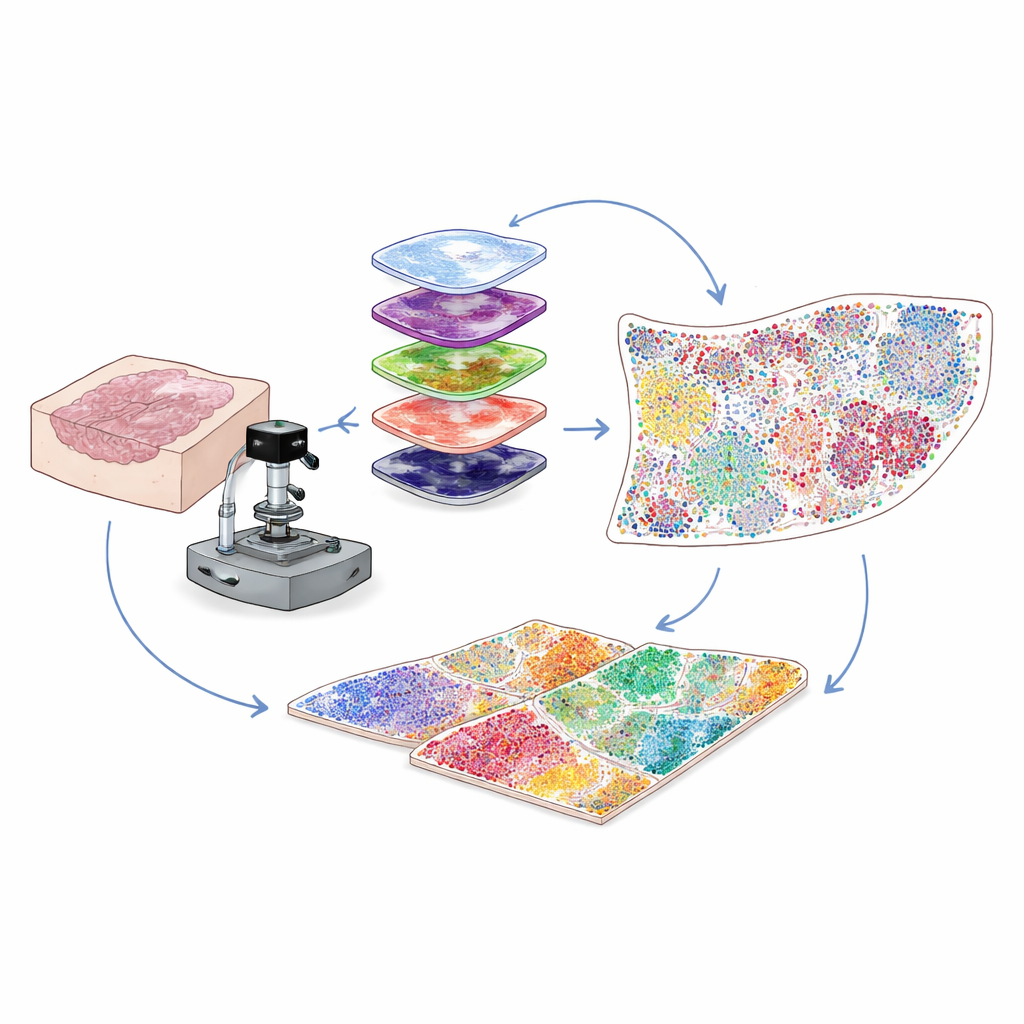
在日常医院样本中看见更多信息
大多数临床癌症样本以薄片石蜡包埋组织(FFPE 块)的形式保存,可存放多年。这些样本是研究的宝库,但一个技术问题阻碍了科学家:此类样本具有天然的背景荧光,会淹没许多重要蛋白的微弱信号。作者通过结合强度可控的光照与温和的化学处理来选择性地抹去这种背景荧光,而不损伤组织或蛋白靶点,从而解决了这一问题。这个光学与化学结合的“漂白”步骤显著提高了图像清晰度,使原本会丢失的微弱蛋白信号得以被检测到。
在同一切片上标记数十个蛋白位点
为了了解存在哪些细胞以及它们在做什么,研究者用针对特定蛋白的抗体对组织进行染色。传统的多重标记方法要么在检测稀有蛋白时信号微弱,要么一次只能追踪有限数量的标志物。本研究团队使用了一种称为循环酪氨酸酶信号放大的方法。在每一轮中,一小组标志物被染色并通过酶促反应“显色”成明亮且永久附着的荧光点。随后温和去除抗体而保留信号,重新漂白背景,再加入下一组标志物。通过重复该循环多次并利用来自细胞核的恒定信号对图像进行对齐,他们能够在单个组织切片上、整个载玻片范围内以单细胞分辨率可靠地可视化 30 到 60 种不同的蛋白。
将彩色图像转化为逐细胞的图谱
高通量图像包含数百万像素,远超过人眼能逐一分析的范围。因此,作者构建了一个计算机视觉流程,首先使用最初为通用细胞分割开发的深度学习工具检测并描出每个细胞核的轮廓。然后,基于每种蛋白荧光出现的位置——膜上、胞质中或细胞核内——以及一组逻辑判定规则,将每个细胞归类为某一类型或亚型,例如肿瘤细胞、辅助性 T 细胞、杀手 T 细胞、B 细胞、成纤维细胞等。输出是一个数字表格,列出载玻片上每个细胞的身份及其确切坐标。这把复杂的图像转化为关于肿瘤微环境中“谁在何处”的定量地图。
揭示塑造预后的细胞邻里
细胞很少独自行动;关键在于它们拥有哪些邻居。为了捕捉这一点,研究人员测试了不同的方式来定义每个细胞周围的局部邻域,并最终采用基于半径的网络方法。想象在每个细胞周围画一个小圆圈——大约相当于一根人类头发的厚度——并列出圈内的“住户”。通过将具有相似邻居组合的细胞分组,该方法识别出反复出现的“功能性生态位”,例如富含免疫细胞的区域、以成纤维细胞为主的屏障或由肿瘤细胞主导的区域。将这一策略应用于结肠组织表明,基于半径的邻域比替代方法更契合已知的解剖结构。在来自预后好与预后差患者的宫颈癌样本中,团队发现入围预后好的患者其免疫细胞丰富的生态位集中在肿瘤边缘,而预后较差的患者则显示出包裹肿瘤细胞的厚重成纤维细胞密集区,似乎将攻击性的免疫细胞隔离在外。
从空间地图到个体化治疗
通过将高质量、经济可行的多蛋白染色与稳健的图像分析相结合,这项工作提供了一个可应用于大量常规医院样本的端到端流程。该方法将保存的组织转化为关于肿瘤细胞、免疫细胞和基质细胞如何排列与相互作用的详细地图。对非专业读者来说,结论是:不仅是细胞类型重要,它们精确的邻里格局也会影响癌症的行为。该平台可能帮助研究者定位保护性的免疫热点、识别抑制性的细胞屏障,并最终支持更准确的预后判断与更精细调整的免疫疗法策略。
引用: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
关键词: 肿瘤微环境, 空间蛋白组学, 多重成像, 癌症免疫学, 单细胞分析