Clear Sky Science · zh
神经嗜性病毒的时间生物学:有节律的病毒入侵与无节律的宿主钟表
为何时机对脑部感染至关重要
许多危险病毒,包括狂犬病病毒和疱疹病毒,擅长侵入大脑和神经系统。这项研究提出了一个看似简单但意义重大的问题:一天中不同时间是否会改变这些“神经嗜性”病毒进入我们神经系统的难易程度,而病毒反过来又能否扰乱我们的生物钟?理解宿主钟表与病毒之间这种双向对话,可能为疫苗、抗病毒药物及轮班安排的时间化提供新思路以降低感染风险。
每日的体内钟与病毒入门口
几乎每个细胞都携带一个内建的24小时定时系统,通常称为昼夜节律钟。它由一组核心钟蛋白驱动,包括 BMAL1 和 REV-ERBα,它们以节律性的波动开启或关闭数千个基因。作者将注意力放在病毒进入细胞所使用的“门把手”——细胞表面的受体蛋白上,涵盖数十种以大脑为靶或能入侵大脑的病毒。通过检查由干细胞培养的类脑类器官、来源于神经的细胞系和小鼠组织,他们发现大多数这些病毒受体在一天中呈升降节律。这些节律与钟成分的活动紧密对应,表明我们的日常计时系统默默控制着任一时刻可用的病毒入侵点数量。
一个细胞周期因子成为钟表信使
进一步深入,研究人员探究了一个通常以控制细胞分裂闻名的蛋白 E2F8 在这一计时网络中扮演何种角色。他们发现 E2F8 本身受昼夜节律控制,并像一个中继,连接钟表与至少一个关键的狂犬病受体 p75NTR。当钟蛋白 REV-ERBα 活跃时,它抑制 E2F8。反过来,低水平的 E2F8 解除对 p75NTR 基因的抑制,使该受体的产生增加,从而让细胞对狂犬病毒更易受感染。显著的是,E2F8 也反馈影响钟表:它可直接结合核心钟基因(如 REV-ERBα 和 PER2)的调控区并削弱其活性。这形成了一个反馈回路,使得细胞周期调控因子帮助塑造每日节律,并通过这种节律影响神经细胞的易感性。
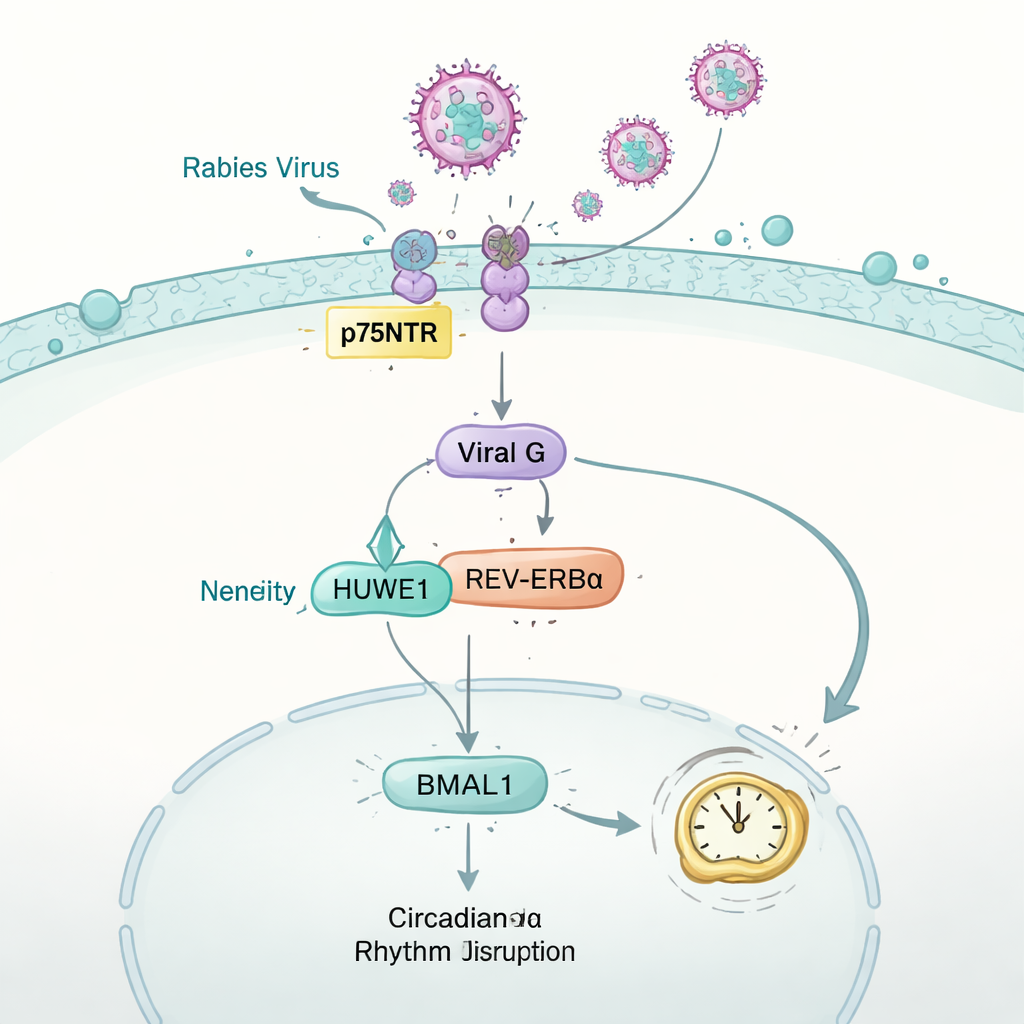
狂犬病毒如何使生物钟偏离轨道
研究随后反过来提问:病毒能否反过来冲击宿主钟表?在被狂犬病毒感染的小鼠中,团队监测了跑轮活动、代谢与呼吸化学指标。尽管在感染早期摄食正常,动物逐渐丧失了健康小鼠所表现的昼夜规律。在大脑及若干器官中,关键钟蛋白 BMAL1 的水平显著下降。在类神经细胞中,这一效应可追溯到狂犬糖蛋白“G”——一种帮助病毒与细胞融合的表面蛋白。G 劫持了宿主酶 HUWE1,该酶通常帮助标记另一个钟蛋白 REV-ERBα 以便降解。通过与 HUWE1 竞争,病毒 G 蛋白使 REV-ERBα 稳定化,导致对 BMAL1 的额外抑制,最终扰乱维持生理24小时节律的钟表机制。
时机、时差与感染严重性
为检验这些分子变化是否对整体生物体重要,研究团队在不同时间段(常规明暗周期、慢性“时差”条件)以及在缺失 REV-ERBα 的基因改造动物中,于不同时间给小鼠接种狂犬病毒。若在其活动(夜间)期开始时感染小鼠——此时狂犬病受体 p75NTR 达到高峰——小鼠体重下降更快,多个脑区的病毒载量更高,脑部炎症更严重,死亡也比在休息期开始感染的小鼠更快速。暴露于模仿轮班工作的反复相位转换的小鼠,大脑丧失正常钟律,p75NTR 水平持续偏高,基础抗病毒信号减弱,病情更严重。相反,缺失 REV-ERBα 的小鼠表达较少 p75NTR,病毒载量较低,感染后存活时间更长,表明这一钟组件是决定狂犬病严重程度的关键门控因子。
对人的意义
简言之,该研究表明我们体内的时钟不仅仅决定睡眠时间;它们还开关着脑部入侵病毒所利用的分子门道,而这些病毒也能通过扰乱钟表来反击。单一因子 REV-ERBα 处于关键交汇点:它与 E2F8 一同影响受体水平和每日节律,而狂犬病毒则利用它谋取利益。这些洞见指明了实际可行的方向。疫苗或抗病毒药物可能在一天中特定时段效果更好——比如受体水平较低或免疫反应较强时。长期节律被扰乱的人群——例如轮班工人或频繁旅行者——可能面对某些神经嗜性感染的更高风险。靶向 REV-ERBα 或相关通路,可能有助于将平衡倾向宿主,减轻感染严重性并改善临床结局。
引用: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
关键词: 昼夜节律钟, 神经嗜性病毒, 狂犬病, 病毒受体, 时间治疗