Clear Sky Science · zh
新辅助化疗后卵巢癌免疫微环境的动态变化
这项研究为何与卵巢癌女性相关
晚期卵巢癌常在手术前或手术后使用强效化疗,然而许多患者仍会复发并对药物失去反应。本研究提出了一个紧迫的问题:化疗如何悄然重塑肿瘤周围的自身防御系统,我们能否调整这种反应以延长治疗效果?通过对单个细胞的分析并在小鼠中测试新药物组合,研究者揭示了脂质类类激素分子——前列腺素在化疗后帮助肿瘤逃避免疫监视中的隐性作用。
围绕肿瘤的战场在变化
卵巢肿瘤并非孤立生长:它们处于充斥免疫细胞、结缔组织和腹腔液体的“邻里”环境中。治疗前,这一环境已偏向癌细胞,有很少的攻击性杀伤性T细胞和大量抑制免疫反应的细胞。团队分析了既往发表的高分化浆液性卵巢癌患者的单细胞RNA测序数据,比较了新辅助化疗(术前化疗)前后的样本。他们发现化疗并不只是杀死肿瘤细胞;它还暂时激活了免疫反应,增加了与T细胞刺激和炎症相关的信号,同时减少了部分通常抑制免疫攻击的调节性T细胞。
有益变化何时转为有害
尽管这种短暂的免疫增强存在,大多数患者仍会复发并对铂类药物(如顺铂)产生耐药。为弄清缘由,研究者深入探究不同细胞类型在治疗后如何相互通讯。他们发现化疗显著提升了肿瘤相关巨噬细胞和成纤维细胞中与前列腺素合成相关基因的表达,并增强了这些细胞与T细胞之间的通讯。借助先进的数学工具,研究显示总体环境向一种促炎但最终抑制性的状态转变,趋升的趋化因子招募髓系细胞的信号增强,同时一些通路会随时间消耗T细胞功能。这表明前列腺素可能充当分子开关,将最初有益的免疫反应转变为对抗肿瘤免疫的长期刹车。
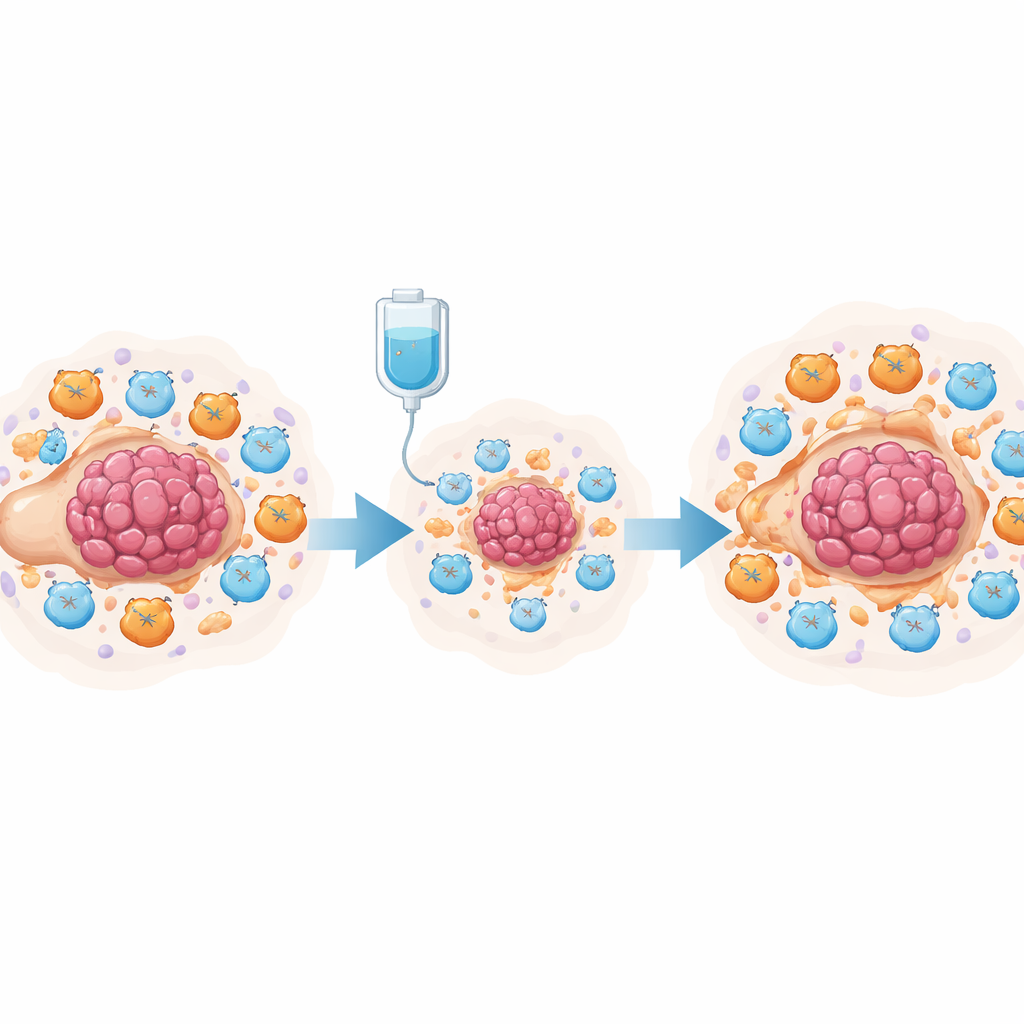
化疗、前列腺素与沉默的T细胞
为了在实验上验证这一想法,团队在顺铂治疗的小鼠卵巢癌模型中进行了研究。对腹腔中数万细胞的单细胞分析显示,顺铂减少了肿瘤细胞并增加了总体T细胞数量,但也显著扩增了髓源性抑制细胞(MDSC)和功能耗竭的杀伤性T细胞。肿瘤细胞和这些抑制性细胞均产生高水平的前列腺素合成酶。在共培养实验中,顺铂处理的肿瘤细胞促使骨髓细胞获得类似MDSC的状态,并削弱了CD8+杀伤性T细胞的功能和增殖。研究者将这一效应追溯到肿瘤细胞中的NF-κB信号通路,该通路开启了PTGES基因,这是生成前列腺素E2的关键步骤。阻断该通路可降低PTGES表达和前列腺素产出。
用联合疗法扭转局势
最具实际意义的问题是:抑制前列腺素是否能增强化疗效果?在小鼠中,科学家通过在肿瘤细胞中基因敲除Ptges、使用中和前列腺素E2的抗体,或使用抑制前列腺素E合酶的小分子药物等方法进行干预。所有这些方法均降低了前列腺素水平,减少了MDSC的积累,并恢复了CD8+ T细胞的杀伤能力和类干性复原力。当与顺铂或标准的顺铂-紫杉醇方案联合使用时,前列腺素抑制剂比单独化疗更有效地减缓肿瘤生长和扩散。数据表明,前列腺素驱动的免疫抑制并非附带现象,而是肿瘤在初次响应后逃逸的核心原因之一。
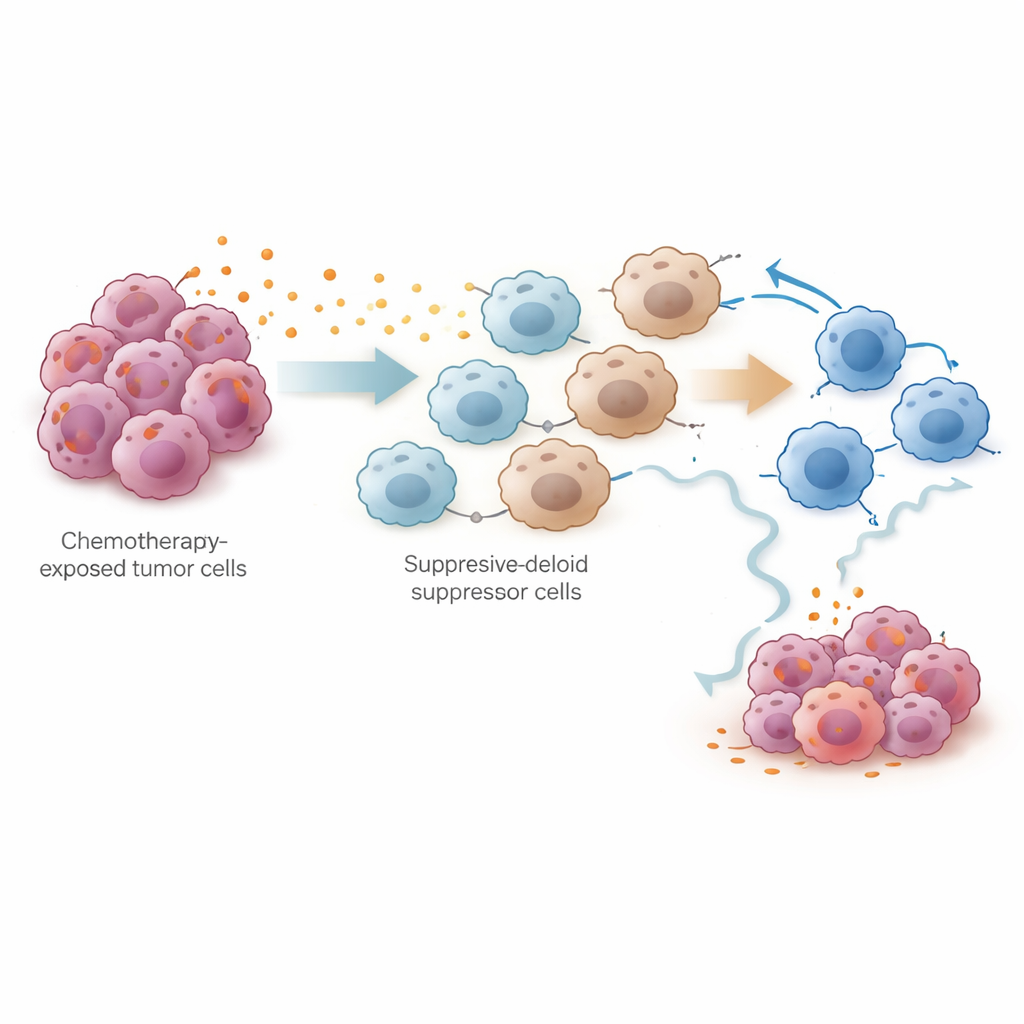
保持疗效的新视角
通俗地说,这项工作表明化疗以两个阶段改变肿瘤周围环境:先是削弱癌细胞并短暂动员免疫系统,随后诱发一波前列腺素,召集抑制性细胞并使机体的天然杀瘤力量疲惫不堪。通过确定由PTGES驱动的前列腺素生成为关键元凶,研究指向了一个可操作的策略:将标准铂类化疗与阻断前列腺素通路的药物配合使用,可能有助于维持强有力的免疫攻击并延缓或预防卵巢癌复发。尽管仍需临床试验验证,这一联合策略为延长现有治疗效益提供了令人鼓舞的新方向。
引用: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
关键词: 卵巢癌, 肿瘤微环境, 化疗耐药, 前列腺素, 免疫疗法