Clear Sky Science · zh
表观遗传背景决定胰腺癌中经典与非经典NF-κB信号转导的转录活性
这项研究对患者为何重要
胰腺癌是最致命的癌症之一,部分原因在于其细胞擅长感知并响应周围环境中的危险信号。本研究考察了两种此类信号——TNFα和TWEAK,揭示了它们如何在癌细胞DNA中开启不同的“读取模式”。理解这些模式可能为减缓肿瘤生长、限制转移并提高治疗效果开辟新的路径。
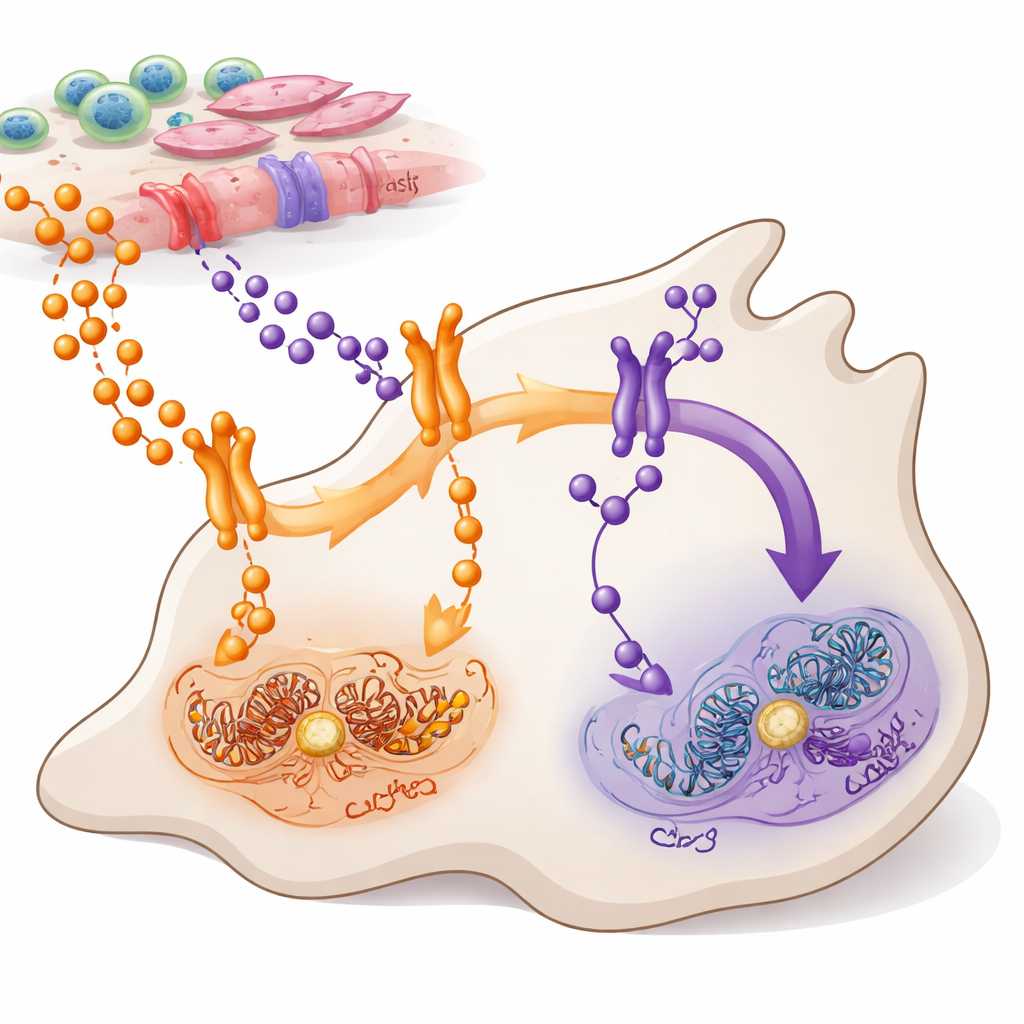
进入癌细胞的两条信息通路
TNFα和TWEAK是肿瘤内外细胞释放的小蛋白信使。它们都会作用于细胞内的一个重要控制系统——NF-κB,该系统帮助决定细胞是增殖、迁移还是死亡。作者把研究重点放在胰腺导管腺癌上,这是胰腺癌中最常见且最具侵袭性的类型,NF-κB在大多数肿瘤中异常活跃。他们绘制了产生TNFα和TWEAK的细胞类型、携带相应受体的细胞,以及这些信号如何通过两个相关的NF-κB分支传导——通常称为经典通路(经RELA)和非经典通路(经RELB)。
谁在肿瘤邻域发送信号
通过将来自患者肿瘤数千个细胞的单细胞RNA测序与高级显微成像相结合,研究团队发现TNFα主要来自免疫细胞,尤其是巨噬细胞以及某些T细胞和B细胞。相比之下,TWEAK由更广泛的细胞群产生:巨噬细胞、成纤维细胞、内皮细胞和星状细胞。它们的受体也不同。肿瘤细胞和其附近的成纤维细胞强烈表达主要的TNFα受体和关键的TWEAK受体。网络分析显示,基于TWEAK的信号在肿瘤细胞与支持细胞之间形成更广泛且更复杂的通信网,而TNFα信号则更集中于富含免疫细胞的区域。
肿瘤细胞内不同深度的反应
在胰腺癌细胞系中,研究人员用TNFα或TWEAK处理细胞,并随时间测量哪些基因被激活。TNFα诱导了快速且广泛的基因激活浪潮,涉及炎症、细胞迁移、组织重塑和存活相关通路。TWEAK则引发了一个较小且更缓慢的变化集合,主要与TNFα的靶基因重叠,而不是启动一套独特程序。这两种信号都能促进细胞迁移并在特定条件下诱导细胞死亡,但在促进迁移方面TNFα效果更强。团队在癌症基因组图谱(TCGA)的患者肿瘤数据中也发现,TNFα或TWEAK水平均高的肿瘤共享许多被激活的基因,证实了这些在人类肿瘤中的模式。
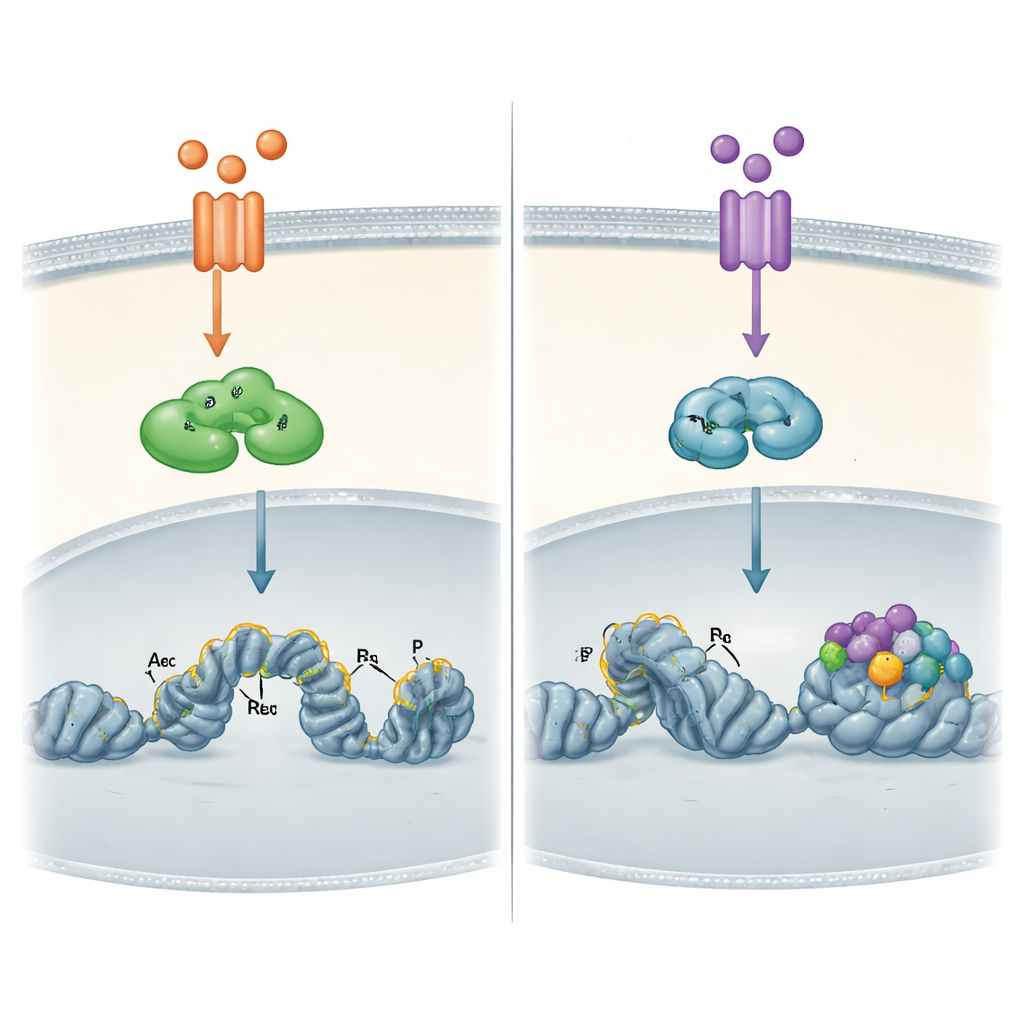
DNA景观如何塑造各条通路
当作者直接观察癌细胞的染色质——即DNA及其相关蛋白的紧密构象时,出现了最显著的差异。通过全基因组结合位点图谱,他们显示TNFα激活的RELA不仅能结合已开放的DNA区域,还能结合更紧密封闭的区域,并通过添加与转录激活相关的化学标记来帮助“打开”这些区域。由TWEAK后期激活的RELB几乎仅结合那些已经可及并装饰着此类活性标记的位点。这些RELB位点特别富含另一个因子家族AP-1的结合基序,表明RELB依赖于其他蛋白先行“准备”环境,才能发挥作用。
这对未来治疗的意义
面向非专业读者,关键结论是TNFα和TWEAK在同一套NF-κB工具箱中发挥着非常不同的作用。通过RELA,TNFα更像一个主开关,能够撬开癌细胞DNA中关闭的片段,激活与生长、存活和扩散相关的广泛基因组。通过RELB,TWEAK更像一位专才,只能在DNA已开放并且存在如AP-1之类的辅助因子时发挥作用。这种分工表明,针对染色质重塑、AP-1或特定NF-κB分支的药物,可能选择性地抑制胰腺癌中的有害基因程序,同时在较大程度上保留其他功能。
引用: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
关键词: 胰腺癌, NF-κB信号传导, 肿瘤微环境, 表观遗传调控, TNF和TWEAK