Clear Sky Science · zh
在乳腺癌治疗中利用焦亡:免疫学机制与新兴生物材料策略
将细胞死亡变为对抗乳腺癌的新武器
乳腺癌仍然是全球最常见且最顽固的癌症之一。许多肿瘤最终会逃避免疫手术、化疗,甚至现代免疫疗法。本文综述探讨了一个新兴思路:在乳腺肿瘤内有意触发一种被称为焦亡的“燃烧式”细胞死亡。通过以可控且有炎性反应的方式使癌细胞破裂,科学家希望既能直接杀死肿瘤,又能激活免疫系统共同参与清除。
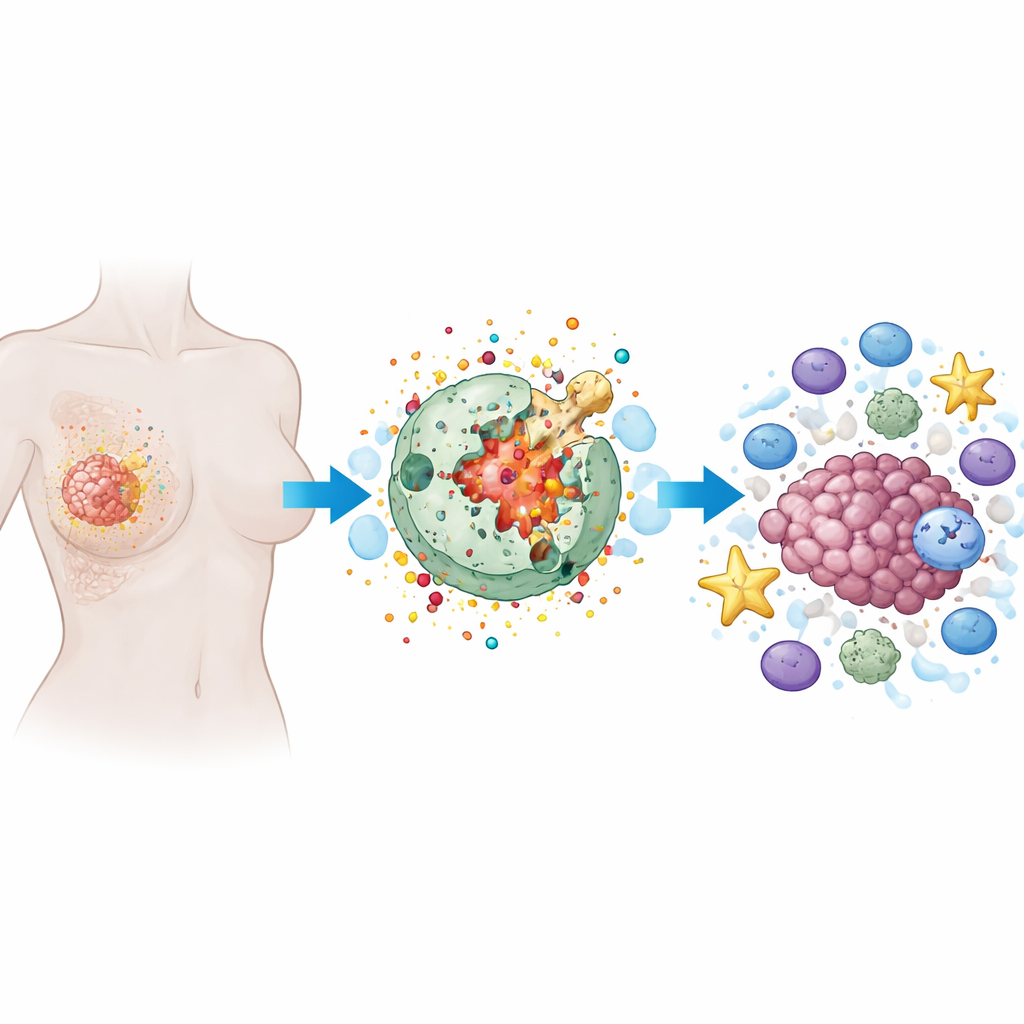
一种“燃烧式”细胞死亡是如何发生的
焦亡是一种程序性细胞死亡,细胞肿胀、外膜出现大量孔洞并最终破裂,细胞内物质外泄。与许多治疗中见到的安静、整洁的细胞死亡不同,焦亡是喧闹且带有炎性的。特殊蛋白,尤其是一类称为气体凝胶(gasdermin)的家族,像微小的爆破装置。一旦被细胞内的酶切割,气体凝胶蛋白就在细胞膜上打出孔洞。这不仅摧毁了癌细胞,还释放出警报信号和炎性分子,能招募并激活免疫细胞。
为什么乳腺肿瘤是一个特殊挑战
乳腺癌并非单一疾病,而是由具有不同行为特征的亚型组成。其中一些,如三阴性乳腺癌,缺乏常见的药物靶点且常对治疗产生耐受性。许多乳腺肿瘤被认为是“免疫学上冷”的,意味着肿瘤内部活跃的免疫细胞很少。综述解释了乳腺肿瘤环境的特征——包括基质细胞、免疫抑制性细胞和局部缺氧——如何既为焦亡的发生创造条件,又在控制不当时将其炎性反应变成肿瘤生长和转移的燃料。这种双刃性使得精准控制尤为重要。
肿瘤细胞内的气体凝胶开关
文章的核心主题之一是不同气体凝胶蛋白如何在乳腺癌细胞内充当分子开关。像GSDMD和GSDME的亚型可以将化疗、放疗或免疫细胞的攻击信号转化为全面的焦亡反应。其他如GSDMC和某些形式的GSDMB在侵袭性肿瘤中常表达更高,其作用可能根据激活方式而促进或抑制疾病进展。许多乳腺癌通过化学方式沉默GSDME,从而削弱焦亡和免疫激活。恢复或选择性触发恰当的气体凝胶蛋白,可能决定一种治疗是仅仅杀死少数细胞,还是将整个肿瘤转变为一种体内疫苗以唤醒免疫系统。
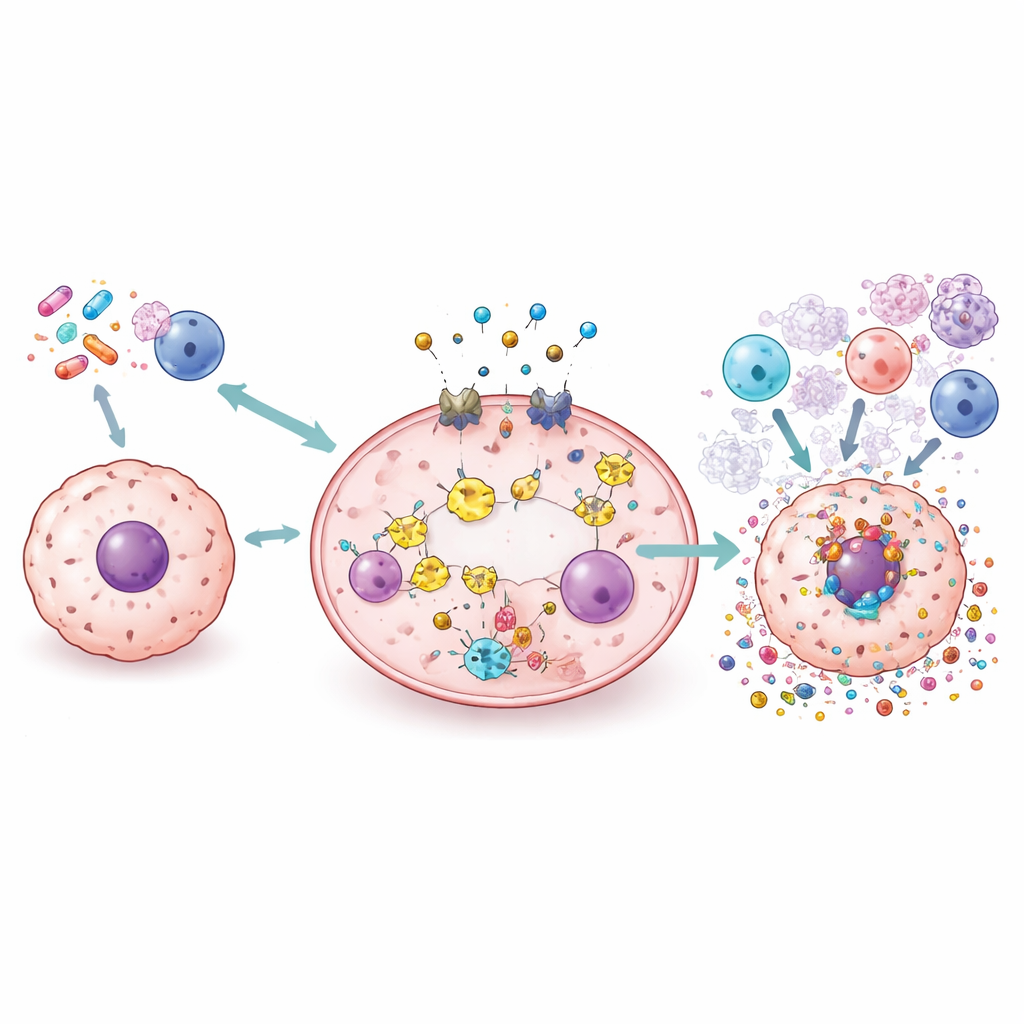
新工具:药物、纳米颗粒、病毒与放疗
综述综览了为安全利用焦亡而研究的多种策略。顺铂和多柔比星等常规药物可以重新定位或重新配方,使癌细胞倾向于由气体凝胶驱动的破裂而非宁静死亡。小分子可放大或阻断通路的某些环节以微调炎性反应。纳米颗粒与仿生载体被设计用于将化疗药物、铜离子或光活化分子直接输送到肿瘤内,在那里诱导焦亡并尽量减少对健康组织的损伤。噬瘤病毒和放疗也可以被工程化或与其他试剂组合,以诱发焦亡并重塑肿瘤免疫格局,可能使免疫检查点抑制剂更有效。
在强效益处与实际风险之间取得平衡
由于焦亡高度炎性,帮助免疫系统抗癌的相同反应也可能损伤正常组织,或在长期存在时反而促进肿瘤生长。作者强调了早期生物标志物——例如基因表达谱、甲基化模式、血液中气体凝胶蛋白片段和细胞因子谱——这些标志物可能有助于识别哪些患者最可能受益、哪些患者面临危险的“细胞因子风暴”。先进的纳米医学设计、精心挑选的药物组合以及对炎性标志物的实时监测,都是用来保持反应高效但可控的研究方向。
这对未来患者可能意味着什么
简言之,这篇综述认为,让癌细胞“响亮地死亡”可能改变乳腺癌的治疗。通过在特定肿瘤细胞亚群中精确触发焦亡,医生既可能缩小肿瘤,又能唤醒强大且持久的免疫反应,将冷肿瘤转为对现代免疫疗法更敏感的热肿瘤。然而,焦亡是一个易变的盟友:若释放过于广泛或持续过久,可能加剧炎症或鼓励耐药细胞存活。未来研究将集中于绘制谁能从中受益、完善靶向递送系统以及开展将诱导焦亡的方法与免疫药物配对的临床试验。如果这些挑战能够被解决,利用焦亡可能为乳腺癌治疗增加一种强有力的新维度。
引用: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
关键词: 焦亡, 乳腺癌, 气体凝胶蛋白, 肿瘤微环境, 纳米医学