Clear Sky Science · zh
绝对的动态与相对的静态:糖酵解与氧化磷酸化在癌症发展中的关系
为何癌细胞的能量选择至关重要
癌细胞像极端的耐力运动员:它们必须持续供能以生长、扩散并躲避免疫或治疗。本文综述解释了肿瘤细胞如何利用两种主要能量系统——一种快速、一种高效——更重要的是,说明它们如何混合并在两者之间切换。理解这些不断变化的能量策略,为在疾病全过程中诊断和治疗癌症提供了新的思路。
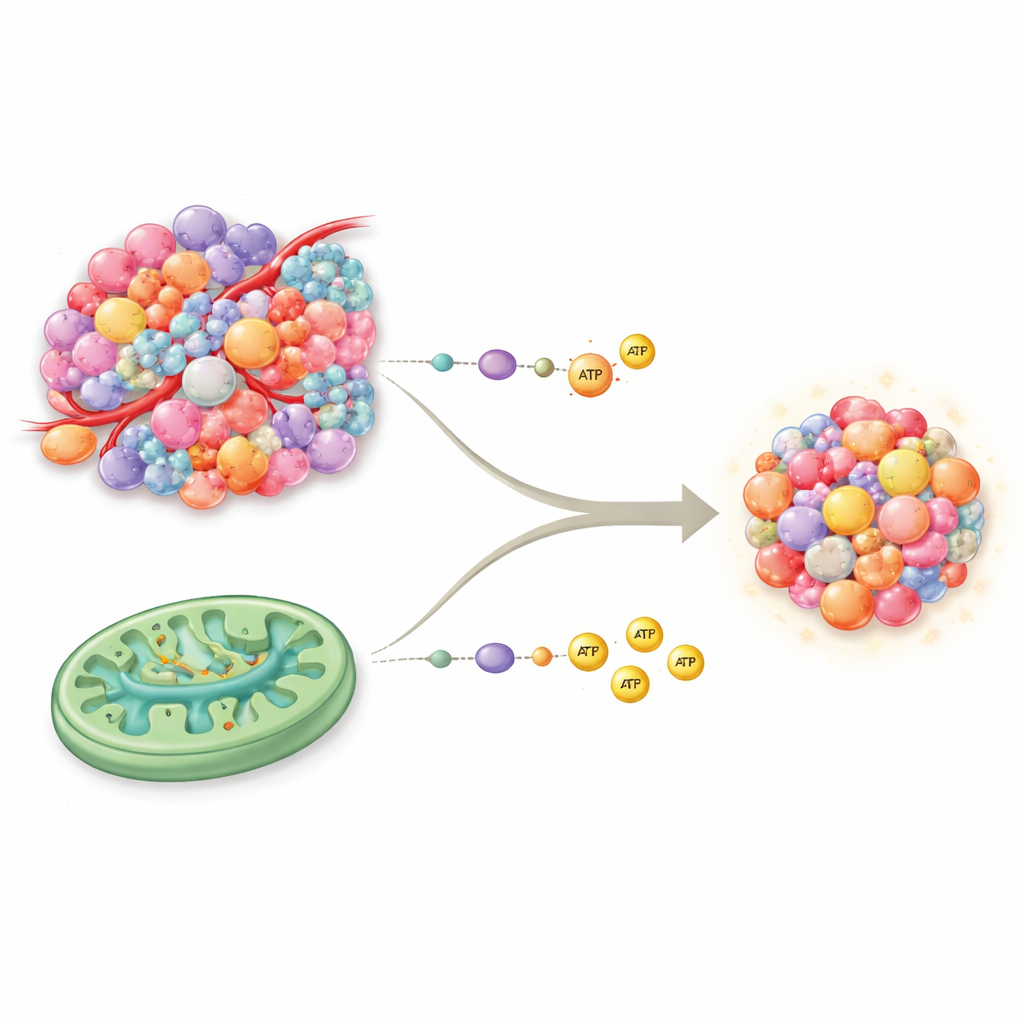
细胞产生能量的两条主路
我们的细胞通常通过两条核心通路产生能量。糖酵解是快捷的“现款”系统,能迅速分解糖类,但单位产能相对较低。氧化磷酸化(OXPHOS)在线粒体内进行,更像高效的发电厂,能产生更多能量但需要充足的氧气和营养供应。数十年来,人们认为癌细胞几乎完全依赖糖酵解,即便在有氧情况下也是如此——这就是著名的瓦伯格效应。新的证据推翻了这一简单观点:许多肿瘤具有正常功能的线粒体,能够在糖酵解之外同时利用OXPHOS和三羧酸循环(TCA),赋予它们比此前认识更丰富、更灵活的能量工具箱。
多种细胞类型,多种能量选择
肿瘤并非单一的肿块,而是一个小型生态系统,包含癌细胞、支持细胞、血管和免疫细胞等,各自有不同的能量需求。有些癌细胞靠近血管,氧气与营养充足;另一些则深处供给不足的区域。因此,同一肿瘤内的细胞可能偏好糖酵解、主要依赖OXPHOS,或两者兼用。这种代谢多样性——称为异质性——源自血流、营养水平、细胞类型及周围环境信号的差异。除此之外,肿瘤常表现出代谢共生:进行糖酵解的细胞将乳酸作为类似废物外排,邻近依赖OXPHOS的细胞则摄取并氧化这些乳酸作为有价值的燃料。类似的乳酸共享也发生在癌细胞与成纤维细胞、血管细胞以及免疫抑制细胞等支持细胞之间,共同帮助肿瘤生存并抵抗治疗。
永远在变:肿瘤能量随时间的转变
肿瘤代谢不仅在同一时间点上多样,而且高度动态。随着肿瘤生长,它们会遭遇氧气不足、酸性堆积、营养匮乏和组织硬度变化等不断改变的条件。在恶劣的低氧环境下,许多癌细胞会向糖酵解转移;在酸性堆积或糖类匮乏时,它们可能再次转向更多依赖OXPHOS。相同的灵活性也出现在关键生物学阶段:快速分裂的细胞倾向于依赖糖酵解以产生新DNA、脂质和膜所需的构建模块;处于静止或循环于血液中的细胞则常更多依赖OXPHOS。在侵袭与转移过程中,癌细胞反复调整其能量选择:某些步骤有利于糖酵解,另一些则偏向OXPHOS,而成功在新器官定植的转移细胞会将代谢调谐以适应目的地组织的“土壤”。
驱动切换的基因、酶与“发电厂”
在细胞的内部机器中,基因和酶引导着这些能量决策。癌基因和肿瘤抑制子可以推动细胞偏向糖酵解或OXPHOS,或使两者同时提升。关键TCA酶的突变或异常——例如处理柠檬酸、琥珀酸或异柠檬酸的酶——可以倾斜代谢平衡,有时推动促癌信号如血管生成和侵袭。位于关键代谢交叉点的酶——例如决定糖源碳是用于能量还是用于构建物质的丙酮酸激酶M2——将糖酵解与线粒体功能联系起来。与此同时,不同肿瘤区域线粒体的数量、结构与性能差异,进一步扩展了可能的能量状态谱系。
通过流动的能量靶点重新审视治疗
由于肿瘤细胞可以在糖酵解与OXPHOS之间切换,仅仅阻断一条通路通常不足以根除它们;癌细胞可能改道其燃料使用并存活。作者认为,肿瘤的能量代谢只是短暂稳定,并且在本质上不断变化。他们建议将肿瘤视为一个需要随时间测量的“能量代谢谱”,而非一次性评估。实践上,这可能意味着在不同疾病阶段追踪肿瘤的燃料偏好,并以组合方式个体化地配对糖酵解和OXPHOS抑制剂。这类动态的、以代谢为导向的治疗策略,或许能更有效切断肿瘤的能量供应,限制其适应能力,并改善疾病的长期控制。
引用: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
关键词: 癌症代谢, 糖酵解, 氧化磷酸化, 肿瘤微环境, 代谢可塑性