Clear Sky Science · zh
通过TGF-β,APOA2介导的内皮间质转化与癌细胞脂质代谢重编程赋予抗血管生成药物耐药性
这一发现对患者为何重要
医生越来越多地使用通过切断肿瘤血供来“饿死”肝脏肿瘤的药物,但许多患者在初期获益后肿瘤又停止响应。本研究提出了一个紧迫的问题:为何有些肝癌会对这些阻断血管的治疗产生耐药,且我们如何能破解它们?研究人员发现了一种血脂蛋白与一条强大生长信号之间的隐秘协作,这使肿瘤既能重塑其血管又能重编程能量利用,指向了一条治疗难治性肿瘤的不同路径。
学会在没有常规生命线下生存的肿瘤
肝细胞癌是最常见的肝癌类型,生长高度依赖新生血管。晚期疾病的标准药物旨在阻断以VEGF及其受体VEGFR2为核心的关键血管生成通路。然而在许多患者中,肿瘤在这些药物面前仍能继续生长。通过比较对抗血管生成药物阿帕替尼有反应和无反应患者的肿瘤样本,作者发现有一个基因APOA2格外突出。来自耐药患者的肿瘤中APOA2水平明显更高——该蛋白以在血液中运输脂质而闻名。这提示APOA2可能帮助肿瘤逃避以血管为靶的药物。
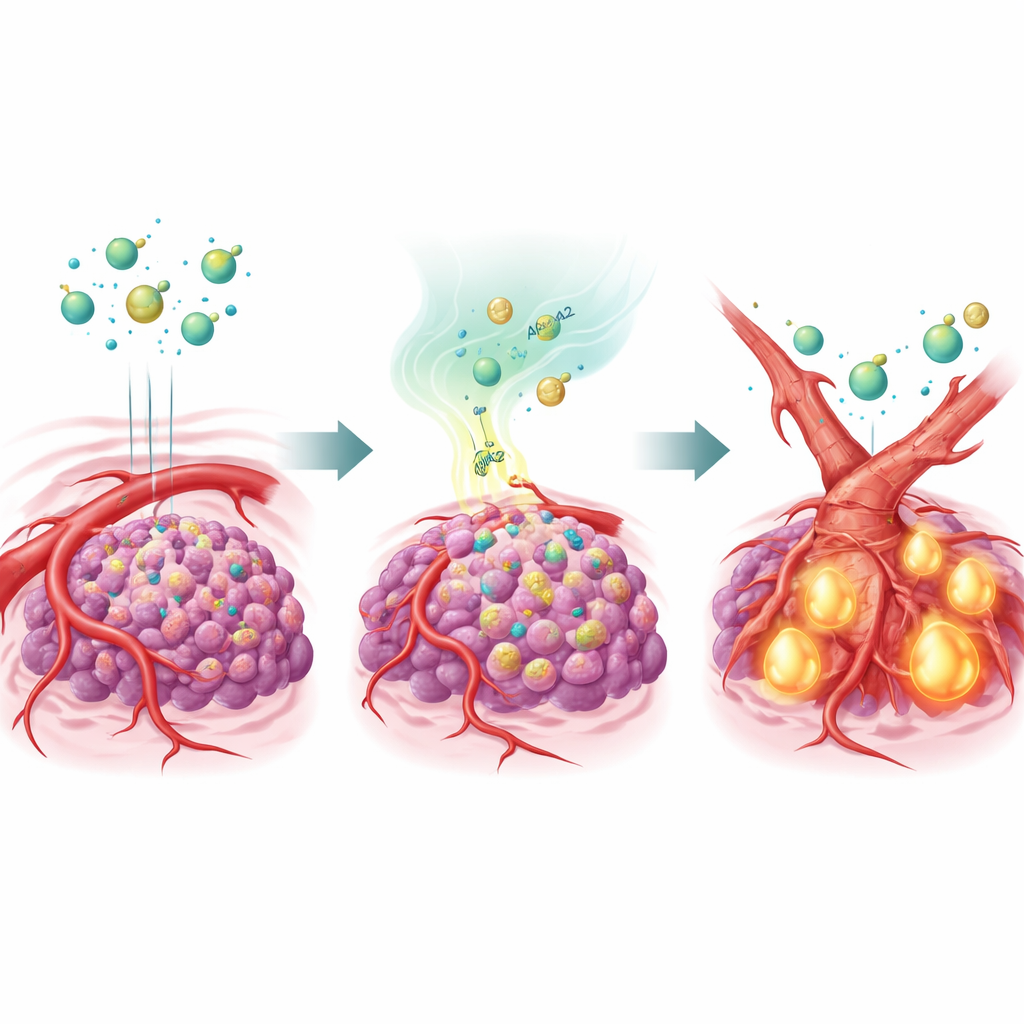
一种重塑血管的脂质运输蛋白
为验证这一假设,研究组使肝癌细胞过表达APOA2并将其移植入小鼠体内。在用多种抗血管生成药物治疗时,这些高APOA2肿瘤基本不受抑制:其血管持续存在,肿瘤继续生长。详细分析显示,一种名为TGF-β的主控信号在这些肿瘤中被强烈激活,其水平在肿瘤微环境和动物血液中均升高。TGF-β作用于血管内皮细胞,推动它们发生一种称为内皮-间质转化(endothelial-to-mesenchymal transition,EndMT)的身份改变。当这些细胞向更像瘢痕的间质样状态转变时,它们丧失了大量VEGFR2——正是抗血管生成药物要作用的靶点。实际上,血管被重塑成药物无法再识别的形式。
保持癌细胞能量的代谢绕道
故事并没有在血管壁停住。由APOA2驱动的同一TGF-β信号也重编程了癌细胞的能量获取方式。APOA2高表达的细胞不再主要依赖糖酵解,而是从周围环境中摄取更多游离脂肪酸,并在线粒体中通过脂肪酸氧化(FAO)燃烧这些脂肪。通过测量营养物利用与耗氧量的实验显示,这些细胞对脂质作为能量来源的依赖性增强,细胞内可用能量(ATP)增加。这一转变使肿瘤细胞即便在抗血管生成治疗削弱血供的情况下仍能快速分裂并避免死亡。
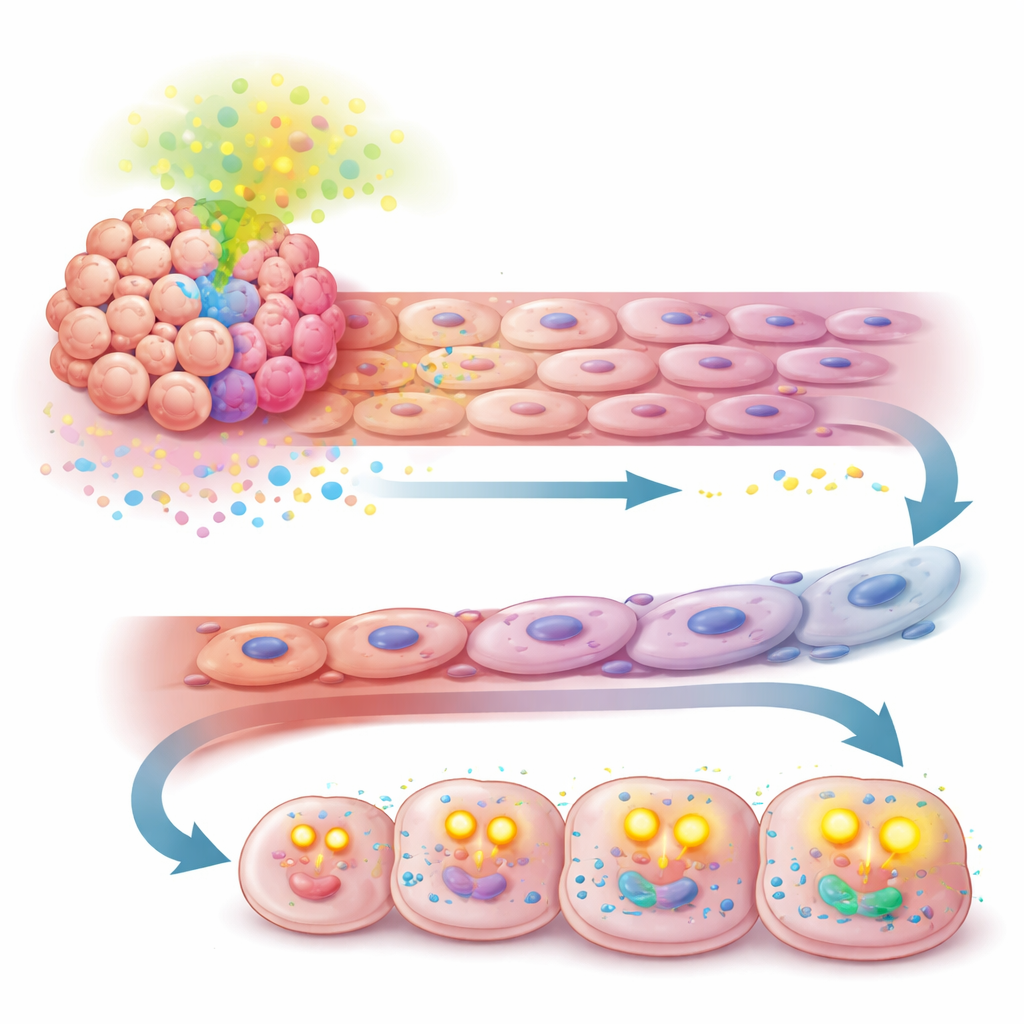
将弱点变为新的治疗靶点
关键的是,当研究者阻断TGF-β时,APOA2带来的优势便被瓦解。在小鼠模型中抑制该信号可减少异常的血管改变、恢复对治疗的敏感性并减缓肿瘤生长。更有希望的是,一种同时阻断TGF-β和免疫检查点PD-1的双功能抗体在APOA2高表达肿瘤中比单独方法效果更佳。这些结果表明,在一部分以高APOA2为标志的肝癌中,疾病已悄然将依赖性从通常的VEGF通路转向以TGF-β为中心的途径,以维持血管和肿瘤代谢两方面。
这对未来肝癌护理的意义
对普通读者来说,关键信息是:一些肝肿瘤通过同时重接管它们的“管道”和“能源供应”来逃避现有的抗血管生成药物。一种与脂质相关的蛋白APOA2增强了TGF-β信号,进而让血管“伪装”起来,使现有药物无法识别,同时教会癌细胞更依赖脂肪而非糖来维持生存。研究表明,对肿瘤进行APOA2检测可能帮助筛选出不太可能从标准抗血管生成药物获益但可能对阻断TGF-β的药物(尤其与现代免疫疗法联合使用)有反应的患者。简言之,通过揭示肿瘤如何适应,这项工作指向了一种更为个体化的策略,既打击血管也切断这些顽强肿瘤依赖的能量来源。
引用: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
关键词: 肝细胞癌, 抗血管生成耐药, APOA2, TGF-β信号, 癌症脂质代谢