Clear Sky Science · zh
肌肉激素Irisin通过SIRT1/RANBP2/FTO信号轴抑制骨髓间充质干细胞的脂肪分化并保护骨质疏松
为什么肌肉激素对脆弱骨骼很重要
骨质疏松看似只是“骨头脆弱”的简单问题,但在我们骨骼深处,一场悄然的拉锯战正在进行。骨髓中的相同干细胞可以分化为造骨细胞或脂肪细胞。随着年龄增长,尤其在绝经后,这一平衡倾向于产生更多脂肪,从而使骨骼变薄更易骨折。本研究探讨了一种由运动肌肉释放的激素——irisin,如何将这些干细胞重新引导向造骨而非形成脂肪,提示未来运动相关激素或可成为防治骨质疏松的途径。
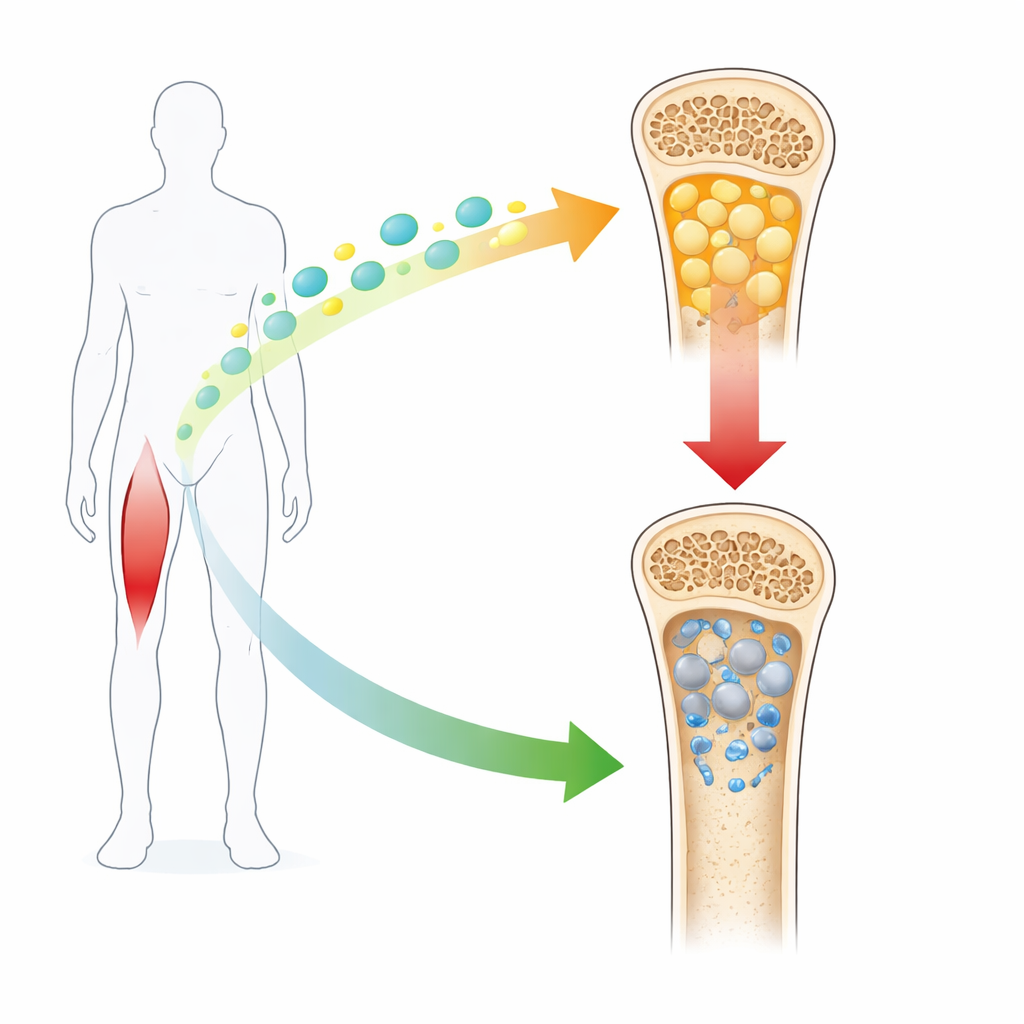
当骨变成脂肪时
骨髓并非空洞,而是干细胞活跃的工作间,这些细胞可以选择不同的命运。在健康成人中,足够多的细胞分化为造骨细胞以维持骨骼强度。在骨质疏松,特别是绝经后女性中,更多的这些细胞转向脂肪储存细胞。这种“骨髓肥胖”与脆弱的骨骼和骨折密切相关。研究人员首先确认,这种向脂肪转变伴随着irisin水平下降——在雌激素缺失的小鼠和患有骨质疏松的人类患者中均可观察到,将激素下降与骨健康恶化联系起来。
与运动相关的信号的双重作用
Irisin由运动时的肌肉释放,已被研究其对代谢和能量使用的影响。本文研究团队询问irisin是否也参与决定骨髓干细胞走向脂肪或骨的命运。在体外实验中,他们向小鼠骨髓间充质干细胞添加irisin并观察结果。Irisin增强了细胞向造骨分化的能力,增加了矿化沉积和关键骨生成基因的活性。同时,它强烈抑制了向脂肪细胞的转变,减少脂滴并下调驱动脂肪形成的基因和蛋白。在切除卵巢以模拟绝经后骨量流失的活体小鼠中,每周注射irisin可保持骨量和微结构,并减少髓腔内脂肪积聚。
细胞决策机制内部
为理解irisin如何行使这种控制,研究人员考察了在干细胞暴露于irisin以促脂肪形成时基因活性的变化。其中一个突出因子是SIRT1,一种已知调节衰老、代谢和应激反应的蛋白。团队展示了降低SIRT1会使细胞更易向脂肪分化,而增强SIRT1则有相反效果。重要的是,当SIRT1被抑制时,irisin便无法有效阻断脂肪形成——在细胞和小鼠中均是如此——表明SIRT1是irisin骨保护信号的关键中继。
使“脂肪”蛋白失去作用的分子链
进一步研究聚焦于另一种与肥胖和脂肪储存相关的蛋白FTO。高水平的FTO支持脂肪细胞发展,部分原因是它稳定了脂肪主调控子PPARγ。研究人员发现SIRT1并不改变FTO的基因表达量,而是影响FTO蛋白的稳定性。Irisin激活的SIRT1提高了第三种蛋白RANBP2的活性,RANBP2以一种标记方式对FTO进行修饰,使其走向降解。当RANBP2被降低时,SIRT1无法再降低FTO蛋白水平,脂肪形成随之回升。通过这一链条——irisin至SIRT1,SIRT1至RANBP2,RANBP2促使FTO降解——细胞由趋向脂肪的命运回转为造骨角色。
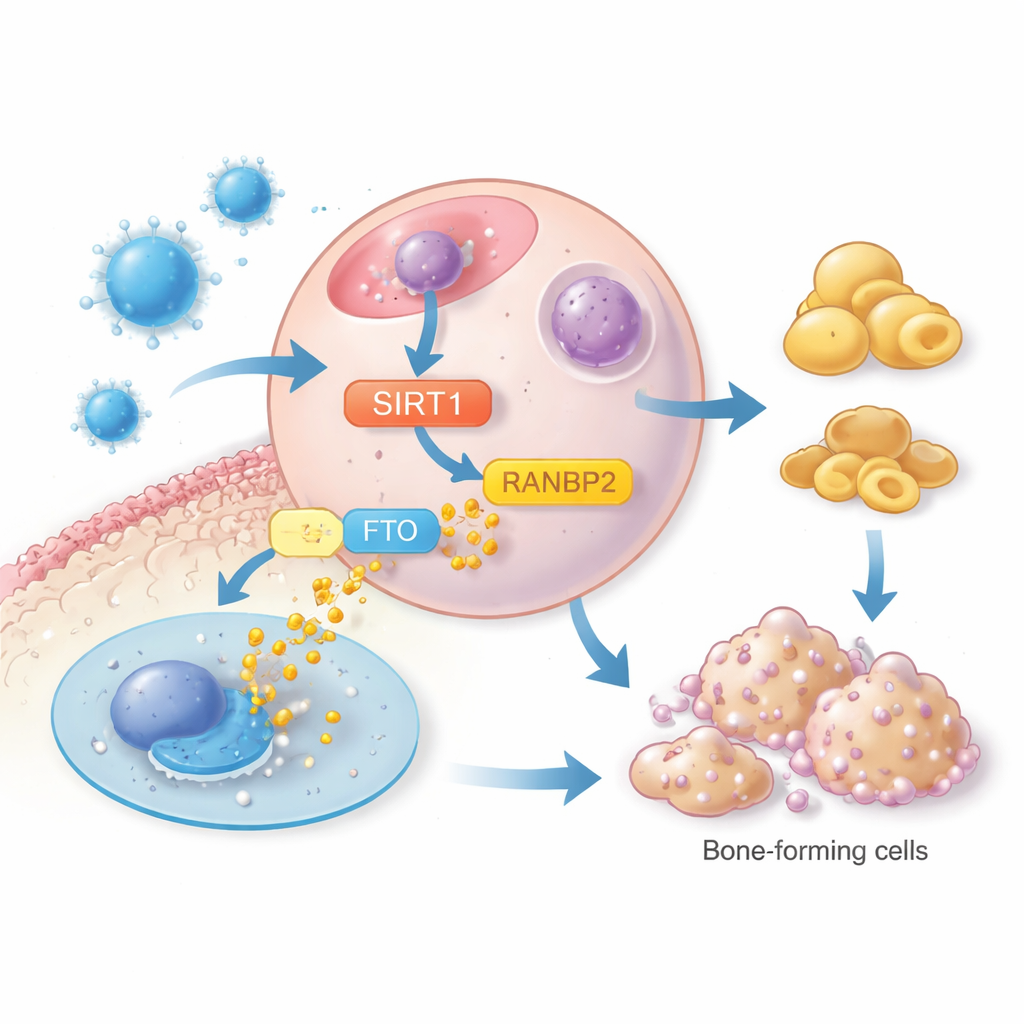
这对未来骨骼护理的意义
通过描绘这一逐步通路,研究将irisin展示为不仅仅是一个简单的运动激素。它在骨髓中承担分子“交通指挥”的角色,通过SIRT1–RANBP2–FTO信号轴将干细胞从脂肪分化引导回造骨方向。对非专业读者而言,这意味着维持或模拟体内天然的irisin信号,有朝一日可能成为预防或治疗骨质疏松的策略,补充像运动这样的生活方式干预。尽管仍需在更大规模的人体研究中进一步验证,这些发现为保持骨骼更强壮提供了一组有前景的分子靶点。
引用: Chen, J., Liu, J., Fu, Q. et al. Irisin inhibits adipogenic differentiation of bone marrow mesenchymal stem cells through the SIRT1/RANBP2/FTO signaling axis and protects against osteoporosis. Cell Death Discov. 12, 114 (2026). https://doi.org/10.1038/s41420-026-02976-5
关键词: 骨质疏松, irisin, 骨髓干细胞, 骨脂平衡, SIRT1信号