Clear Sky Science · zh
KCTD1 稳定 c-Myc 以上调 PD-L1 并在肝细胞癌中抑制抗肿瘤免疫
这对未来癌症治疗为何重要
许多肝癌患者无法从当今最令人振奋的免疫治疗中获益,这些疗法旨在释放机体自身的 T 细胞去攻击肿瘤。本研究探讨了为何一种主要类型的肝癌——肝细胞癌,即便在治疗期间仍能逃避免疫攻击,并识别出一个新的分子开关 KCTD1,可能使现有免疫治疗药物更有效。
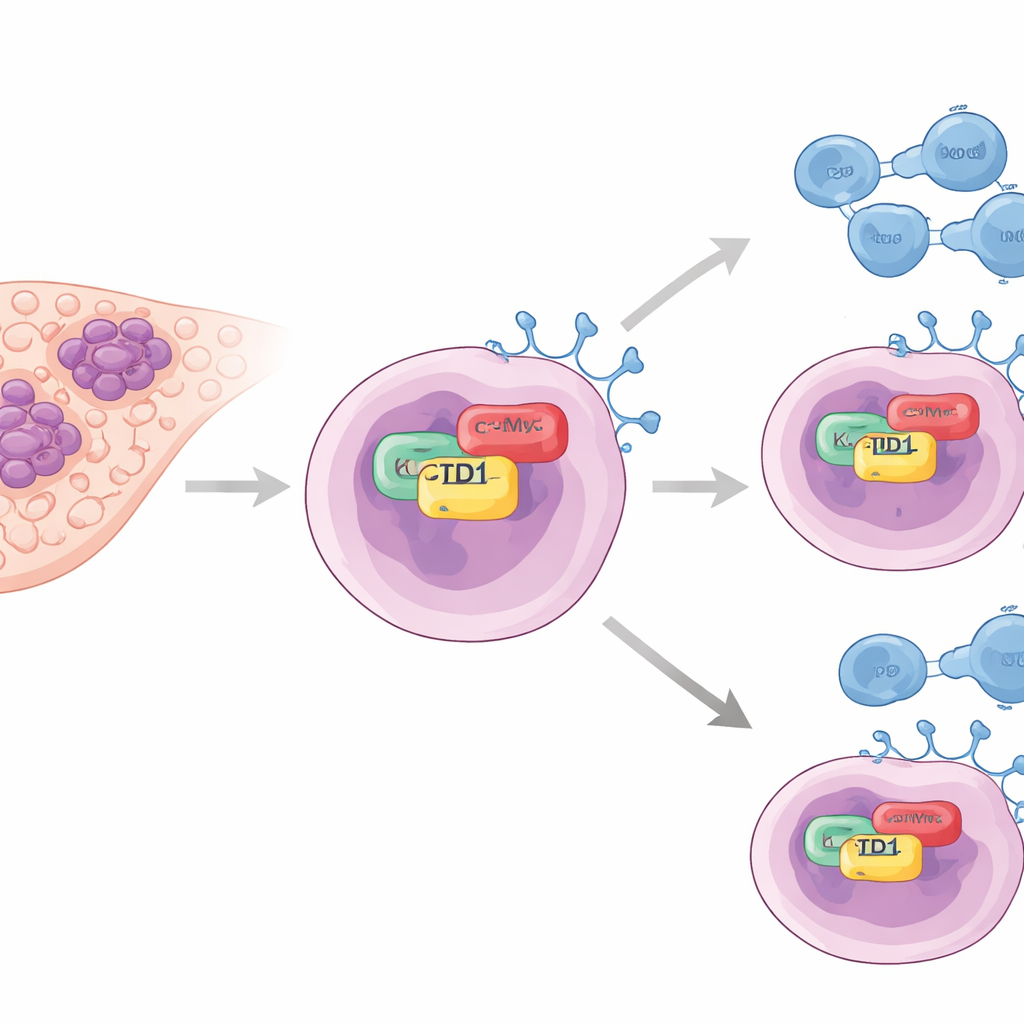
肿瘤“关闭开关”的隐秘帮手
作者将注意力集中在一种名为 KCTD1 的蛋白上,先前曾与肝肿瘤生长相关但在免疫逃逸方面研究不多。在患者的肿瘤样本中,他们发现 KCTD1 在癌变肝组织中的表达显著高于正常肝组织。重要的是,富含 KCTD1 的肿瘤同时伴有较高水平的 PD-L1——一种在癌细胞表面表达的蛋白,可结合 T 细胞上的 PD-1,从而实质上告诉免疫系统撤退。肿瘤中 KCTD1 低的患者通常存活时间更长,提示该蛋白与疾病严重度及肿瘤免疫屏障的强度相关。
在癌细胞内连接分子线索
为了解 KCTD1 如何促进 PD-L1 表达,团队在体外培养的肝癌细胞系中开展实验。当他们减少 KCTD1 时,PD-L1 蛋白水平下降且剩余的 PD-L1 更快降解,这表明 KCTD1 帮助稳定 PD-L1,而不仅仅是激活其基因表达。通过生化拉下实验和荧光显微镜观察,他们显示 KCTD1 在细胞核内与另一重要致癌驱动蛋白——致癌蛋白 c-Myc 发生物理结合。该相互作用通过两种蛋白的特定接触区域实现,并导致 c-Myc 更加稳定,从而增强 PD-L1 的产生。当单独降低 c-Myc 时,即便 KCTD1 丰富,PD-L1 仍会下降,表明 c-Myc 是 KCTD1–c-Myc–PD-L1 链条中关键的中间环节。
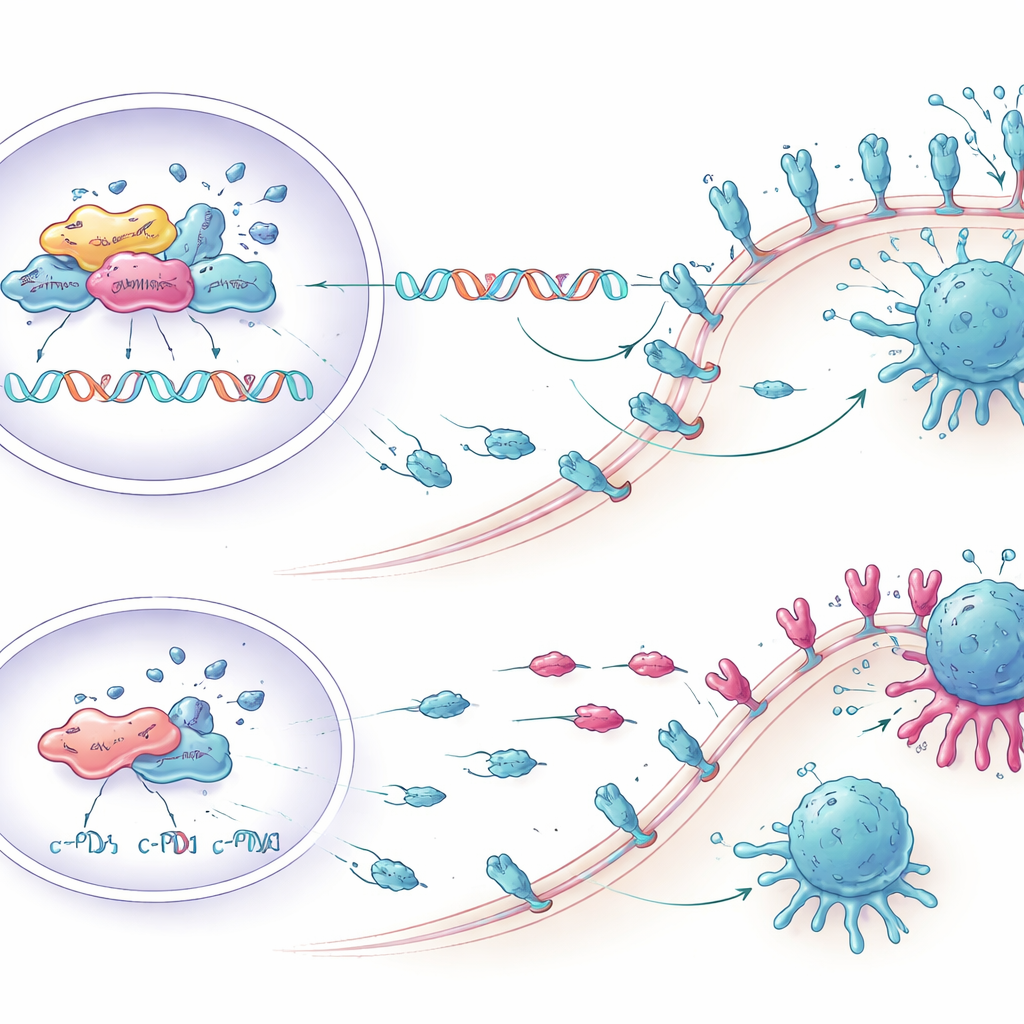
在实验室中重新激活 T 细胞
研究者接着探究降低 KCTD1 是否能实际增强免疫攻击。他们将人源肝癌细胞与来自献血者的免疫细胞共同培养。被工程化降低 KCTD1(因而 PD-L1 较少)的肿瘤细胞,触发了 CD8 T 细胞——免疫系统中主要的肿瘤杀伤细胞——更强的反应。更多的这些 T 细胞产生了 TNF-α 和干扰素-γ 等炎性分子,显示出更高的增殖和激活标志,并表现出较少的耗竭特征。因此,当抑制 KCTD1 时,更多肿瘤细胞进入程序性细胞死亡,表明分子变化转化为免疫杀伤的实际增益。
在小鼠体内检验该机制
为观察在生物体内是否存在相同模式,团队将缺失 KCTD1 的小鼠肝癌细胞直接植入小鼠肝脏。KCTD1 降低的肿瘤形成的结节更少且更小,细胞分裂速度较慢,且更多癌细胞进入凋亡。这些肿瘤也表达更少的 c-Myc 和 PD-L1。若去除小鼠体内的 CD8 T 细胞,这些益处大部分消失,表明肿瘤增速放缓在很大程度上依赖于 T 细胞活性。最后,当研究者将 KCTD1 敲低与抗 PD-1 抗体(现有的一类免疫检查点药物)联合使用时,小鼠显示出最小的肿瘤负担以及最高水平的 CD4 和 CD8 T 细胞浸润肿瘤。
这对患者可能意味着什么
总体而言,该工作揭示了 KCTD1 是一个核心协调因子,它稳定 c-Myc、提升肝癌细胞表面的 PD-L1,并削弱 CD8 T 细胞的攻击。破坏这一路径使肿瘤对免疫系统更脆弱,并在小鼠中提高对 PD-1 阻断药物的反应。对患者而言,这提示未来可将针对 KCTD1 或其与 c-Myc 接触面的药物与现有免疫疗法配合使用,帮助更多肝癌患者从持久的免疫控制中获益。
引用: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
关键词: 肝细胞癌, 肿瘤免疫治疗, PD-1 PD-L1 通路, c-Myc 信号, T 细胞抗肿瘤免疫