Clear Sky Science · zh
金属硫蛋白‑2A在椎间盘退变中的保护性上调通过激活PI3K/AKT/mTOR通路抑制髓核细胞铁死亡
为什么这种背部问题重要
下腰痛影响全球数亿人,是致残的主要原因之一。一个重要罪魁祸首是位于脊椎骨之间的缓冲结构——椎间盘的逐渐退化。本研究提出了一个充满希望的问题:机体自身的保护分子能否帮助保护这些椎间盘免受损伤?增强这些分子是否能为慢性腰痛带来新的治疗思路? 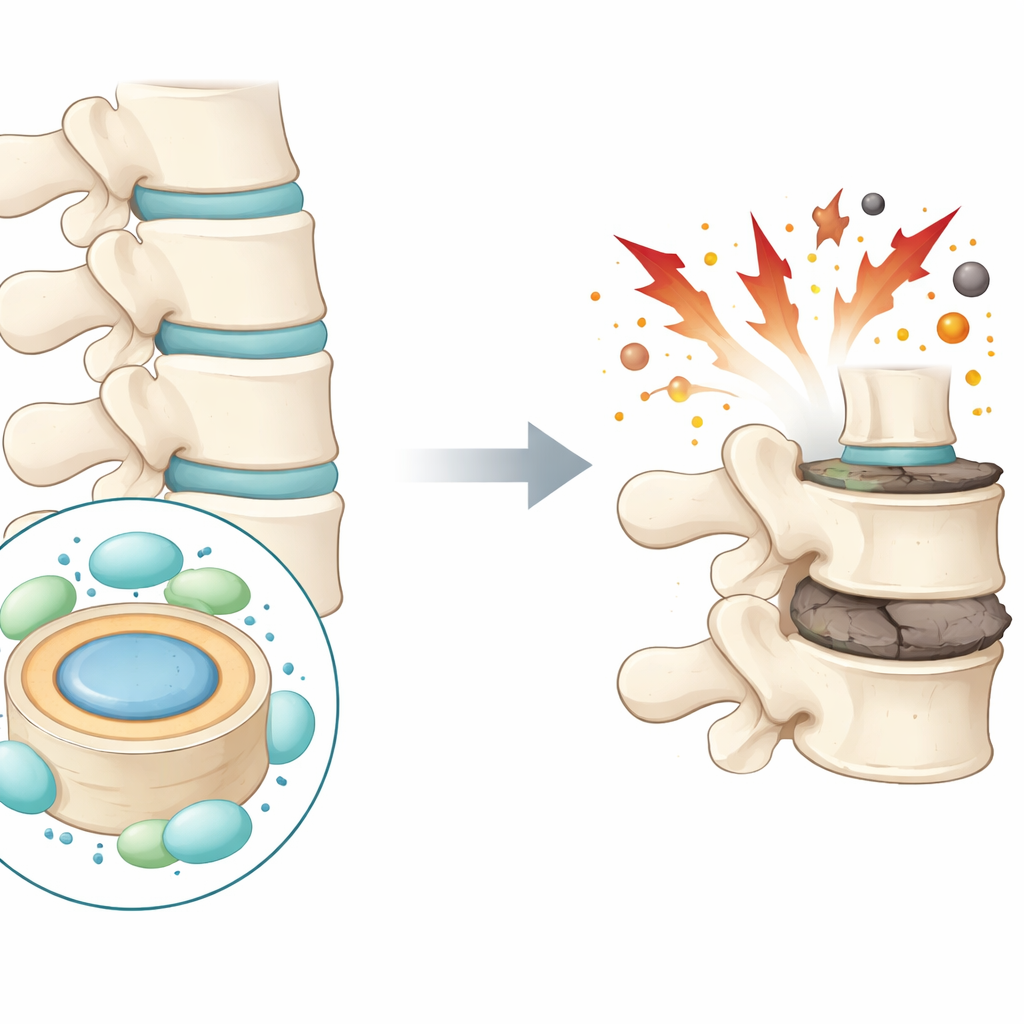
脊柱内部的缓冲垫
每个椎间盘都有一个柔软、凝胶状的中心,称为髓核,外面被较坚韧的纤维环包绕。这些结构像脊柱的减震器一样工作。随着椎间盘退变,中间区域的细胞死亡,支撑的蛋白质和水分基质逐渐流失。椎间盘变扁并出现裂隙,可能导致疼痛和活动受限。作者关注一种最近在多种疾病中才受到注意的特定细胞死亡类型:以铁为驱动、与氧化相关的死亡,称为铁死亡。他们怀疑这一过程在椎间盘破坏中起关键作用。
当铁与氧化失控
铁死亡由细胞内游离铁和活性氧分子积累触发,损伤细胞膜中的脂质,特别是小型能量工厂——线粒体。研究团队分析了人类椎间盘组织的单细胞基因数据,发现退变椎间盘中铁死亡相关基因发生明显改变。尤其是通常保护细胞免受此类损伤的标志物,如酶GPX4,在患者和大鼠的退变椎间盘中均减少。与此同时,促进损伤和炎症的标志物增多,勾勒出随着椎间盘退变细胞遭受氧化攻击的图景。
一种内建的金属结合保护因子
在众多在病变椎间盘中变化的基因中,有一个特别显眼:金属硫蛋白‑2A(MT2A),一种能结合锌等金属并清除有害活性分子的短小蛋白。MT2A在更严重退变的人类椎间盘和大鼠椎间盘损伤模型中明显升高。乍看之下这似乎矛盾——为什么保护性分子在受损组织中会增加?研究人员假设机体正在发起一种代偿性反应,试图对抗铁驱动的应激激增。在体外实验中,当椎间盘细胞暴露于模拟氧化应激的化学物质时,随着细胞健康恶化,MT2A水平上升,进一步支持它作为一种防御被启动的观点。
关闭与开启保护开关
为检验MT2A究竟是有保护作用还是有害,团队在人体椎间盘细胞中精细调控其表达水平。当他们抑制MT2A产生时,氧化应激引起的细胞死亡大幅增加,铁积累更多,脂质损伤更强,线粒体严重受损。相反,提升MT2A或用已知的铁死亡抑制剂处理细胞,许多问题得到缓解:铁与活性分子下降,保护性抗氧化物恢复,线粒体形态更健康。这些变化也反映在对细胞支撑基质蛋白的更好保存上,而这些基质蛋白对维持椎间盘饱满和功能至关重要。 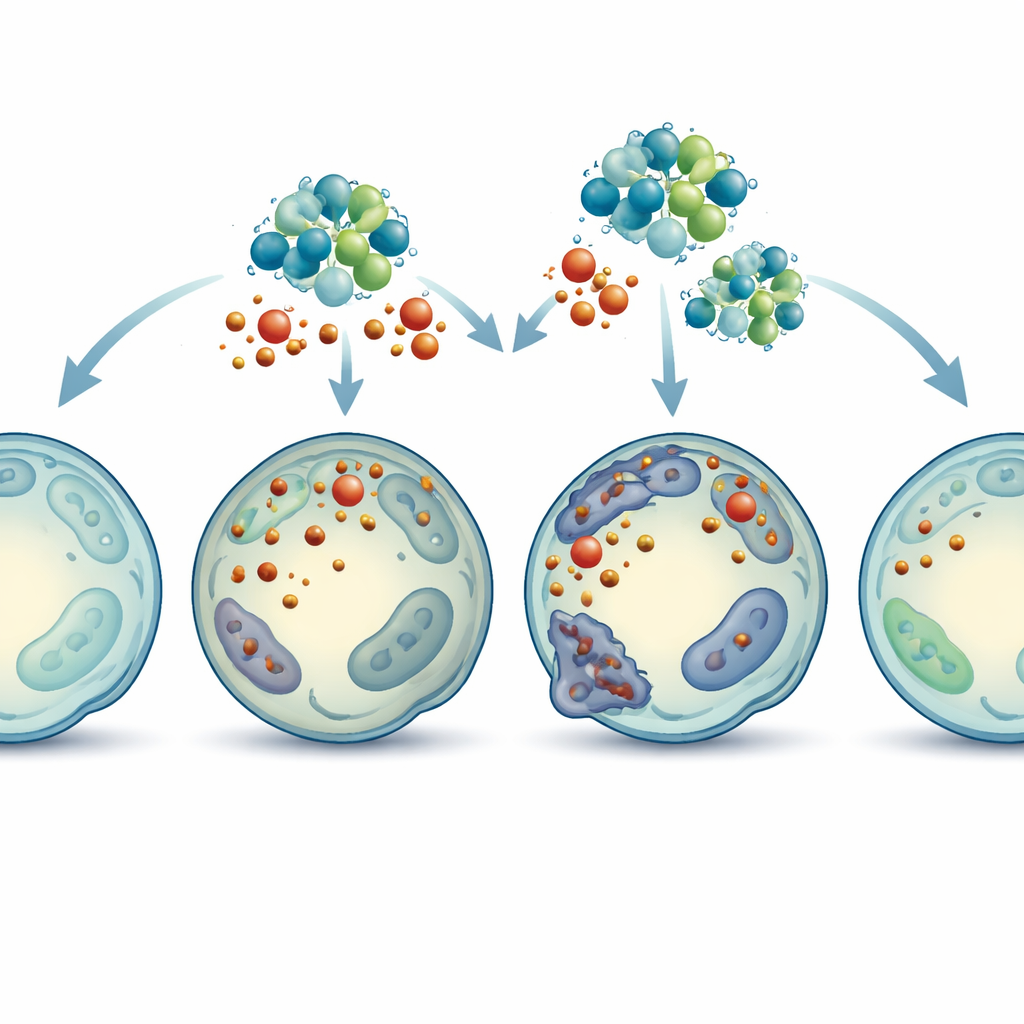
细胞内的一条关键信号通路
进一步研究表明,MT2A如何在细胞内部传递保护信号。基因测序和蛋白质检测指向PI3K/AKT/mTOR通路——一条调控生长、代谢与存活的著名内部控制系统。降低MT2A会抑制该通路的活性,而提升MT2A则激活它。当研究者使用药物阻断该通路的不同步骤时,MT2A过表达带来的益处消失:铁死亡标志再次上升,氧化损伤恢复,椎间盘细胞结构蛋白流失增多。这表明MT2A主要通过激活这条促存活的信号通路来保护椎间盘细胞,进而抑制铁死亡。
在动物中的概念验证
最后,团队评估在活体中提升MT2A是否能减缓椎间盘退变。在大鼠中,他们通过针刺造成椎间盘损伤,然后将一种旨在增加椎间盘内MT2A的病毒直接注入椎间盘。数周后,影像和组织分析显示,具有额外MT2A的椎间盘保留了更多高度,内部结构更清晰,关键基质蛋白流失更少,与未经处理的受伤椎间盘相比改善明显。铁死亡标志物也减少,支持了MT2A在抵抗氧化和铁应激导致的椎间盘塌陷方面具有保护作用的观点。
这对未来腰痛护理意味着什么
综上所述,这项工作表明MT2A并非旁观者,而是一种内建的安全因子:当椎间盘开始衰退时它会上调,试图保护细胞免受有害的铁驱动氧化。通过激活细胞内的生存通路,MT2A限制了一种特定形式的细胞死亡,维持椎间盘结构并减缓退变——至少在动物模型和细胞培养中如此。对患者而言,这提示MT2A及其信号伙伴可能是有前景的药物或基因治疗靶点,旨在保护或恢复脊柱椎间盘,长期来看可能提供超越止痛和手术的治疗选择。
引用: Cai, H., Zheng, Hl., Chen, Qz. et al. The protective up-regulation of metallothionein-2A in intervertebral disc degeneration inhibits nucleus pulposus cell ferroptosis through activation of the PI3K/AKT/mTOR pathway. Cell Death Discov. 12, 111 (2026). https://doi.org/10.1038/s41420-026-02972-9
关键词: 下腰痛, 椎间盘退变, 铁死亡, 金属硫蛋白‑2A, PI3K AKT mTOR 通路