Clear Sky Science · zh
多组学揭示由人类神经干细胞诱导的少突胶质细胞前体的异质性与功能亚群
为什么保护大脑绝缘层很重要
我们大脑的神经连接依赖于一种称为髓鞘的脂质包膜,它像电缆的绝缘层一样包裹在神经纤维周围。当髓鞘受损时(如多发性硬化和其他疾病中),信号传导会减慢或中断,导致运动、视力和认知方面的问题。本研究考察了一类能重建髓鞘的人类细胞,并提出了一个实用问题:哪些细胞最适合用于未来修复这一关键绝缘层的细胞疗法?
从起始的脑细胞到髓鞘制造者
研究人员以人类神经干细胞为起点——这些来自胎脑组织的多能起始细胞已注定向神经系统细胞分化。他们在体外诱导这些干细胞转分化为少突胶质细胞前体(hOPCs),即形成髓鞘细胞的直接前体。在显微镜下,细胞由简单的圆形转变为具多分支的复杂形态,并启动了标志成熟髓鞘产生过程的特征蛋白表达。这为深入分析提供了稳定且相对安全的人类髓鞘生成前体来源。
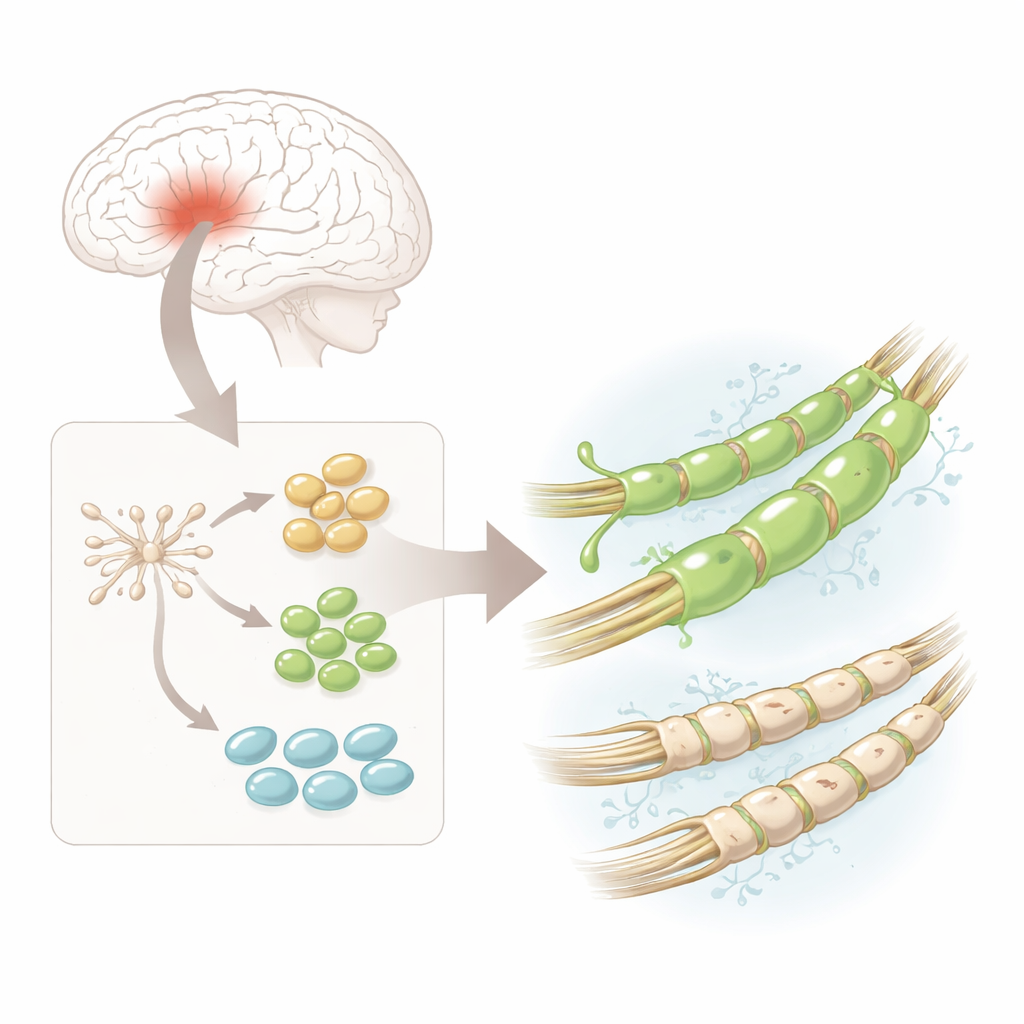
同一种细胞,许多隐蔽的变体
利用单细胞RNA测序——一种读取成千上万单个细胞中基因活动的方法,团队发现hOPC并非同质。相反,它们可分为三个主要阶段:早期的“前前体”、更为承诺的前体以及接近完整少突胶质细胞身份的细胞。在所有这些阶段中,有一个基因尤为突出:PDGFRA,它编码一个细胞表面受体。高灵敏度的成像方法RNA-Scope证实,PDGFRA的转录本和蛋白在各个阶段均比其他关键标志物更为丰富,提示该受体可能界定出特别有能力的髓鞘构建细胞。
筛选出最强的修复细胞
为验证这一观点,科学家将hOPC按其表面是否携带PDGFR-α受体分为两组。他们随后在一系列功能性测试中比较了PDGFR-α阳性细胞、PDGFR-α阴性细胞和未分选细胞。移植到无法形成正常髓鞘的“颤抖”小鼠体内时,PDGFR-α阳性细胞在神经纤维周围产生了更致密、更紧凑的髓鞘,优于其他组。这些细胞在体外实验中也迁移更远、增殖更快。换言之,PDGFR-α阳性群体在迁移到需要修复的部位、扩增数量并重建绝缘层方面最为有力。
驱动生长与修复的内部信号
进一步比较PDGFR-α阳性与阴性细胞的基因活动,研究发现阳性细胞激活了与胶质细胞生长与髓鞘形成相关的基因网络,以及若干关键的细胞内信号通路。其中两条通路尤为显著:长期与细胞生长及髓鞘生成相关的PI3K–AKT–mTOR通路,以及影响幼年脑细胞命运选择的TGF-β信号。数据表明,PDGFR-α的激活可上游作用于PI3K–AKT–mTOR,进而增强与TGF-β相关的信号,共同推动细胞朝有效的髓鞘制造者方向分化。
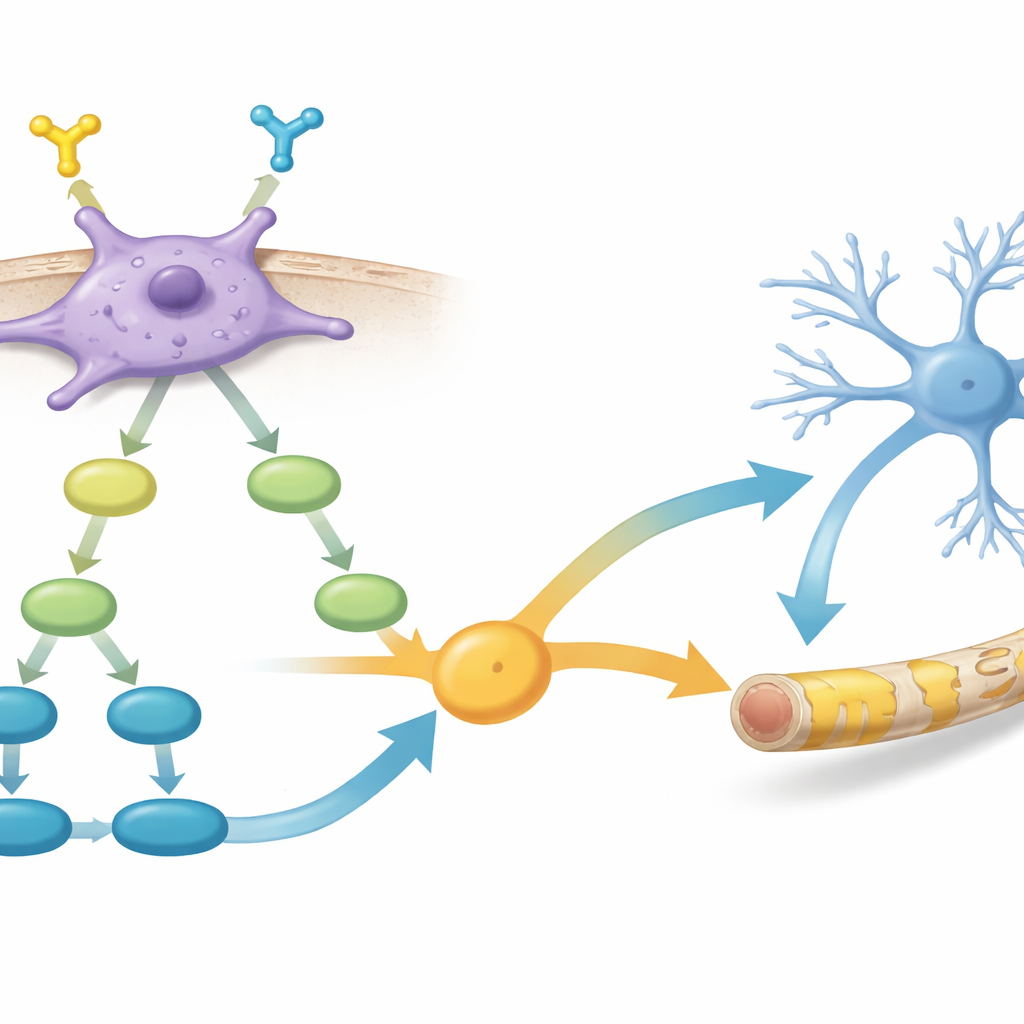
用化学助剂增强髓鞘修复
研究人员接着探问是否可以进一步强化这些有前途的细胞。他们用一种激活TGF-β通路的小分子处理PDGFR-α阳性hOPC,并检查了基因表达与行为学变化。处理后,这些细胞显示出更多髓鞘相关基因的上调,并在移植到颤抖小鼠时产生更厚、更完整的髓鞘包裹,与未处理的PDGFR-α阳性细胞相比效果更佳。这支持了这样一种观点:在已精挑细选的前体细胞中,精细调控内部信号可以进一步提升其作为活体髓鞘修复工具的功能。
这对未来治疗的意义
对非专业读者而言,核心信息是:并非所有髓鞘生成前体细胞都相同。通过结合强大的基因读取与成像工具,本研究识别出一个表现突出的亚群——PDGFR-α阳性hOPC——它们迁移更好、分裂更多,并比同类更有效地重建髓鞘。研究还指出了可通过化学手段调整、从而增强这些细胞效能的内部信号通路。总体而言,这些见解为设计更安全、更高效的细胞疗法铺就了路线,用以在髓鞘丧失的疾病中恢复大脑的绝缘层。
引用: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
关键词: 髓鞘修复, 少突胶质细胞前体, 神经干细胞, 细胞疗法, 单细胞RNA测序