Clear Sky Science · zh
敲低SREBP1通过抑制Nrf2‑XCT/GPX4轴在卵巢癌中诱导铁死亡
将癌细胞的“脂肪工厂”变为己用
卵巢癌常在晚期被发现且治疗困难。本研究探讨了这些肿瘤的一个出人意料的脆弱点:对脂肪合成的依赖。研究者表明,关闭癌细胞中一个关键的“脂肪工厂”开关,既能减缓其生长,又能触发一种特殊的细胞死亡形式,同时还使免疫系统更容易攻击肿瘤。
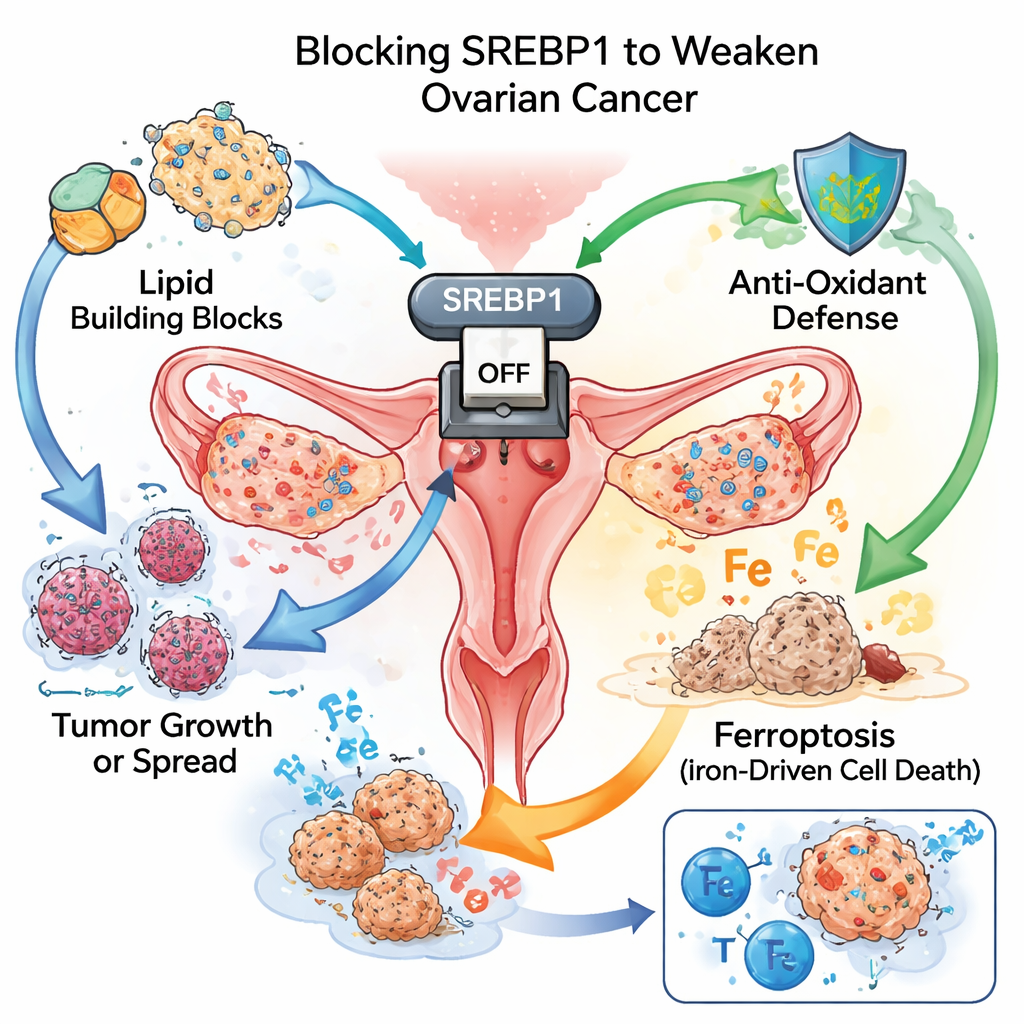
肿瘤燃料的主控开关
像生长迅速的杂草一样,癌细胞需要大量的构建材料和能量。它们满足这种需求的方式之一是改写脂质的合成与利用途径。团队关注的是SREBP1,这是一种作为脂质生成主控开关的蛋白。在来自一百多名患者的组织样本中,卵巢肿瘤的SREBP1水平明显高于邻近的正常组织。肿瘤中SREBP1染色更强的患者通常病情更具侵袭性,生存更短,这表明该蛋白既驱动肿瘤进展,又可作为不良预后的提示标志。
通过切断脂质供应减缓生长与转移
在体外培养的卵巢癌细胞系中,下调SREBP1显著降低了细胞增殖与克隆形成能力。细胞在细胞周期的特定阶段被阻滞,无法有效分裂。研究者还观察到运动与侵袭能力减弱:划痕实验和Transwell迁移实验显示SREBP1减少的细胞迁移能力下降,表型转变过程(即上皮–间质转化,EMT)的关键标志物也向更“正常”的状态回转。同时,甘油三酯和胆固醇含量下降,染色显示细胞内脂滴减少,证实其内部的脂质合成机器被关闭。
诱发一种以铁为燃料的细胞灭亡
抑制SREBP1最显著的效应是激活了铁死亡(ferroptosis),这是一种由铁以及细胞膜脂质过氧化驱动的、近年被识别的细胞死亡形式。只有铁死亡抑制剂能救回SREBP1沉默的细胞,而其他死亡途径的抑制剂无效,表明铁死亡是它们死亡的主要原因。化学检测显示氧化脂质的损伤产物增多,抗氧化分子谷胱甘肽减少,反应性脂质分子水平升高。两种通常保护细胞免受铁死亡的蛋白——xCT和GPX4,在SREBP1被敲低时显著下降,去除了对这种破坏性过程的关键保护缓冲。
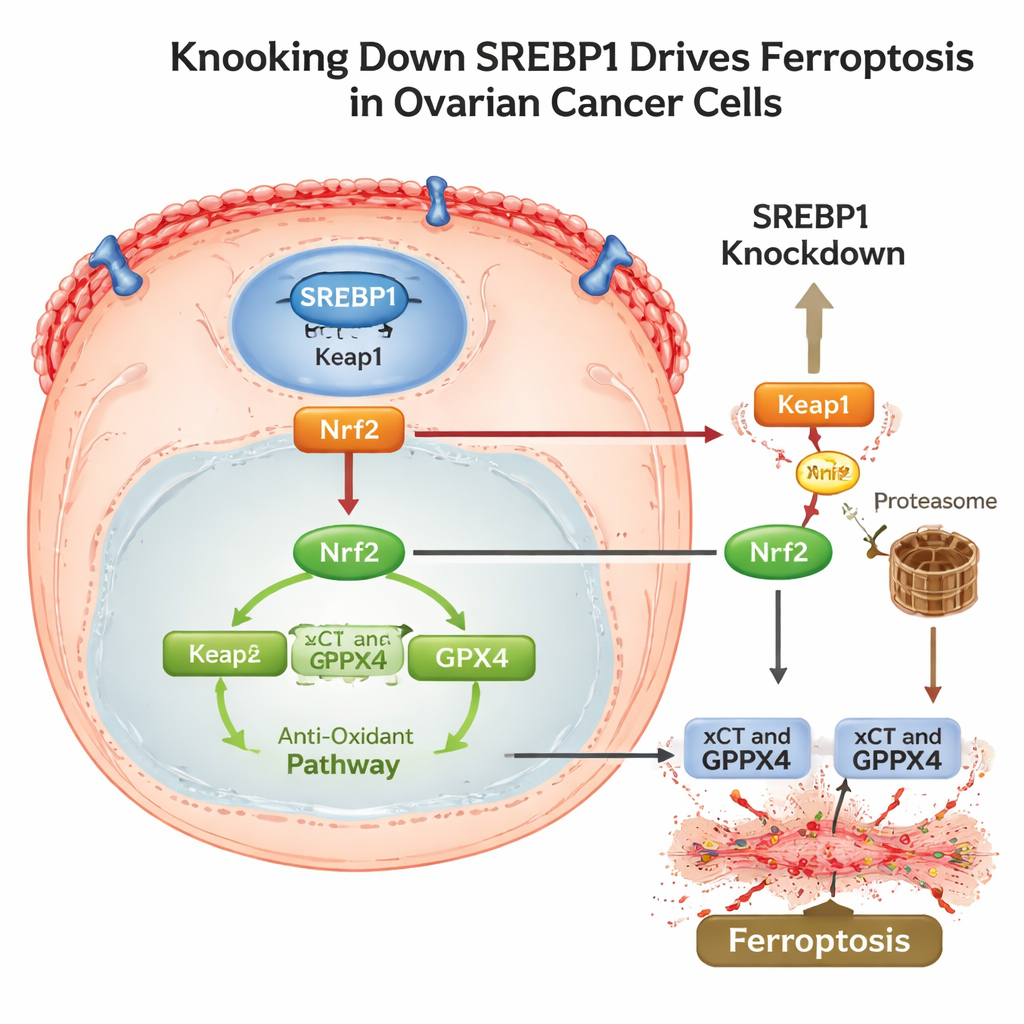
解除细胞的抗氧化盾与免疫逃避伎俩
为理解SREBP1如何关联到这一死亡程序,科学家追踪到另一个主要应激反应蛋白Nrf2介导的通路。在正常情况下,Nrf2通过启动抗氧化基因(包括xCT和GPX4)帮助细胞存活。研究发现,下调SREBP1会提高Keap1水平,Keap1会标记Nrf2以便降解,导致Nrf2被更多降解并减少进入细胞核。随着Nrf2下降,其下游防御减弱,铁死亡随之发生。重要的是,富含SREBP1的肿瘤还表现出更高的PD‑L1水平,这是一种帮助癌细胞躲避免疫T细胞攻击的表面蛋白。在小鼠肿瘤中沉默SREBP1后,癌症生长变慢,脂质损伤迹象增多,Nrf2和GPX4降低,PD‑L1减少,并伴有免疫活性增强。
这对未来治疗的意义
简而言之,卵巢肿瘤似乎把SREBP1作为一个双刃生存工具:它通过增强脂质生成来供养肿瘤生长,同时为肿瘤配备抗氧化盾和免疫伪装。这项工作表明,关闭SREBP1可以饿死肿瘤的脂质供应、剥夺其对铁驱动损伤的保护并降低其免疫躲避能力。因此SREBP1成为有吸引力的药物靶点,并提示将SREBP1抑制剂与能诱导铁死亡或激活免疫的治疗联合,可能为患者提供更有效且持久的病情控制。
引用: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
关键词: 卵巢癌, 脂质代谢, 铁死亡, SREBP1, 肿瘤免疫