Clear Sky Science · zh
半胱天冬酶活化驱动人表皮中抗脱钙粘蛋白3诱导的失粘作用
当身体转而攻击自身的“皮肤胶水”
寻常型天疱疮是一种罕见但危险的疾病,患者的免疫系统攻击将皮肤细胞粘在一起的“胶水”,导致疼痛性水疱和开放性溃疡。本研究在显微镜下探查一个关键问题:这些水疱仅仅是由于抗体阻断了这种“胶水”而形成,还是还有额外的细胞死亡信号帮助将皮肤细胞撕裂?弄清这一点可能有助于为患者开发更有针对性且副作用更小的治疗方法。
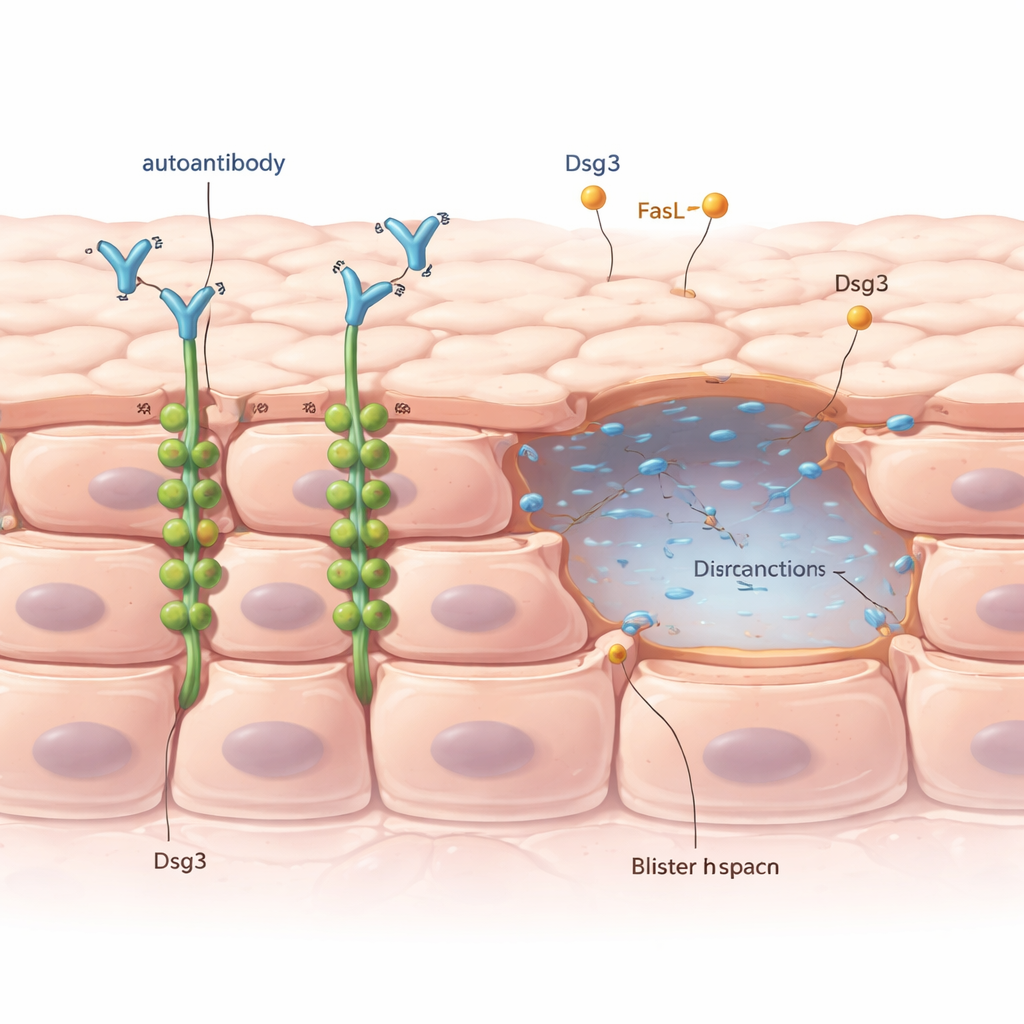
皮肤细胞通常如何保持粘连
我们皮肤的最外层由紧密排列的细胞组成,这些细胞通过称为桥粒的小结构相互连接,桥粒在邻近细胞间起到铆钉的作用。这些铆钉的一个关键成分是名为脱粘蛋白3(简称 Dsg3)的蛋白。在寻常型天疱疮中,患者产生的抗体错误地结合到 Dsg3 上。临床上早已知道,这种抗体攻击会引发称为失粘的过程,即细胞失去接触并出现水疱。但令人费解的是,尽管有害抗体分布于整个皮肤,水疱却只在特定部位和特定时间出现。
单靠抗体就能启动损伤
为了解抗体本身的作用,研究者使用了健康人皮肤片和一种实验室培养的皮肤细胞系,暴露于已被广泛研究的抗 Dsg3 抗体。他们发现,该抗体能削弱细胞间的黏附并触发失粘,即便未激活细胞内典型的细胞死亡程序。关键事件是 Dsg3 被从细胞表面牵拉进入细胞内部,常以小囊泡的形式被包裹。这种将 Dsg3 从细胞间“铆钉”中移除,使桥粒变短且效能降低,从而允许细胞开始分离。
当细胞死亡信号加入时,情况更糟
团队接着探讨一种在天疱疮中已知的细胞死亡信号——称为 Fas 配体(FasL)的分子,是否会改变这一局面。FasL 能激活称为半胱天冬酶的酶,尤其是半胱天冬酶-8,这些酶通常推动细胞进入程序性死亡。在患者皮肤样本和他们的皮肤模型中,研究者在受损区域观察到活化的半胱天冬酶-8,但这些区域并无典型的细胞死亡迹象。当他们将少量不致死的 FasL 与抗 Dsg3 抗体联合使用时,水疱形成更快且更严重,尤其发生在表皮较深的层次。在细胞培养中,单独的 FasL 并不会削弱黏附,但与抗体联合时却大大增加了细胞的破裂——而当半胱天冬酶-8 被阻断时,这种增强效应消失了。
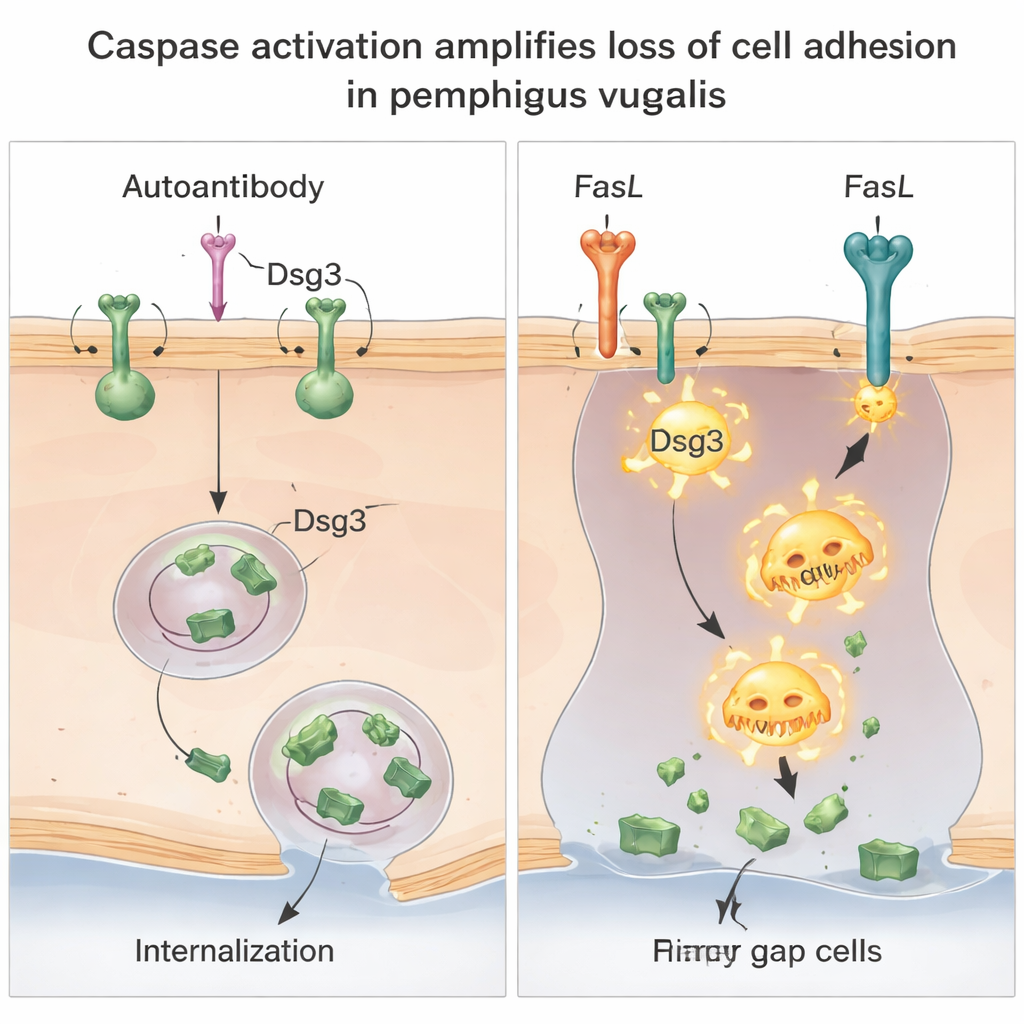
破坏同一连接的两种路径
深入研究显示,Dsg3 的丢失实际上有两条不同但相互协作的途径。其一,抗体促进完整的 Dsg3–抗体复合物从细胞表面被内吞到特化的膜隔室中,减少了细胞连接处可用的 Dsg3。这一步不依赖半胱天冬酶,且通过阻断常见的蛋白降解途径也无法阻止,表明这是 Dsg3 在细胞内的一种特定重排。其二,当存在 FasL 时,半胱天冬酶-8 被激活并切割 Dsg3 为更小的片段,尤其在膜上附着较松弛的部分。这种由半胱天冬酶驱动的切割进一步降低了完整功能性 Dsg3 的含量,并放大了抗体触发的黏附丧失。
对患者和未来治疗的意义
综合来看,结果表明在寻常型天疱疮中,针对 Dsg3 的抗体通过从细胞表面剥离 Dsg3 启动起泡过程,而 FasL 驱动的半胱天冬酶活化则像放大器一样,通过切割残余的 Dsg3 使损伤更为严重。重要的是,其中大部分过程发生在皮肤细胞真正死亡之前。对患者而言,这意味着有效的治疗可能不仅需要降低有害抗体,还需阻断 FasL 或半胱天冬酶以防止水疱形成或扩散。这一双重机制也可能解释了为何该病在不同个体或不同部位的表现差异很大,并指向保持皮肤“天然胶水”完整性的更精确的新方法。
引用: Schmidt, M.F., Feoktistova, M.A., Panayotova-Dimitrova, D. et al. Caspase-activation powers anti-Desmoglein 3-induced acantholysis in human epidermis. Cell Death Discov. 12, 102 (2026). https://doi.org/10.1038/s41420-026-02963-w
关键词: 寻常型天疱疮, 自身免疫性起泡病, 脱粘蛋白3, 半胱天冬酶-8, Fas 配体