Clear Sky Science · zh
关节软骨细胞增殖性衰老与化学诱导衰老的表型和分子比较分析
为什么“疲惫”的关节细胞很重要
关节酸痛、僵硬是常见的衰老伴随现象,但研究者发现,一类特殊的“疲惫”细胞可能是全球最常见关节疾病——骨关节炎的关键推动者。这类称为衰老细胞的细胞停止分裂,并开始释放一系列刺激性分子,对周围组织造成损伤。本研究提出了一个看似简单却至关重要的问题:当研究人员在实验室培养软骨细胞以研究骨关节炎时,用哪些方法使这些细胞“变老”最能模拟真实关节中发生的情况?
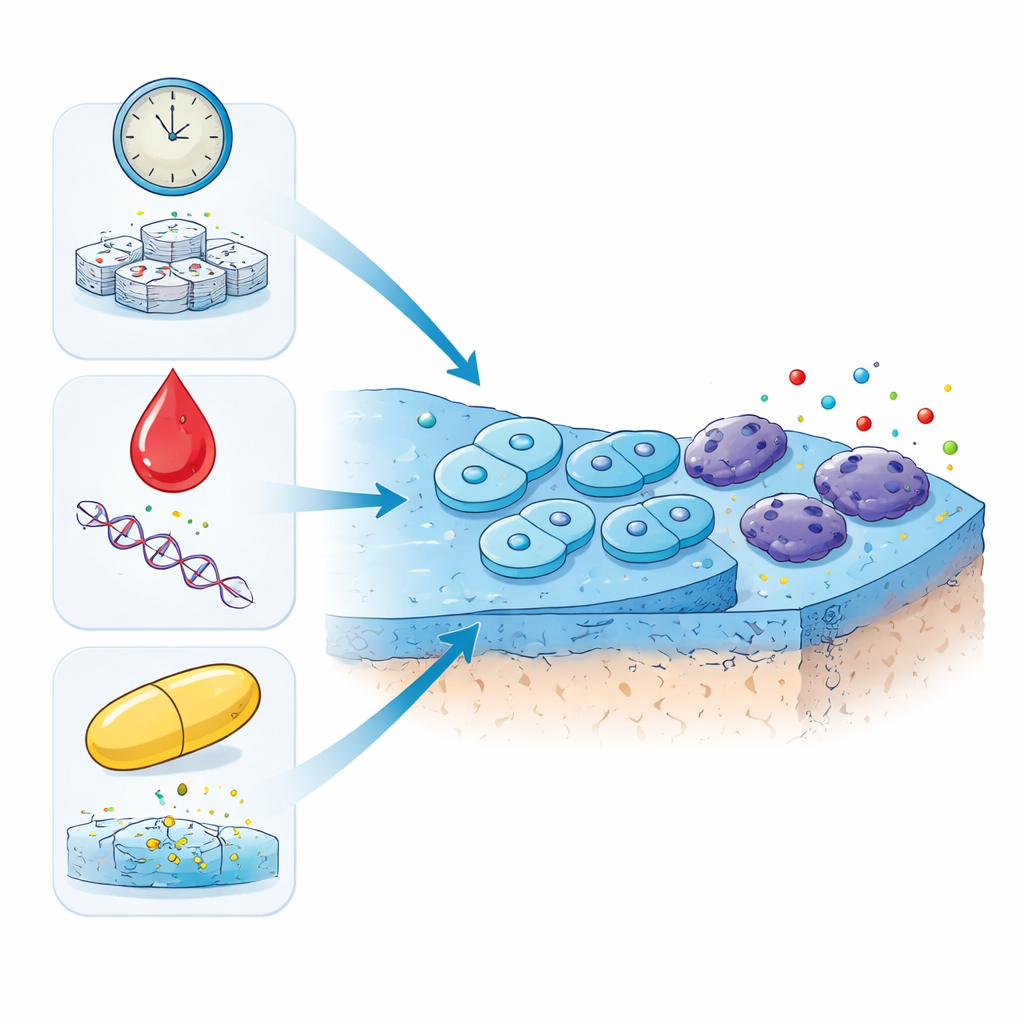
三条通向“疲惫”细胞的不同路径
研究者把注意力放在维持骨端光滑软骨的软骨细胞上。他们使用来自绵羊关节的细胞,通过三种不同方式诱导细胞进入衰老状态。一种方法是让细胞持续分裂多代,直到达到一种老化、疲惫的状态,模拟随时间推移的自然衰老。另两种方法则将年轻细胞暴露于两种在临床上使用的低剂量药物:多柔比星(一种会损伤DNA的化疗药)和地塞米松(一种注射到疼痛关节中的强效抗炎类固醇)。所有三种处理都经过调控,使细胞能存活足够长时间以形成稳定的类老化状态。
细胞衰老的共同特征
在三种方法中,软骨细胞都表现出衰老的典型标志。它们停止增殖、细胞周期发生变化,并表现出一种常用来识别衰老细胞的酶活性升高。细胞的内部结构也发生改变,呈现出更大、更扁平的形态以及DNA包装方式的变化。在更深层次上,细胞的线粒体——产生细胞能量的小“发电站”——不再高效工作。通过强大的基因和蛋白质分析,研究团队发现关键的能量产生通路和新蛋白合成系统在所有模型中都被下调。综合来看,这些变化描绘出这样一幅图景:软骨细胞退出了“工作岗位”,处于一种代谢迟缓但持续存在的状态。
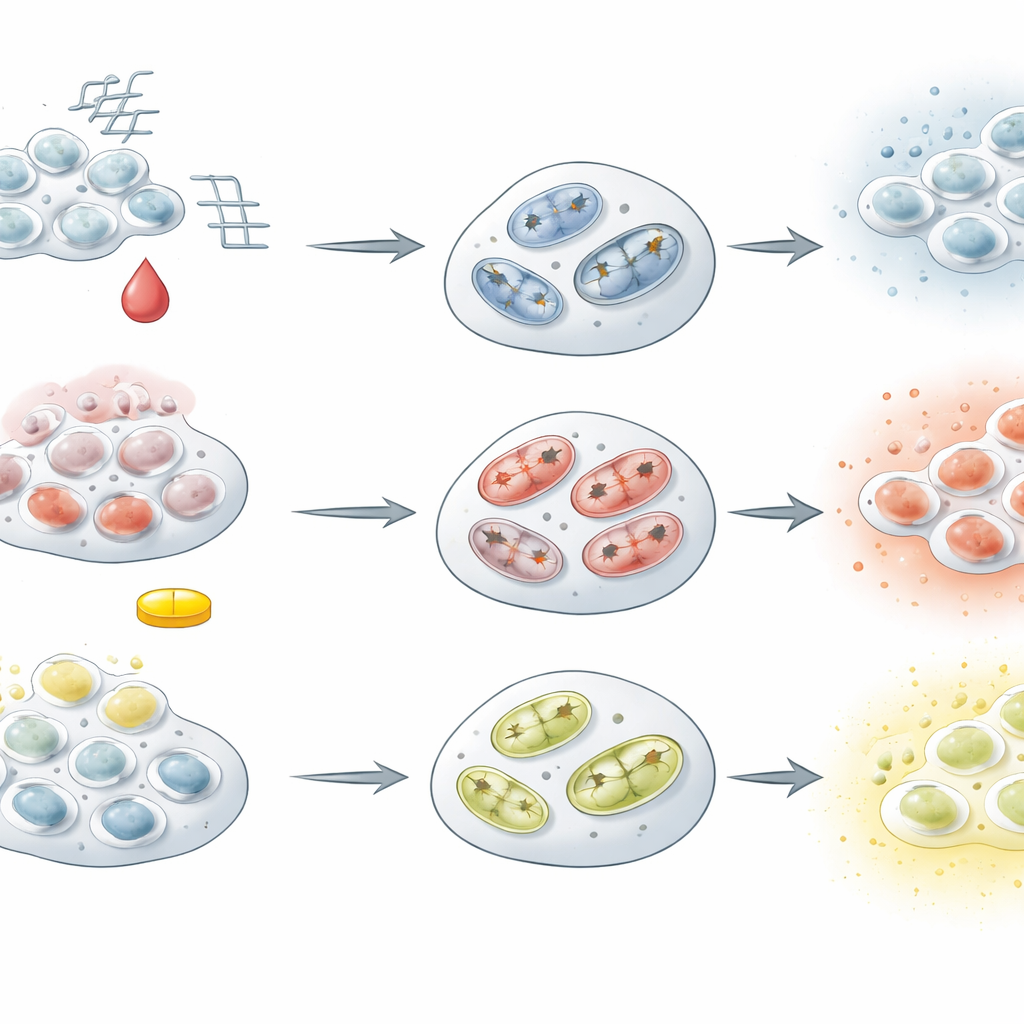
相同的终点,不同的路径
尽管存在这些共同特征,三种模型并非完全相同。通过多轮分裂而衰老的细胞表现出端粒缩短、氧化代谢副产物积累、能量丧失,并向外释放更多结构性软骨蛋白——这些特征类似于缓慢、与年龄相关的软骨磨损。相比之下,多柔比星处理的细胞激发了强烈的DNA损伤反应,启动了细胞死亡程序,并产生高水平的炎性信号,表明更剧烈、更像损伤的情形。地塞米松处理的细胞也进入了衰老状态,但没有出现同样剧烈的氧化损伤或凋亡反应。相反,它们维持甚至提高了能量输出,并产生大量与炎症和组织重塑相关的分泌因子,反映了类固醇药物对本来健康软骨的复杂、双重影响。
向关节发出的信号
这些衰老细胞释放的物质——统称为衰老相关分泌表型(SASP)——在不同模型间差异显著。长期分裂的细胞分泌较少典型的炎症和应激相关蛋白,但在软骨基质成分方面更为富集。相比之下,两组药物处理的细胞,尤其是类固醇暴露的细胞,释放出大量能够吸引免疫细胞、促进炎症并重塑周围组织的分子。这些不同的“分泌指纹”很重要,因为在活体关节中,它们要么在数十年中悄然削弱软骨,要么在损伤、化疗或反复类固醇注射后推动更剧烈、发作性的损害。
这对理解和治疗关节疾病意味着什么
对非专业读者而言,核心信息是并非所有“老化”的软骨细胞都相同。研究表明,不同的实验室方法虽然都能将软骨细胞推入一种衰老状态,但它们通过不同类型的应激产生不同后果。通过时间和反复分裂而衰老的细胞与自然衰老和长期骨关节炎中观察到的细胞最为相似;而受化疗或类固醇压力的细胞更能模拟药物或急性损伤加速关节退化的情形。通过谨慎地将实验模型与现实情景匹配,研究者可以更有效地测试清除衰老细胞或抑制其有害分泌的药物。该研究还强调了线粒体功能衰退和能量平衡紊乱是所有衰老软骨细胞共同的薄弱环节——这为未来旨在保持关节更长久健康的治疗策略提供了有吸引力的靶点。
引用: Arteaga, M.B., Tarasova, K., Kidtiwong, A. et al. Comparative phenotypic and molecular profiling of replicative and chemically-induced senescence in articular chondrocytes. Cell Death Discov. 12, 106 (2026). https://doi.org/10.1038/s41420-026-02961-y
关键词: 骨关节炎, 细胞衰老, 软骨细胞, 线粒体功能障碍, 软骨退变