Clear Sky Science · zh
神经元缺氧应答的新机制:HIF-1α/STOML2 介导的 PINK1 依赖性线粒体自噬激活以抵御神经元损伤
为何大脑对低氧的反应至关重要
许多常见疾病——包括中风、睡眠呼吸暂停、心力衰竭,甚至高原暴露——都会使大脑缺氧。当氧气下降时,脑细胞面临永久性损伤的风险,可能导致记忆问题和其他神经系统障碍。本研究揭示了神经元在缺氧早期所启用的一种内在“自我保护”机制,帮助细胞在低氧环境中维持存活和功能。了解这一机制可能为在严重伤害发生前保护大脑开辟新的治疗途径。
早期受困,但尚未崩溃
为探究大脑如何应对低氧,研究者将小鼠置于约13%氧气的环境中——相当于生活在高原——不同时间长度。前几天里,动物在记忆和迷宫测试中表现正常,显微镜下脑细胞外观亦健康。只有在连续一周的低氧后,鼠类才开始出现明显的记忆丧失和脑细胞结构紊乱。该模式表明,至少在早期,神经元并非氧气损失的被动受害者;相反,它们会启动保护性反应,以延缓或防止损伤。
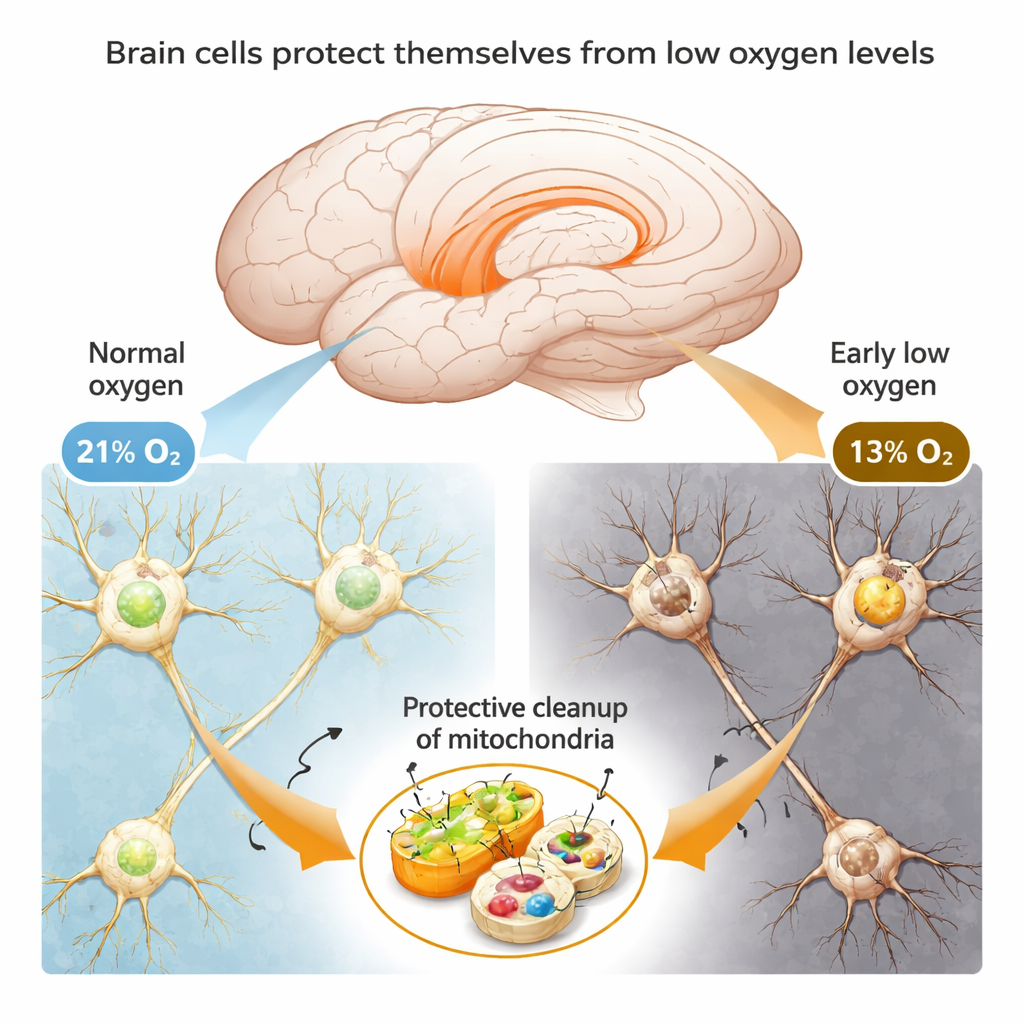
细胞清理工作:清除损坏的“发电厂”
研究的一个重点是细胞的能量工厂——线粒体。线粒体对神经元尤为重要,因为思考和记忆消耗大量能量。在低氧下,线粒体可能功能失常并泄漏有害副产物,损伤细胞。研究团队发现,在缺氧的早期阶段,神经元暂时增强了一种特殊的清理过程——线粒体自噬(mitophagy),该过程选择性地去除受损的线粒体而保留健康的。在小鼠大脑和人源神经细胞的培养中,这种清理过程的标志物在氧气下降后很快上升,恰在细胞仍能正常工作的时期。当科学家用化学方法阻断线粒体自噬时,细胞存活率下降且损伤迹象增加,表明这一清理步骤对保护至关重要。
神经元内的保护性连锁反应
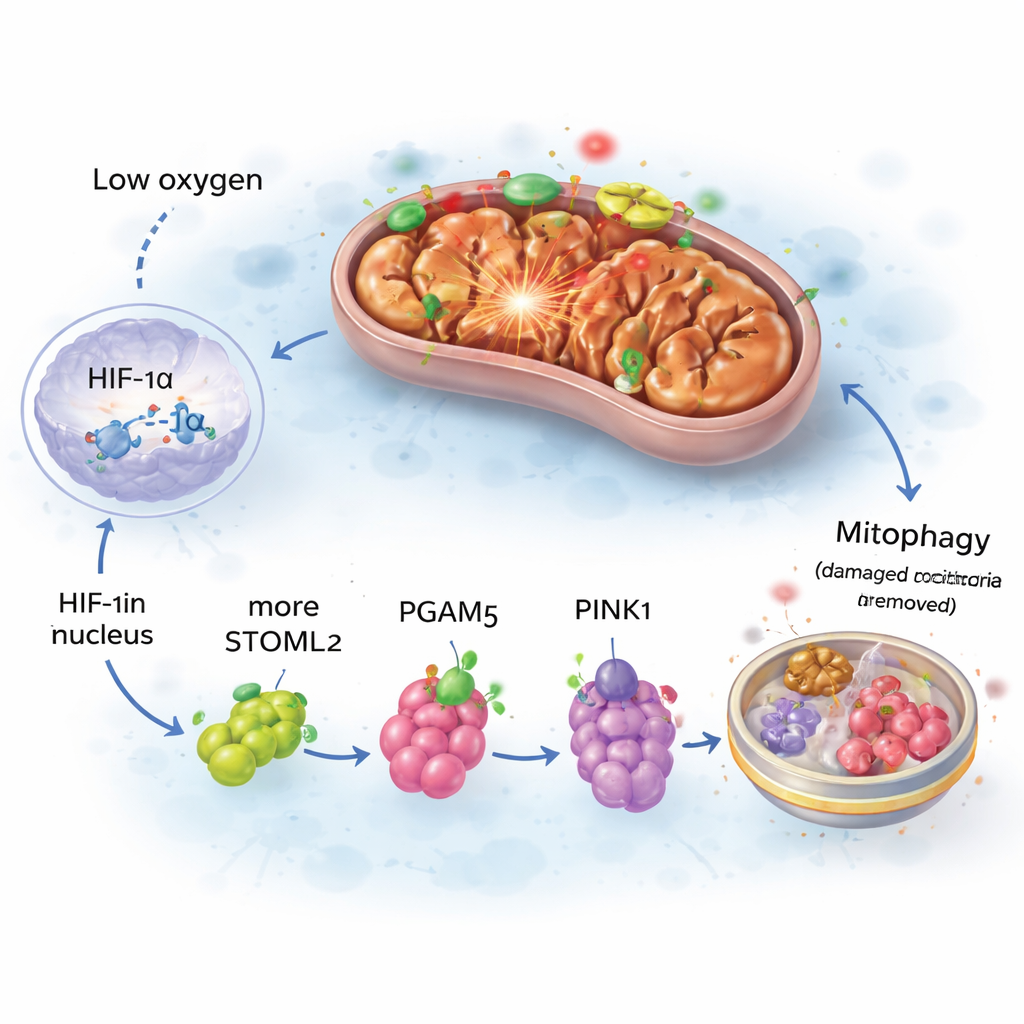
进一步研究中,研究者追踪了这一线粒体清理如何被激活。低氧使感应蛋白 HIF‑1α 稳定并进入细胞核,改变基因表达。其中一个靶基因是 STOML2,该蛋白会重新定位到线粒体表面。在那里,STOML2 有助于维持另一蛋白 PGAM5 的全长形式。PGAM5 反过来允许 PINK1 在受损线粒体外膜上积累。随后 PINK1 将这些故障的“发电厂”标记给细胞的回收体系。当研究团队在小鼠大脑中选择性下调 HIF‑1α、STOML2、PGAM5 或 PINK1 时,早期的线粒体自噬波消失,神经元在低氧暴露中遭受更多损伤。由 HIF‑1α→STOML2→PGAM5→PINK1 组成的逐步链条浮现为一条核心保护通路。
用间歇性低氧“训练”大脑
该研究还测试了一种称为间歇性缺氧的“调理”策略:在面临长期低氧之前,让小鼠经历短暂、反复的低氧与正常氧交替循环。这种预处理开启了相同的 HIF‑1α/STOML2/PGAM5/PINK1 通路并增强了大脑中的线粒体自噬。值得注意的是,接受间歇性缺氧的小鼠在连续一周低氧后仍保持记忆表现,而未经处理的动物则表现下降。这些发现表明,精心控制的短暂低氧能够训练神经元更有效地激活自身清理系统,类似于运动使肌肉更能应对压力。
这对保护大脑意味着什么
通俗地说,研究表明神经元具有一套针对低氧情形的内在应急方案:它们能迅速感知氧气变化,提升一串保护性蛋白的活性,并在故障扩散之前清除失常的能量工厂。当这套方案被中断时,脑细胞更易受损。通过详尽绘制该通路并证明间歇性缺氧能安全触发它,研究指向了未来可能模拟或增强这种天然防御的治疗方法。这类方法或能在中风、睡眠相关呼吸障碍以及其他氧供受威胁的疾病中,为大脑提供保护。
引用: Li, Y., Xu, Z., Tian, Z. et al. Novel mechanism of neuronal hypoxia response: HIF-1α/STOML2 mediated PINK1-dependent mitophagy activation against neuronal injury. Cell Death Discov. 12, 104 (2026). https://doi.org/10.1038/s41420-026-02960-z
关键词: 大脑缺氧, 线粒体自噬, 神经元保护, 间歇性缺氧, 线粒体