Clear Sky Science · zh
PDHA1通过上调AIFM2增强抗缨脱性凋亡的前列腺癌对铁死亡的抵抗
为什么有些前列腺癌细胞拒绝死亡
当癌细胞从肿瘤脱落并进入血流时,大多数在到达新器官前就会死亡。然而,有一小部分危险的细胞能够存活、迁移并播下常致命的转移灶。本研究提出了一个关键问题:是什么让某些前列腺癌细胞能抵抗在失去与原位组织接触后通常会发生的一种细胞死亡形式?通过揭示这些细胞内的一个隐蔽生存回路,研究为从源头阻断转移指明了新的途径。
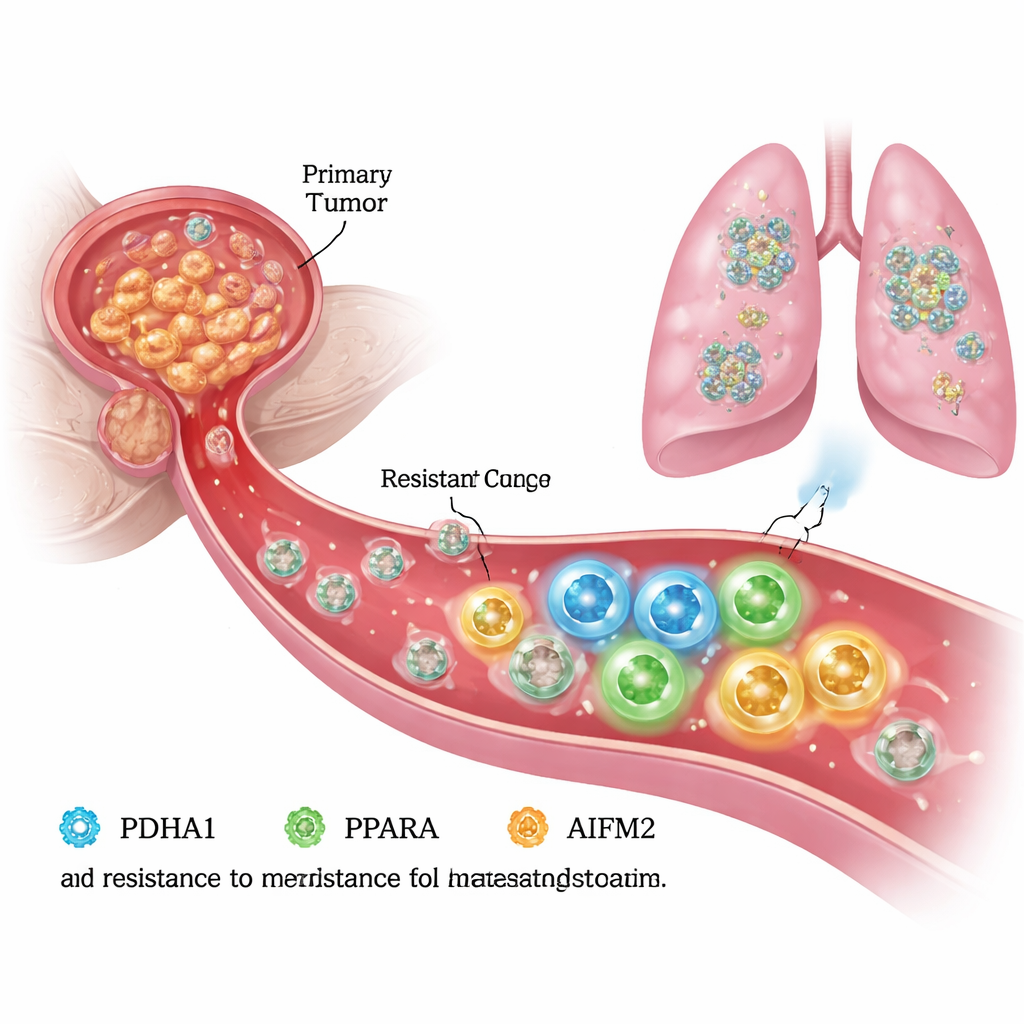
在血流中逃避死亡
为了扩散,前列腺癌细胞必须在没有周围组织支持(即细胞外基质)的情况下生存。在这种“脱离”条件下,健康细胞会经历一种称为缨脱(anoikis)的程序性死亡,许多癌细胞同样易感于一种相关的、由铁驱动的死亡过程——铁死亡。作者在实验室中构建了缨脱抵抗的前列腺癌细胞,并将其与原始“亲代”细胞进行了比较。他们发现,抵抗性细胞不仅迁移和侵袭更强,而且在脱离条件下存活能力更高,提示这些细胞已重塑内部机制以避免铁死亡并持续生长。
具有第二功能的代谢开关
深入研究时,团队将注意力集中在一种代谢酶PDHA1上,该酶以帮助细胞在线粒体中将源自糖的丙酮酸转化为乙酰辅酶A以推动能量产生而著称。在缨脱抵抗细胞中,PDHA1的水平和活性明显升高,且临床样本显示来自发生淋巴结或远处转移患者的原发肿瘤中PDHA1含量更高。当研究者降低PDHA1时,抵抗性细胞的迁移、侵袭和存活能力大幅下降。令人意外的是,这些细胞中相当一部分PDHA1不再局限于线粒体;它已转位到细胞核内,而细胞核中DNA与组蛋白结合,组蛋白可被化学修饰以开启或关闭基因表达。
改写基因活性以阻断铁死亡
在细胞核内,PDHA1似乎促进了局部乙酰辅酶A的生成,乙酰辅酶A是组蛋白乙酰化的关键底物。作者证明,核内PDHA1在名为PPARA的基因调控区增加了特定的标记——H3K9乙酰化。该变化有如放松染色质“线轴”,使PPARA更容易被激活。PPARA进一步作为主开关,通过结合AIFM2的启动子并提高其转录来增加AIFM2的产生。因此,PDHA1并非直接调整AIFM2基因,而是通过PPARA发挥作用,建立了从代谢改变到基因调控改变的多步骤通路。
构建针对铁介导损伤的防护盾
AIFM2被认为是铁死亡的内部刹车:它有助于保护细胞膜中的脂质免受破坏性氧化。在抵抗性前列腺癌细胞中,PDHA1上调导致AIFM2水平升高,而敲低PDHA1则使其下降。功能性检测显示,降低PDHA1会加剧铁死亡的特征——更多活性氧、更多脂质损伤、线粒体膜电位降低以及典型的线粒体收缩——尤其是在细胞暴露于诱导铁死亡的药物erastin时。过表达AIFM2能逆转这些效应,在细胞培养中挽救细胞存活,并在小鼠中恢复肺转移,即使在PDHA1被抑制的情况下也能如此。这证实AIFM2是PDHA1驱动的铁死亡抗性中的关键下游效应子。
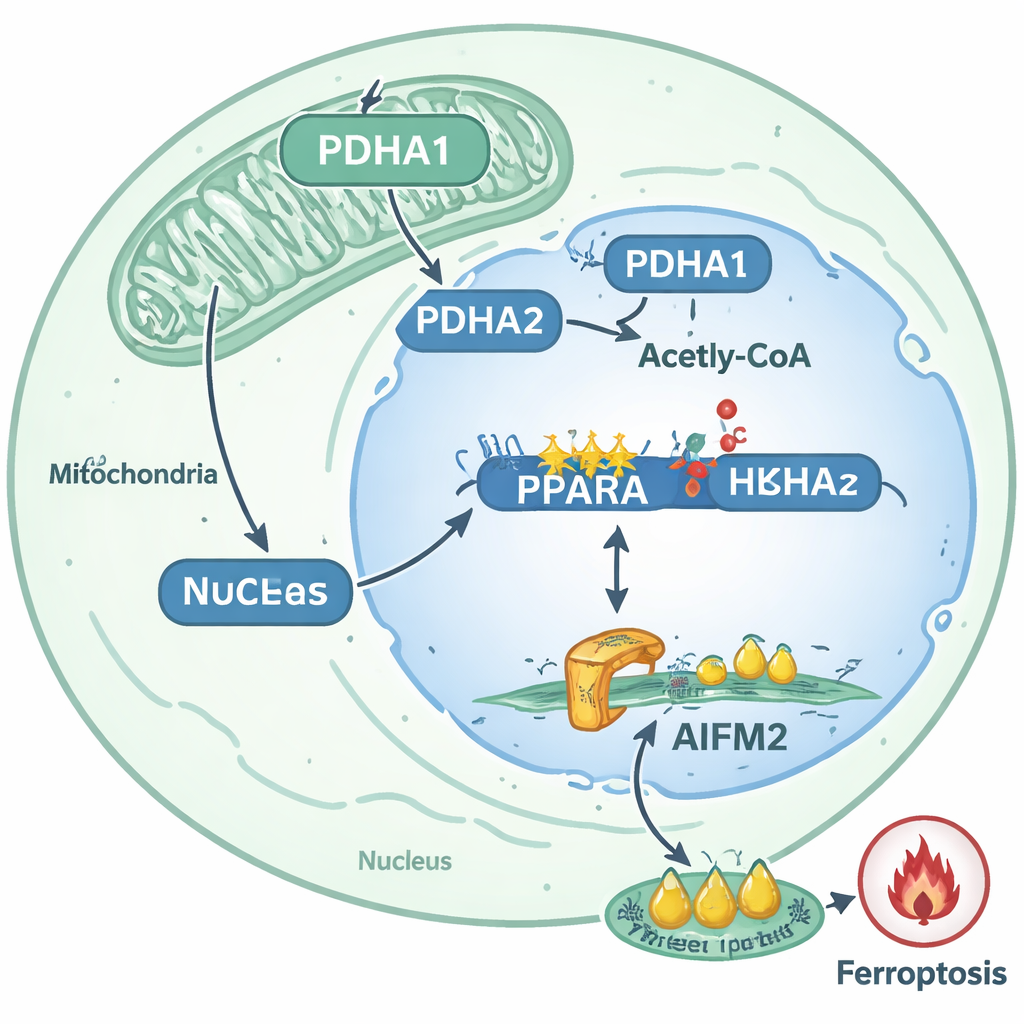
从分子回路到治疗思路
通过描绘这些事件,研究勾勒出一条清晰路径,说明脱离的前列腺癌细胞如何变得更难被杀死:PDHA1进入细胞核,在PPARA基因处增加组蛋白乙酰化,提升PPARA活性,从而提高AIFM2水平以阻断铁死亡。该通路与患者肿瘤和动物模型中的转移行为密切相关。对非专业读者来说,结论是某些癌细胞将一种常见代谢酶重新利用为一种表观遗传工具,改写基因活性并构筑一层生化屏障以抵御一种强大的细胞死亡形式。作者提出,未来或可将针对PDHA1、PPARA或AIFM2的药物——或有意触发铁死亡的疗法——联合使用,以剥夺转移性前列腺癌细胞的这一生存优势,使它们在最脆弱的旅程中——从一个器官跳跃到另一个器官时——变得更为脆弱。
引用: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
关键词: 前列腺癌转移, 铁死亡, 缨脱抗性, PDHA1, AIFM2