Clear Sky Science · zh
调节代谢特征以缓解FLT3-ITD急性髓性白血病细胞模型中对卡博替尼抗药性的研究
这对癌症治疗为何重要
许多现代癌症药物旨在针对肿瘤细胞中的单一异常蛋白。这类靶向药能诱导显著缓解,但癌症常常通过适应机制重新生长。本文探讨了一种血液癌——急性髓性白血病(AML)如何对一种靶向药物卡博替尼产生抗性,以及重塑癌细胞能量利用方式是否能帮助临床应对这种抗性。
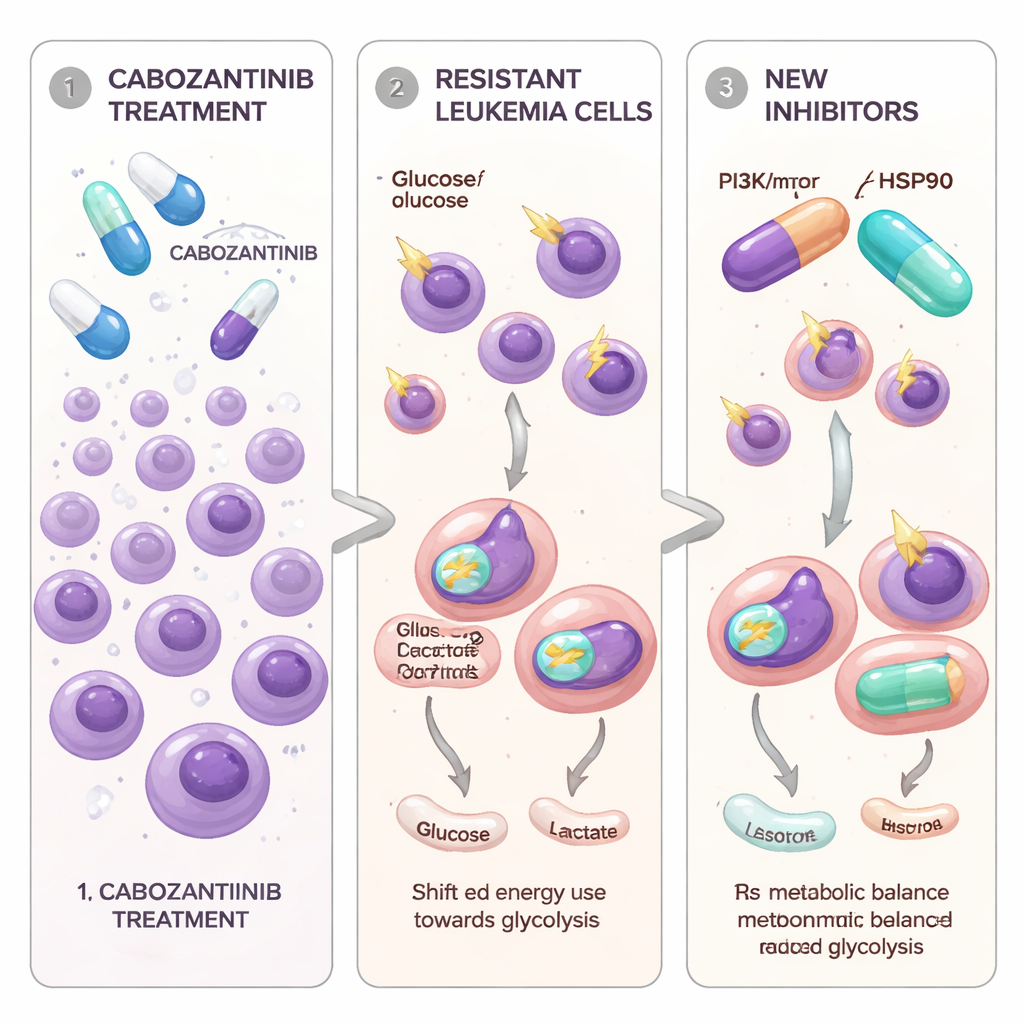
学会躲避靶向药的白血病细胞
研究者聚焦于携带FLT3-ITD这一生长信号开关突变的AML细胞,该突变已知会驱动更具侵袭性的疾病。卡博替尼是一种已用于多种实体瘤的口服药物,在体外可强烈抑制FLT3驱动的白血病细胞。为模拟患者随时间出现的情况,研究团队逐步用递增剂量的卡博替尼处理两种FLT3突变的AML细胞系,直到部分细胞存活并重新开始增殖。新形成的细胞群体被命名为Molm13‑XR和MV4‑11‑XR,它们可耐受远高于原始“亲代”细胞的卡博替尼浓度。这些耐药细胞对另外两种已获批的FLT3靶向药物索拉非尼和奎扎替尼的敏感性也下降,但仍对另一种抑制剂gilteritinib保持敏感。
帮助癌细胞生存的基因改变
深入分析显示,这些耐药白血病细胞在FLT3基因中出现了新的改变。两个耐药细胞系都获得了位于FLT3激酶结构域关键区域的相同点突变D835Y,该位点是多种药物耐药性的已知热点。MV4‑11‑XR这一系还出现了一个异常的1.3千碱基缺失,删除了FLT3的整个外显子,抹去了对药物结合重要的结构域部分。这些改变似乎是在长期暴露于卡博替尼过程中被选择出来的:耐药细胞中FLT3的突变版本比起始群体更为常见。与此同时,FLT3下游的关键信号通路——例如ERK、STAT5和AKT——被更强烈地激活,支持了耐药细胞更快的生长和更强的克隆形成能力。
癌细胞切换能量供给系统
研究组接着探讨抗性是否不仅与遗传有关,还与细胞的能量代谢方式相关。借助RNA测序和专门的代谢检测,他们发现了一个一致模式:对卡博替尼耐药的细胞在有氧条件下也更强烈依赖糖酵解——即细胞质中对葡萄糖的快速分解。这些细胞摄取更多葡萄糖、产生更多乳酸、关键酶GAPDH活性更高,并且多种与糖酵解相关基因的表达上调。相比之下,支持更高效能量生成的线粒体活性和数量都下降。氧耗测量显示基础和最大线粒体呼吸均降低,细胞内活性氧升高,指向线粒体处于应激和功能受损状态。
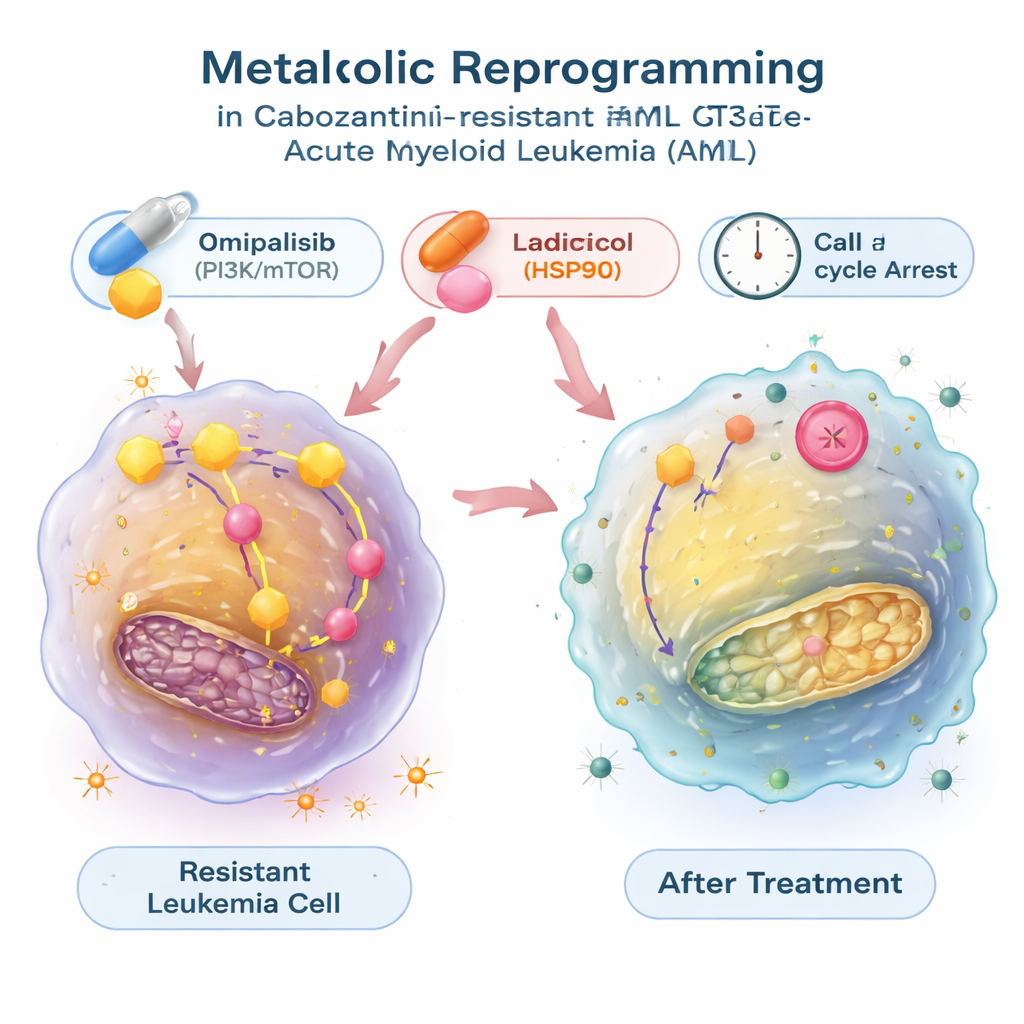
寻找能将代谢开关翻回来的药物
为验证这种能量代谢的转变是否可逆,研究者利用一个大型公共数据库,该数据库将基因表达模式与数千种化合物的效应关联起来。他们检索预测可逆转耐药白血病代谢特征的药物,集中发现两种候选物:radicicol,它抑制一种名为HSP90的蛋白伴侣;以及omipalisib,它抑制控制生长与代谢的PI3K/mTOR信号通路。在体外测试中,这两种分子不仅减缓了耐药细胞的生长,还降低了其过度活跃的糖酵解,恢复了葡萄糖摄取和乳酸释放至更正常水平并下调了糖酵解相关基因表达。这些化合物使白血病细胞进入细胞周期的静止期,且radicicol还在一定程度上诱导了细胞程序性死亡。与卡博替尼联合使用时,omipalisib——以及在一种模型中radicicol——表现出协同作用,使这些耐药细胞更易被消灭。
对未来白血病治疗的意义
对非专业读者来说,结论是白血病细胞不仅通过突变其直接靶点来逃避靶向药物,还可以通过改变能量的产生和使用方式来适应治疗。本研究显示,卡博替尼耐药的AML细胞采用了“以糖为主”的代谢策略,同时放任线粒体功能衰退。通过瞄准支持这种重塑代谢的通路——例如使用omipalisib或HSP90抑制剂——可能有望恢复对卡博替尼及类似药物的敏感性。尽管这些发现来自细胞模型而非患者,但它们提示,将靶向药物与调节代谢的药物联合使用,可能是延缓或克服FLT3突变AML抗性的有前景策略。
引用: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
关键词: 急性髓性白血病, 药物抗性, FLT3 突变, 癌症代谢, 卡博替尼