Clear Sky Science · zh
骨细胞脂质运载蛋白‑2 通过依赖铁的铁死亡和 Wnt 抑制在局部调节骨形成
当骨细胞悄然影响全身健康时
大多数人把骨骼视为刚性支架,但骨内有活跃的细胞持续重建和修复骨骼。本研究揭示了一种由骨细胞产生的小蛋白——脂质运载蛋白‑2(lipocalin‑2)如何通过扰乱细胞对铁和能量的处理,悄然削弱骨质。理解这一隐匿过程可能为治疗骨质疏松和年龄相关的骨量流失指明新途径。
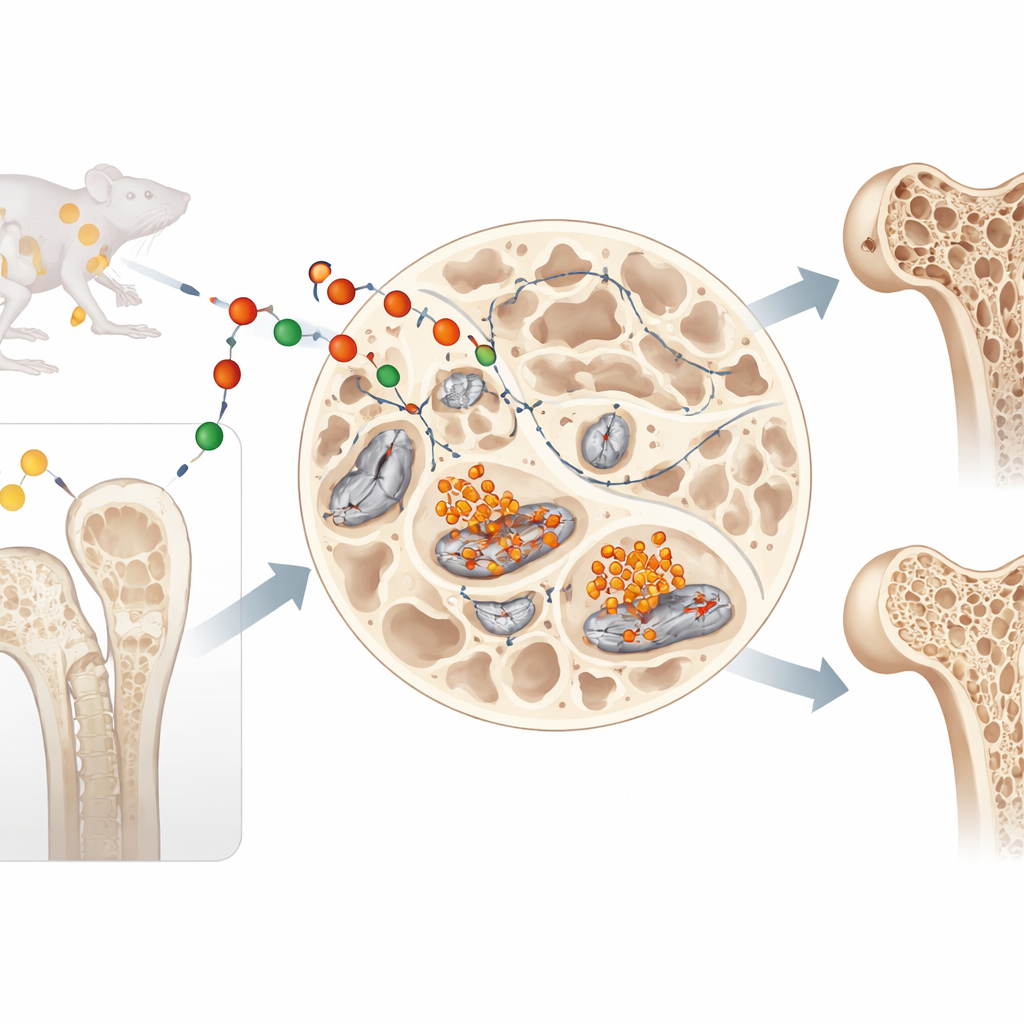
兼具两面角色的信使蛋白
脂质运载蛋白‑2 被认为是一种循环激素,通过血液行走,参与食欲和体重调节,并通过结合铁来抵御感染。但本文作者提出了另一个问题:脂质运载蛋白‑2 在其生成地点——骨内,到底做什么?他们聚焦于骨细胞(osteocytes),这些长期存活、深埋于骨内的细胞感知机械力并指挥骨重塑。研究团队发现,骨细胞在成熟过程中不仅持续产生脂质运载蛋白‑2,而且其产量实际上增加,表明该蛋白在骨骼内具有重要的局部作用。
铁超载与类似“生锈”的细胞死亡
鉴于脂质运载蛋白‑2 能运载铁,研究者检测它是否会促进骨细胞内铁的积累。在培养的骨细胞中,加入脂质运载蛋白‑2 导致细胞内铁积聚、促生有害的活性氧分子,并触发对富含脂质的细胞膜的严重损伤。这些都是一种新近识别的细胞死亡形式——铁死亡(ferroptosis)的特征,在此过程中铁类似“生锈”,触发破坏性化学反应。用螯合剂封锁铁完全阻止了损伤和细胞死亡,证实该过程依赖铁。
门控受体与线粒体后果
为弄清脂质运载蛋白‑2 如何将铁货送入骨细胞,研究团队把目光投向一种细胞表面受体 SLC22A17。当他们在类骨细胞中降低该受体表达时,脂质运载蛋白‑2 不再促进铁进入、氧化应激或铁死亡,即便在铁超载条件下亦如此。研究还显示,脂质运载蛋白‑2 损害细胞的能量工厂:线粒体。额外的脂质运载蛋白‑2 导致线粒体膜电位丧失和能量生成下降,而去除脂质运载蛋白‑2 则恢复了线粒体功能。在小鼠模型中,缺乏骨细胞来源脂质运载蛋白‑2 的骨组织中,支持线粒体呼吸和质量控制的基因被上调,暗示这些细胞在能量上更为稳健。
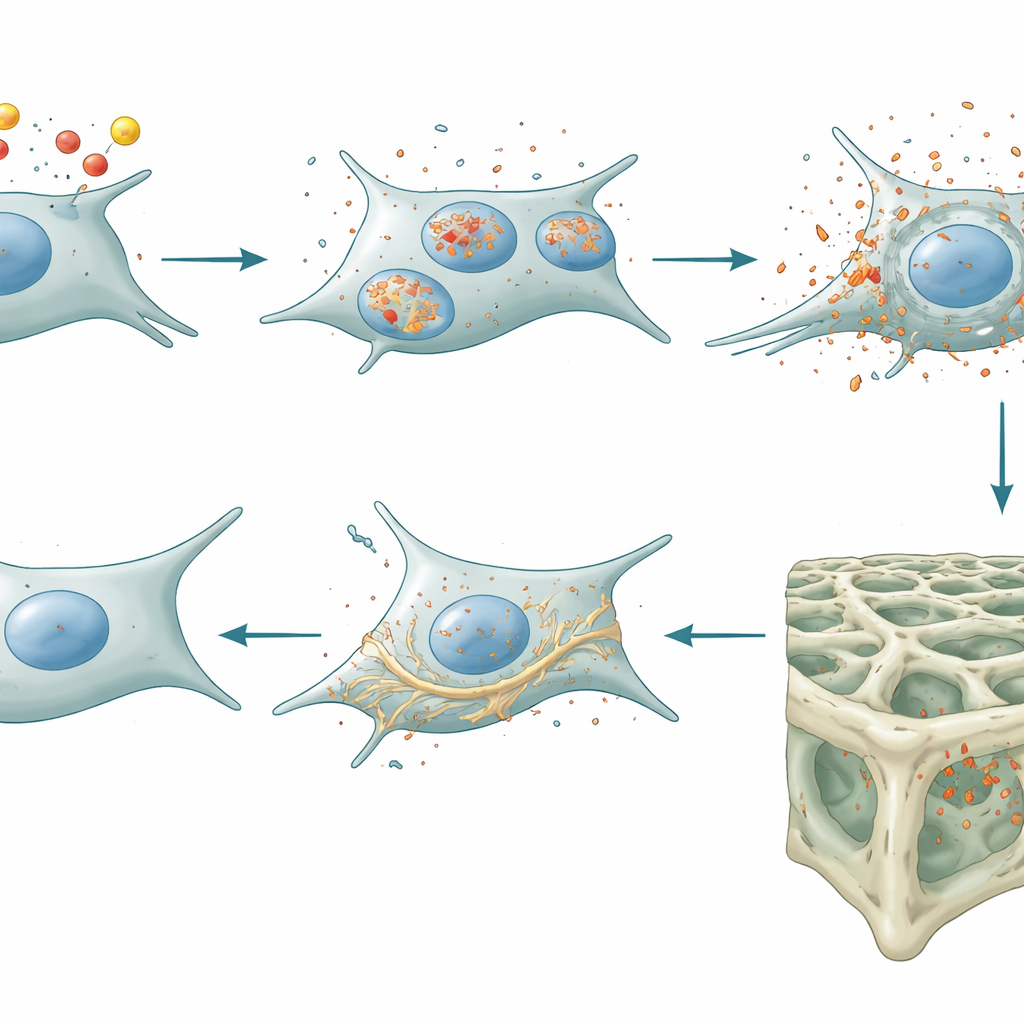
从细胞应激到骨质变弱,以及解除“刹车”如何有益
随后研究者在完整小鼠模型中专门删除了晚期成骨细胞和骨细胞中的脂质运载蛋白‑2。他们发现这些动物的骨细胞内铁含量较低,并显示出更强的抗氧化防御以抵抗铁死亡。重要的是,这些小鼠还产生较低水平的两种关键抑制蛋白——sclerostin 和 DKK1,这两者通常作为 Wnt/β‑catenin 通路的“刹车”,而该通路是骨形成的重要驱动因子。随着这些抑制被解除,促进成骨细胞的信号增强。微型CT 扫描和骨形成标记实验证实了结果:缺乏骨细胞脂质运载蛋白‑2 的小鼠构建了更多且连通性更好的松质(小梁)骨,主要是通过提升骨形成而非抑制骨吸收。尽管骨骼发生这些变化,它们的体重、血糖控制、代谢和活动水平保持正常,说明该效应局限于骨内,而非全身性激素效应。
这对维持骨强壮意味什么
简言之,这项工作表明骨细胞内的脂质运载蛋白‑2 像一个局部开关,提高铁水平、削弱线粒体、使细胞易受铁死亡损伤并抑制一条关键生长通路,从而共同限制新骨形成。当这个内部“刹车”被移除时,骨细胞更健康,发出更多促进成骨的信号,松质骨变得更致密且连通性更好,而总体代谢不受影响。鉴于脂质运载蛋白‑2 水平和铁失衡都会随着年龄增长和慢性炎症而上升,针对脂质运载蛋白‑2—受体系统或可提供一种新的策略,保护骨骼免于从内向外“生锈”。
引用: Khanal, V., Carroll, M., Moradi, F. et al. Osteocytic Lipocalin-2 regulates bone formation locally through iron-dependent ferroptosis and Wnt suppression. Cell Death Discov. 12, 113 (2026). https://doi.org/10.1038/s41420-026-02956-9
关键词: 骨骼健康, 骨细胞, 铁代谢, 铁死亡, Wnt 信号