Clear Sky Science · zh
胰腺癌中的线粒体自噬:机制见解及新型治疗策略的启示
为何细胞的“发电厂”在胰腺癌中至关重要
胰腺导管腺癌是死亡率极高的癌症之一,部分原因在于肿瘤迅速学会抵抗几乎所有可用治疗。本文综述探讨了一个出人意料的抗性因素:线粒体自噬——细胞识别并回收受损线粒体的内建机制,线粒体是负责能量产生的微小“发电厂”。理解胰腺癌如何劫持这一清理程序,可能为更有效、持久的治疗开辟新途径。
细胞清理队与癌症的生存伎俩
线粒体不仅仅负责产生能量;它们还参与代谢调控、细胞凋亡以及处理称为活性氧(ROS)的有害分子。当线粒体受损或数量过多时,细胞通过线粒体自噬对其标记并清除。这一过程主要通过两条途径实现。一是被称为PINK1/Parkin通路,依靠损伤传感器PINK1和标记酶Parkin将受损线粒体标记以便降解。另一种则依赖位于线粒体表面的受体蛋白,例如BNIP3、NIX和FUNDC1,直接将线粒体与细胞的“废物回收囊”自噬体连接,而无需相同的标记步骤。这些通路常常协同工作,使细胞能够在低氧或药物暴露等压力下灵活调整线粒体库。 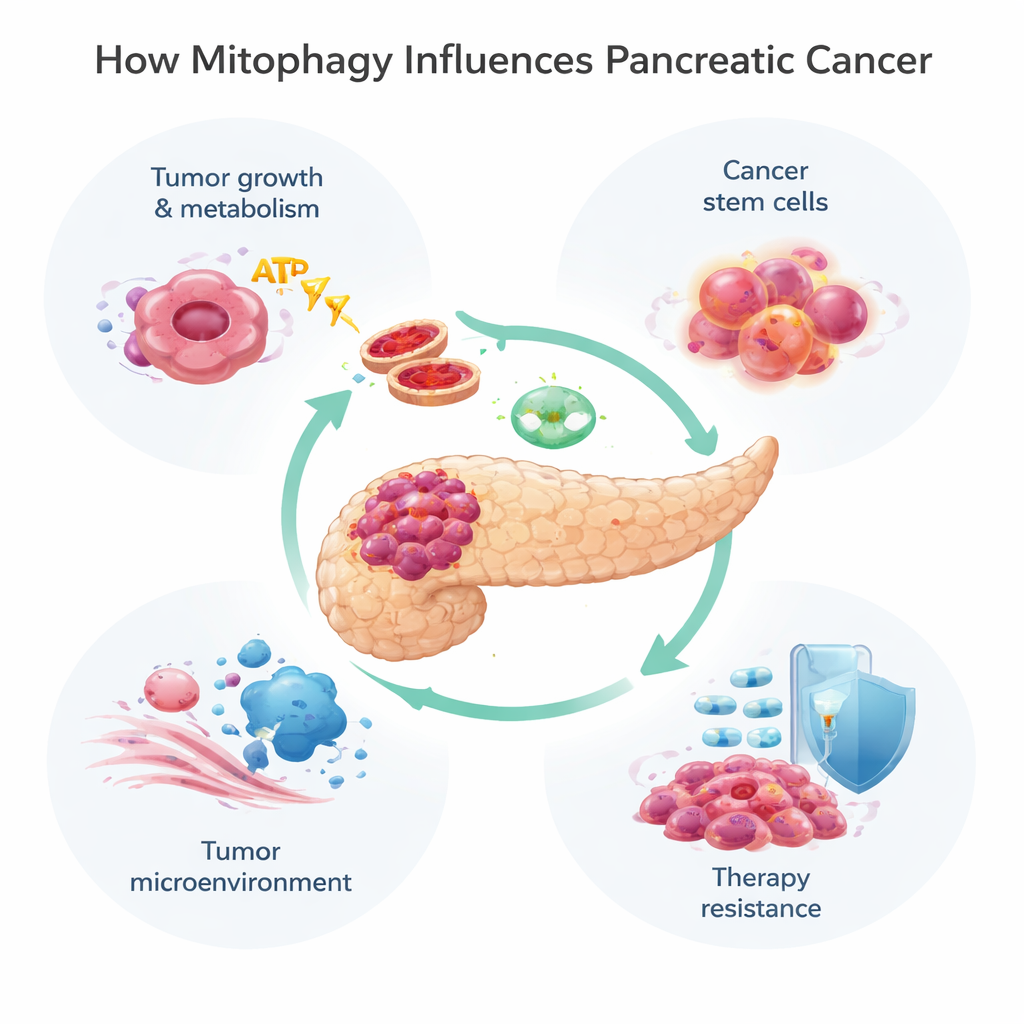
胰腺肿瘤如何重塑能量利用
胰腺肿瘤生存在恶劣的环境:血氧供应不足,并被致密的类瘢痕组织包围。为求生存,癌细胞会重编能量系统,常常从依赖线粒体的氧化呼吸转向更原始的糖酵解过程。线粒体自噬有助于微调这一转变。在肿瘤早期,PINK1或Parkin的丢失会通过导致铁离子堆积、活性氧增多并推动向糖酵解转变,从而加速癌变。与此同时,另一种线粒体自噬蛋白NIX可以移除仍然功能正常的线粒体,进一步将细胞推向糖酵解代谢并促进更快速的生长。相比之下,BNIP3的模式更为复杂:它在早期出现,且在许多晚期肿瘤中被沉默,而当其恢复表达时可以减缓癌细胞生长,提示某些线粒体自噬通路可能抑制癌症,而其他通路则助长癌症。
癌症干细胞与肿瘤微环境
并非所有癌细胞都相同。一小部分通常被称为癌症干细胞,具有自我更新、播散新肿瘤并特别能抵御化疗的能力。在胰腺癌中,这些细胞依赖线粒体自噬以保持代谢灵活性。一种叫ISG15的修饰蛋白支持这一过程并维持其干性特征,将线粒体自噬直接与复发和治疗失败联系起来。除癌细胞本身外,线粒体自噬也塑造肿瘤微环境——肿瘤周围的支持细胞、免疫细胞和结缔组织的混合体。例如,癌相关成纤维细胞可能被驱动进入“反沃伯格效应”,它们自身增强线粒体自噬和糖酵解,然后以富能产物供养肿瘤。线粒体自噬还影响免疫细胞识别和攻击癌症的方式,通过改变诸如MHC‑I等免疫标志的展示,以及肿瘤用来伪装的制动分子如PD‑L1的水平。
为何阻断或增强清理会改变药物反应
许多胰腺癌的标准和试验性治疗(包括化疗药物吉西他滨以及针对常见KRAS‑G12D突变的新靶向药物)都会损伤线粒体。肿瘤细胞常通过启动线粒体自噬来应对,清除损伤以逃避死亡。研究表明,PINK1驱动的线粒体自噬可以削弱化疗和某些天然化合物的杀伤作用,帮助癌细胞存活。另一方面,在特定条件下,过度诱导线粒体自噬——尤其通过BNIP3和NIX——可能剥夺细胞过多功能线粒体,使其陷入能量危机并促进细胞死亡。这种双重性意味着线粒体自噬既能保护肿瘤免受治疗,也能在以正确方式被推动时使其更脆弱。 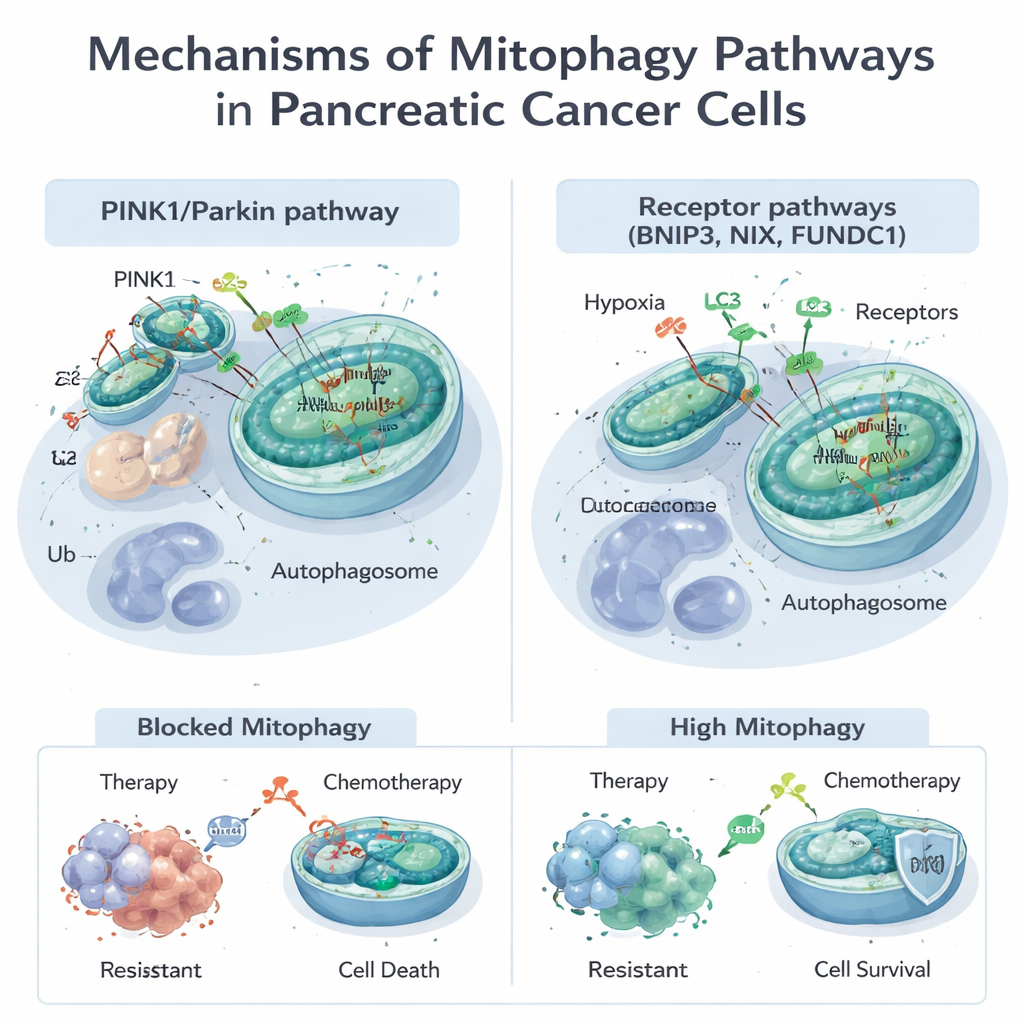
新治疗思路与精准匹配患者的必要性
由于线粒体自噬处在代谢、应激反应与细胞死亡的交汇点,它成为组合疗法的有吸引力目标。目前的药物策略多为间接作用:一些化合物干扰线粒体分裂与融合;另一些如氯喹和羟氯喹通过阻断自噬体与酸性降解区融合来抑制回收过程的最后阶段。若干临床试验正在测试这些药物与胰腺癌标准化疗的联合疗法。然而迄今结果喜忧参半——部分患者获益,另一些则无效。问题的一部分在于肿瘤在其基础线线粒体自噬和代谢特征上差异巨大:有的严重依赖线粒体呼吸,有的则更依赖糖酵解。作者认为,未来的成功将依赖于更好的生物标志物和基因签名,以根据线粒体自噬活性和能量利用对患者分层,并开发更精确的药物,选择性地调整特定的线粒体自噬通路,而不是粗暴地开启或关闭自噬。对非专业读者来说,关键结论是:学会识别并谨慎调控这一线粒体清理系统,可能有助于把胰腺癌从难以战胜的敌人,变为更可控的疾病。
引用: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
关键词: 胰腺癌, 线粒体自噬, 线粒体, 化疗耐药, 肿瘤代谢