Clear Sky Science · zh
经预激的间充质干细胞通过 Itgb2-Rac1 轴增强巨噬细胞亚群转换与吞噬凋亡细胞能力,从而减轻血吸虫病相关纤维化
减轻一种常见寄生虫导致的肝部瘢痕
血吸虫病是一种影响全球超两亿人的寄生虫病,即便虫体被清除后,常在肝脏留下顽固的瘢痕。这样的瘢痕被称为纤维化,可能进展为肝硬化和危及生命的肝功能衰竭。本研究探索了一种新的细胞疗法思路,通过教导机体自身的免疫细胞更有效地清理损伤,为逆转寄生虫诱导的肝脏瘢痕提供了新的切入点。
为何肝脏瘢痕难以愈合
当血吸虫在肝脏产卵时,免疫系统会在卵周形成紧密的细胞簇——肉芽肿。随着时间推移,这种保护性反应会沉积过量的瘢痕组织,使肝脏逐渐僵硬。巨噬细胞在这一过程中发挥关键作用:一种被称为“炎性”巨噬细胞的亚型通过释放促损伤的化学信号助长病情;而另一种更偏向“修复”的亚型则有助于分解瘢痕组织并平息炎症。本研究的核心问题是我们是否能够安全地将巨噬细胞从有害状态推动到有利于愈合的状态。
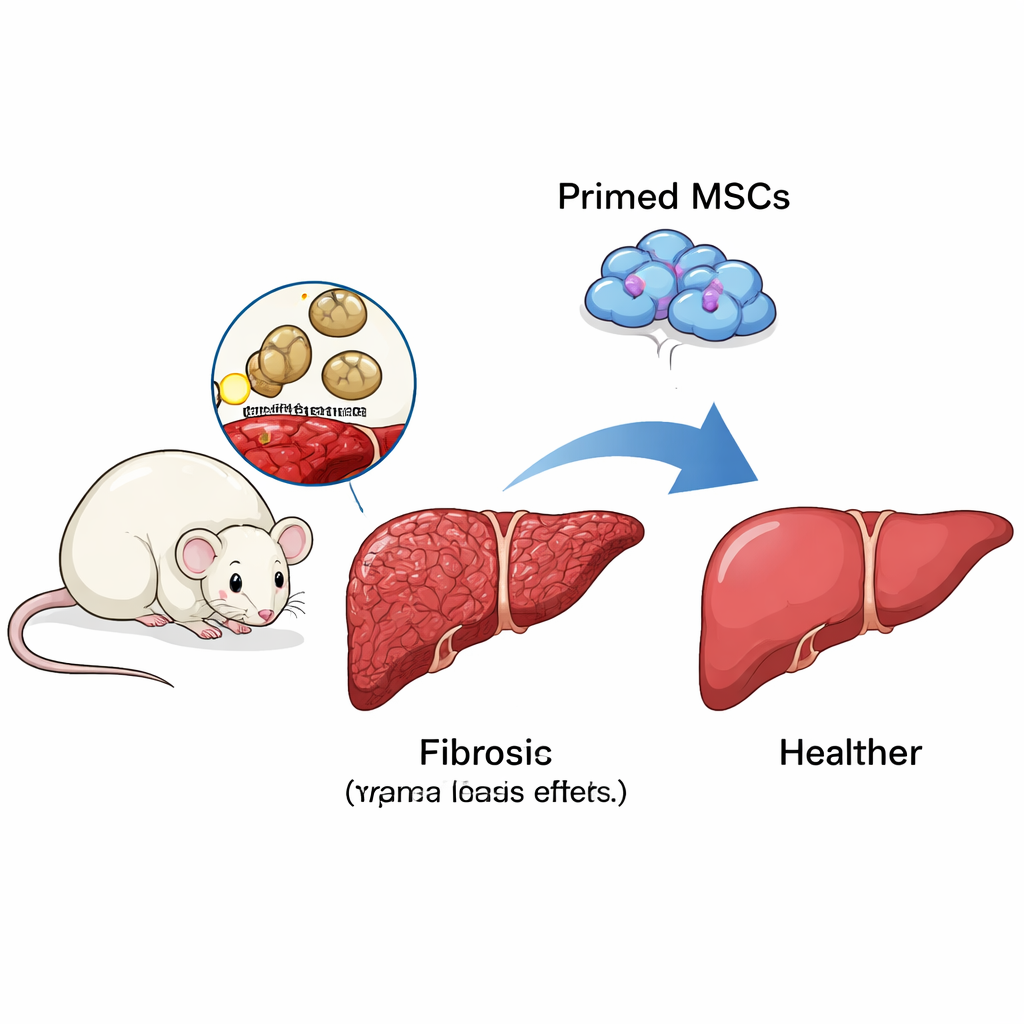
训练干细胞以引导免疫系统
间充质干细胞(MSCs)是存在于骨髓及其他组织中的多能细胞,被视为治疗肝纤维化的潜在候选。然而,单独使用时,疗效并不稳定。研究人员发现,在体外用两种免疫刺激信号 IFN‑γ 和 LPS 对 MSCs 进行“预激”后,在感染日本血吸虫的小鼠中其疗效显著提升。与未处理或接受未预激 MSCs 的动物相比,接受预激 MSCs 的小鼠肝脏肉眼更健康、体重恢复更好,显微镜下肉芽肿更小、胶原沉积减少。成纤维细胞活化的标志物也下降,表明纤维化确实减少,而不仅仅是表面改善。
重编程机体的清理队伍
进一步研究表明,预激 MSCs 对巨噬细胞行为产生了显著影响。在处理过的肝脏中,炎性巨噬细胞数量减少,而更有利于分解瘢痕的修复型巨噬细胞增多。与此同时,经典炎性分子的水平下降,而有助伤口愈合的因子则保持在一种平衡范围,而不是被极端驱动。当研究者阻断新进炎性巨噬细胞迁入肝脏时,修复型细胞的数量和纤维化改善均减弱。这表明预激 MSCs 并非简单地补充新细胞,而是将进入的炎性巨噬细胞转化为更为和平、以修复为导向的表型。
帮助巨噬细胞通过吞噬走向愈合
研究接着聚焦于一种称为吞噬凋亡细胞(efferocytosis)的过程——有序地“吞食”死亡细胞,特别是耗尽的中性粒细胞。在接受预激 MSCs 的感染小鼠肝脏中,巨噬细胞更常见到吞噬了中性粒细胞的证据,显示清理活动增强。在体外培养中,暴露于预激 MSCs 的巨噬细胞更擅长吞噬带标记的凋亡中性粒细胞,并且其基因表达同时倾向于修复型谱。研究人员鉴定出这一改变的关键分子开关:巨噬细胞表面的受体 Itgb2,它与细胞内控制细胞骨架与吞噬动作的开关 Rac1 通讯。预激 MSCs 提升了 Itgb2 与 Rac1 的活性;阻断任一环节都会显著降低吞噬凋亡细胞的能力,并逆转向修复型巨噬细胞的转变。
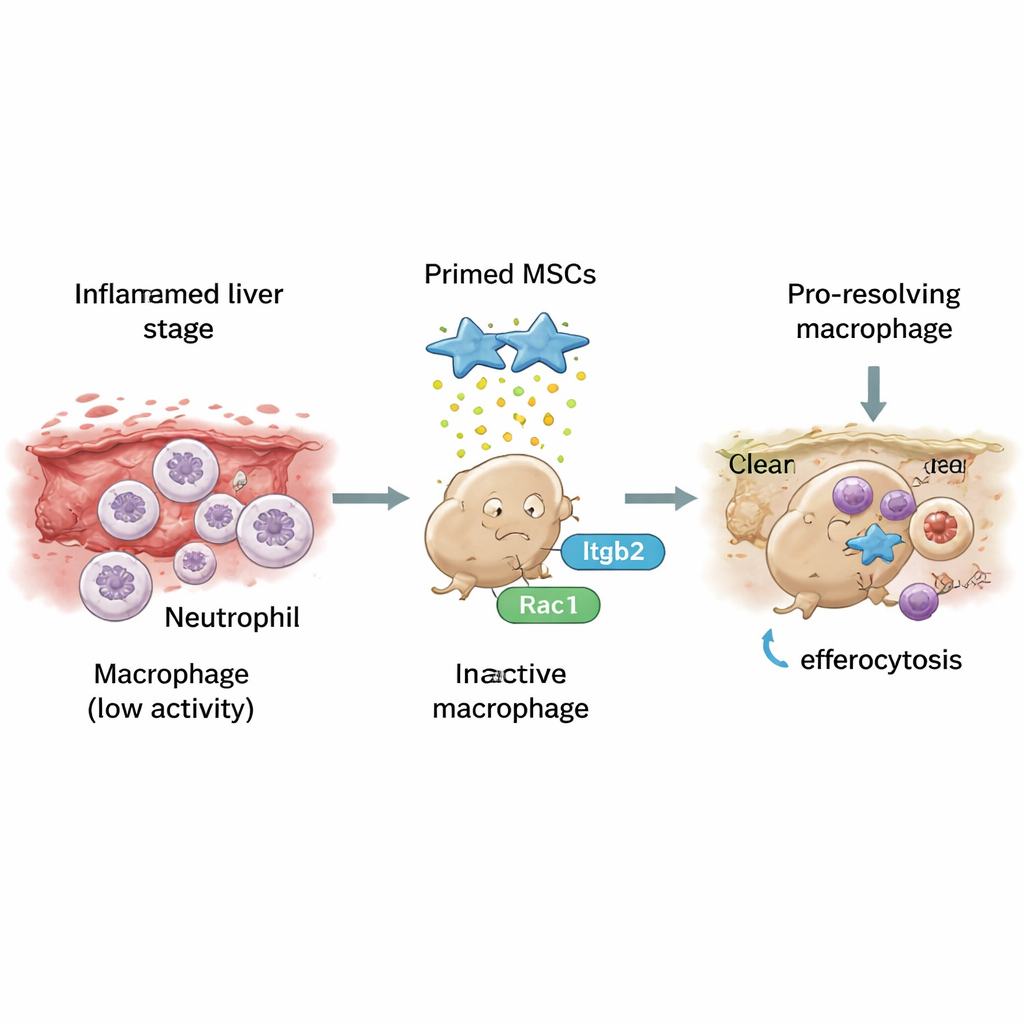
这对未来治疗意味着什么
简而言之,这项工作表明,经过特殊预激的干细胞可以像“教练”一样引导血吸虫病后的免疫细胞,促使它们停止助长炎症,而更有效地清除碎屑和瘢痕组织。通过激活 Itgb2–Rac1 通路,这些预激 MSCs 帮助巨噬细胞顺利处置死亡细胞,随后采纳有助于消退瘢痕的表型。尽管在将该方法用于人体之前还需大量工作,但该研究为设计基于 MSC 的疗法提供了清晰的机制路线图,表明这些疗法不仅能抑制损伤,还能积极帮助肝脏在寄生虫感染后重建自己。
引用: Lei, J., Ren, Y., Chen, Z. et al. Primed mesenchymal stem cells attenuate schistosomiasis fibrosis by enhancing macrophage subset switching and efferocytosis via Itgb2-Rac1 axis. Cell Death Discov. 12, 97 (2026). https://doi.org/10.1038/s41420-026-02947-w
关键词: 血吸虫病, 肝纤维化, 间充质干细胞, 巨噬细胞, 吞噬凋亡细胞