Clear Sky Science · zh
结直肠癌来源的骨桥蛋白通过 PI3K/AKT/CSF1-CSF1R 轴将巨噬细胞重编程为促转移的 M2 状态
这对结肠癌患者为何重要
结直肠(结肠和直肠)癌多数死亡并非由原发肿瘤本身直接造成,而是由于癌症转移到其它器官所致。本研究考察了癌细胞如何与邻近的免疫细胞“对话”以促进肿瘤扩散。通过揭示癌细胞发送的一种关键信号,能将免疫细胞重新编程为帮凶而非战士,研究为延缓或阻止晚期结直肠癌转移提供了新的治疗策略线索。
一种有黏性的蛋白与它的黑暗面
研究者关注一种称为骨桥蛋白(osteopontin,缩写 OPN)的蛋白,该蛋白由肿瘤细胞及肿瘤内的某些免疫细胞产生。长期以来,OPN 与多种癌症的不良预后相关,但其在结直肠癌中如何促进转移尚不清楚。通过分析大规模患者数据库和肿瘤样本,团队发现结直肠癌组织中 OPN 水平明显高于正常结肠组织,尤其在病情进展和远处转移的患者中更高。肿瘤中 OPN 含量较高的患者总体生存较差,表明 OPN 与侵袭性、难治的癌症密切相关。
并非只有癌细胞本身在作祟
令人意外的是,当科研人员在体外强制使结直肠癌细胞产生更多或更少的 OPN 时,这些癌细胞自身并没有变得更具侵袭性或迁移性。它们的增殖、迁移以及穿透人工膜的能力变化很小。这一发现挑战了 OPN 主要通过直接增强癌细胞自身能力来起作用的常见观点。研究团队转而关注肿瘤的“邻里”——即肿瘤微环境,特别是一类名为巨噬细胞的免疫细胞,这些细胞可以处于攻击肿瘤的“M1”状态,也可以处于支持肿瘤的“M2”状态。
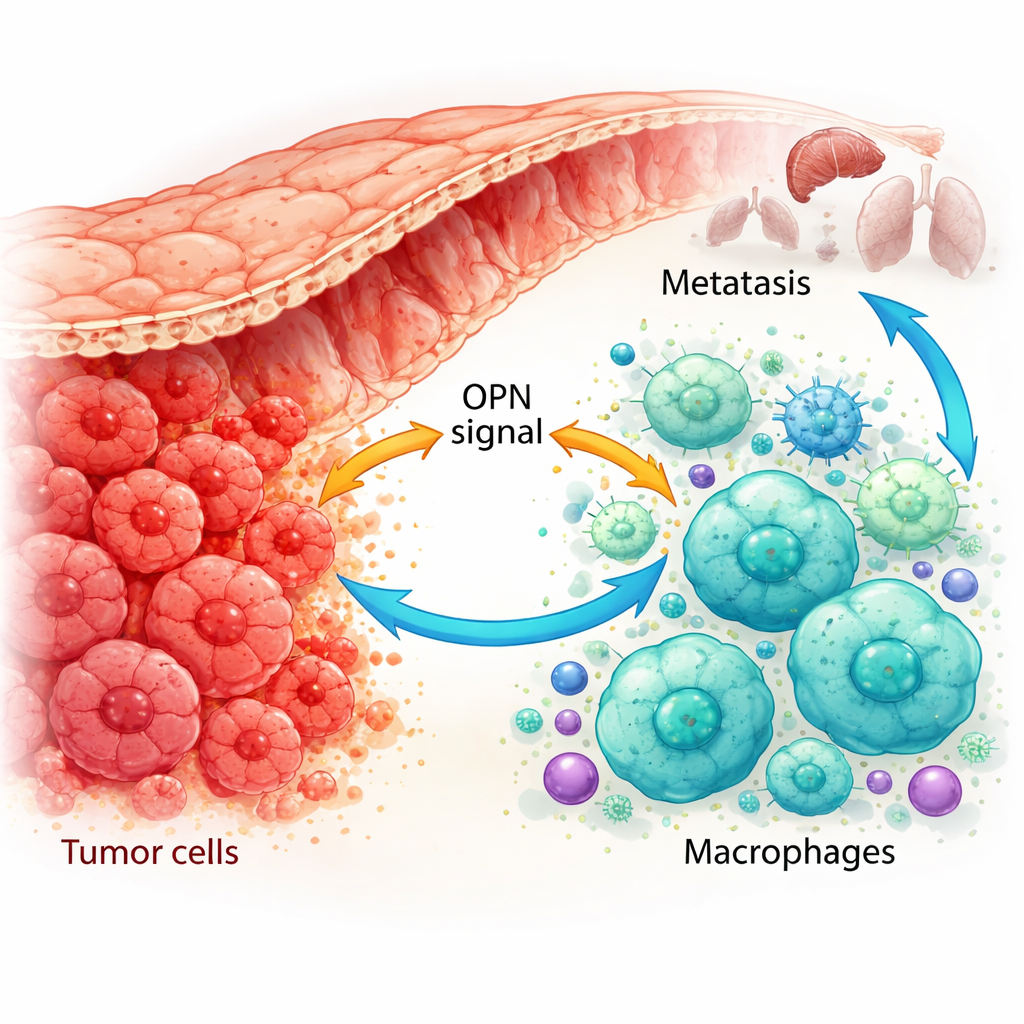
免疫细胞如何被重编程为肿瘤帮手
利用单细胞基因组图谱和对患者组织的高级染色技术,研究者显示 OPN 不仅由癌细胞产生,也由肿瘤相关巨噬细胞产生。在已发生转移的肿瘤中,癌细胞和某一特定亚型的巨噬细胞都富含 OPN。这类巨噬细胞倾向于呈现 M2 样、支持肿瘤的状态,并且当肿瘤 OPN 水平高时其数量更多。在小鼠模型中,工程化产生更多 OPN 的肿瘤吸引了更多这些 M2 样巨噬细胞并生长更快,而减少 OPN 的肿瘤则伴随更少的 M2 巨噬细胞并生长更慢。这提示 OPN 是一个强有力的巨噬细胞招募者和重编程因子。
通向转移的隐秘信号链
为弄清分子事件链,团队将产生不同含量 OPN 的结直肠癌细胞与人源巨噬细胞共同培养。他们发现,高 OPN 的癌细胞促使巨噬细胞向 M2 状态转化,并鼓励了双向的移动:巨噬细胞向肿瘤迁移,而肿瘤细胞则响应这些巨噬细胞的信号变得更具侵袭性。进一步研究表明,OPN 在巨噬细胞内激活了一条名为 PI3K/AKT 的信号通路。这一激活反过来促使巨噬细胞大量释放另一种分子 CSF1,并在其表面增加该分子的受体 CSF1R。CSF1 随后以回路方式进一步强化 M2 的促转移状态,并持续吸引巨噬细胞进入肿瘤。
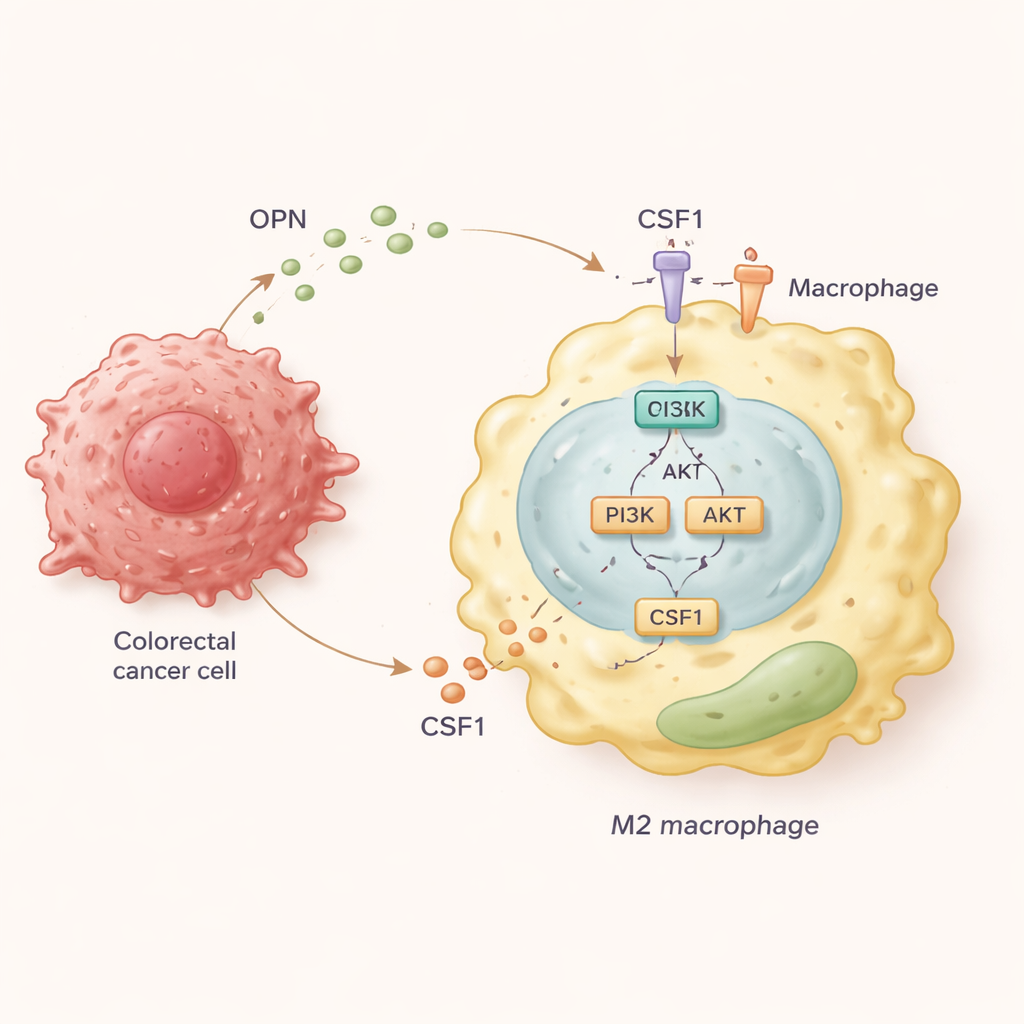
阻断这一回路以减缓扩散
在腹腔内已发生转移的结直肠癌小鼠模型中,研究人员测试了一种名为 PLX3397 的 CSF1R 阻断药。携带高 OPN 肿瘤的小鼠出现了许多转移结节,但采用 CSF1R 抑制剂治疗显著减少了转移数量和肿瘤中 M2 样巨噬细胞的存在。肿瘤细胞显示出更少的生长和更多的程序性细胞死亡迹象。重要的是,该药物主要耗竭了促进肿瘤的巨噬细胞而并未大幅影响更具炎症性的那类巨噬细胞,提示这是一种相对有针对性的方法来削弱肿瘤的支持系统。
这对未来治疗意味着什么
对非专业读者而言,主要信息是:一些结直肠癌之所以能够成功转移,不仅因为癌细胞本身具有侵袭性,更因为它们劫持邻近的免疫细胞并将其变成帮凶。本研究表明,癌细胞来源的 OPN 像一个主开关,通过 PI3K/AKT 和 CSF1/CSF1R 信号链重编程巨噬细胞,营造出有利于转移的微环境。通过打断这一链条——尤其是在 CSF1R 这一环节——研究者在小鼠中能够减少肿瘤扩散。这提示检测 OPN 水平可能有助于识别可能从针对巨噬细胞的药物中受益的患者,并且将此类药物与现有治疗或免疫疗法组合,可能为晚期结直肠癌患者带来新的希望。
引用: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
关键词: 结直肠癌, 骨桥蛋白, 肿瘤相关巨噬细胞, 转移, CSF1R 抑制