Clear Sky Science · zh
针对 NXPH4/ALDH1L2 信号通路可抑制前列腺癌对恩杂鲁胺的耐药性
这对前列腺癌患者有何意义
许多晚期前列腺癌患者依赖一种强效的雄激素阻断药物——恩杂鲁胺。起初它常常效果显著,能够缩小肿瘤并延缓病情进展。但在大多数患者中,癌症最终会找到绕过药物的办法并再次生长。本研究深入探讨了这种逃逸机制,并指出了耐药肿瘤中的一个新的薄弱环节——为使现有治疗更持久、更有效提供了潜在途径。
常用治疗遇到顽固疾病
前列腺癌的生长与雄性激素(或称雄激素)密切相关,这些激素通过一种称为雄激素受体的蛋白发挥作用。恩杂鲁胺旨在关闭该受体,是当肿瘤对传统降雄激素治疗不再敏感时的标准疗法。不幸的是,许多肿瘤会适应,成为临床所称的去势抵抗性前列腺癌。本文作者着手发现哪些基因帮助癌细胞在恩杂鲁胺存在下存活,希望阻断这些帮手能恢复药物的效力。
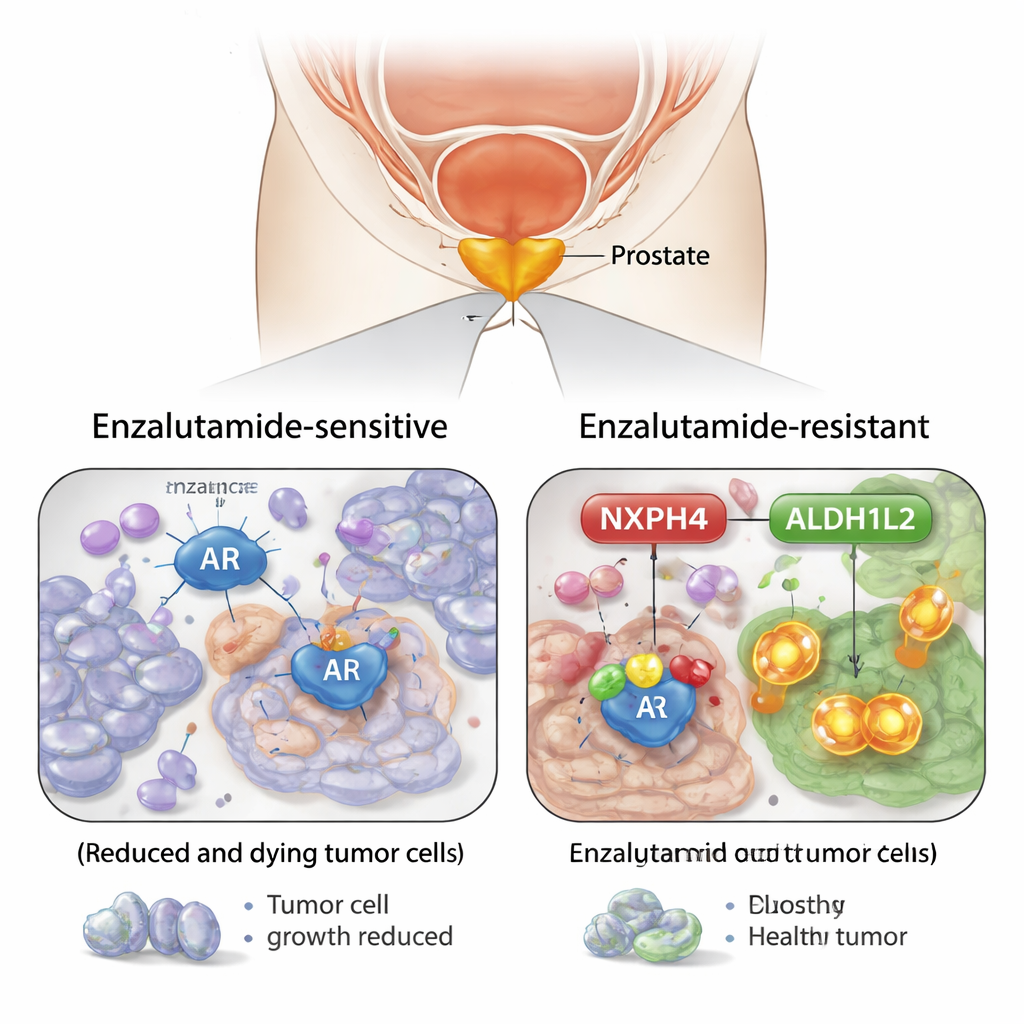
聚焦一个意外的助力分子
通过比较对恩杂鲁胺敏感的前列腺癌细胞与已产生耐药的细胞,研究团队鉴定出一种名为 NXPH4 的蛋白为关键因素。耐药细胞产生的 NXPH4 多得多,并且在细胞长期暴露于恩杂鲁胺时其水平稳步上升。患者的组织样本显示出相同模式:更具侵袭性的肿瘤和对药物不再响应的癌症中 NXPH4 水平更高。当研究人员在耐药细胞中降低 NXPH4 水平时,这些细胞对恩杂鲁胺更易被杀死并在培养皿和小鼠体内形成的克隆更少。相反,强迫细胞过表达 NXPH4 则使其更难以治疗。
雄激素如何推动 NXPH4 激活
研究还探究了为何这些肿瘤中 NXPH4 丰富。答案再次指向雄激素受体。研究人员显示,当细胞处理二氢睾酮(DHT)时,NXPH4 水平上升;额外添加雄激素受体时,NXPH4 增加;阻断受体时,NXPH4 降低。详细的 DNA 实验证实,雄激素受体物理结合于 NXPH4 基因的调控区,启动其表达。这意味着推动前列腺癌生长的同一激素驱动系统也为细胞准备了 NXPH4,铺垫了之后产生药物耐受的条件。
为细胞“发电厂”加速
进一步挖掘表明,NXPH4 改变了癌细胞在其线粒体——细胞内微小的能量工厂——中管理能量与应激的方式。在阻断激素条件下,一部分 NXPH4 转移到线粒体并与另一种蛋白 ALDH1L2 结合,该蛋白对于生成 NADPH 至关重要。NADPH 是一种帮助控制有害活性氧(ROS)的关键分子。在耐药细胞中,NXPH4 与 ALDH1L2 形成复合体,增强线粒体的“呼吸”、维持膜电位、增加 NADPH 水平并降低 ROS。这一组合使线粒体保持功能,从而让癌细胞能承受恩杂鲁胺引发的应激,而不是像通常那样死亡。
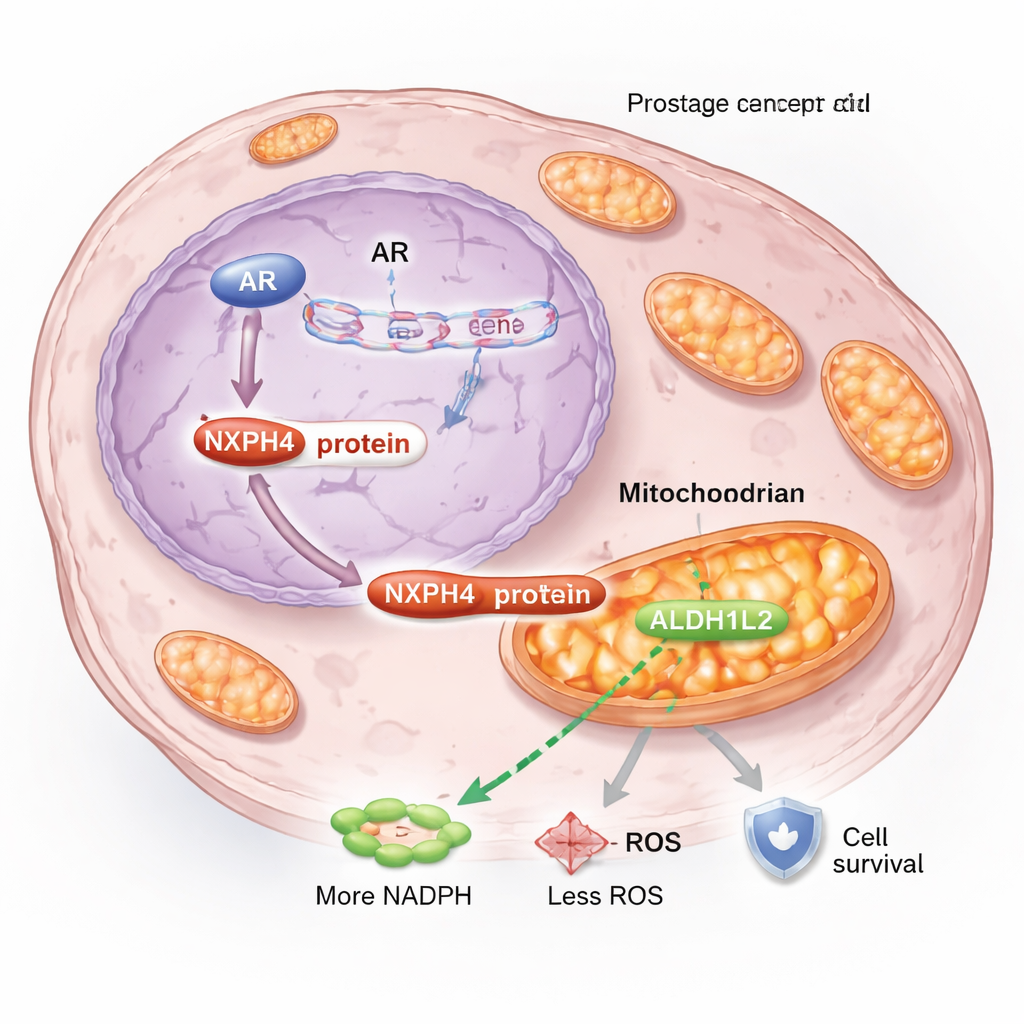
打破耐药回路
当研究人员破坏这一线粒体支持系统时,结果令人瞩目。在耐药细胞中敲低 NXPH4 会降低线粒体活性、提高氧化应激、减缓生长,并使细胞对恩杂鲁胺更为敏感。沉默 ALDH1L2 也有类似效果,并抹除了过表达 NXPH4 的保护效应,证实这两种蛋白协同作用。在小鼠模型中,缺乏 NXPH4 的肿瘤生长更慢;将 NXPH4 缺失与恩杂鲁胺联合使用,比单独任一方法使肿瘤缩小得更多。这些发现表明 NXPH4–ALDH1L2 伙伴关系不仅是耐药的副产物,而是其驱动因素之一。
这对未来治疗可能意味着什么
简言之,这项工作表明一些前列腺癌通过重构其能量供应来在恩杂鲁胺下存活。由雄激素受体激活的 NXPH4 与 ALDH1L2 在内线粒体中联合工作,使线粒体持续运转、抵御氧化损伤,帮助肿瘤细胞度过激素阻断治疗。针对 NXPH4 或其与 ALDH1L2 的相互作用,可能削弱这一生存回路。尽管针对 NXPH4 的药物尚不存在,但该研究将这对分子标识为有前景的新靶点。未来,将恩杂鲁胺与破坏 NXPH4‑ALDH1L2 信号的药物联合使用,或能帮助患者更长时间地领先于耐药前列腺癌。
引用: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
关键词: 前列腺癌, 恩杂鲁胺耐药, 线粒体代谢, NXPH4, ALDH1L2