Clear Sky Science · zh
罗特林触发SLC7A11与GPX4的双重降解以驱动肝细胞癌的铁死亡并增强化疗敏感性
为何这种天然化合物对肝癌重要
肝细胞癌是最常见的原发性肝癌类型,通常诊断较晚且难以治疗。本研究探讨了一种植物来源的分子——罗特林,长期以来以其广泛的抗癌作用为人所知,是否可以被用来在肝癌细胞中诱导一种较新的细胞死亡方式:铁死亡。通过解析罗特林在分子水平上的作用机制,研究者希望为更有效且不易被耐药的治疗打开新途径。
杀死癌细胞的新方式
传统抗癌药物通常将肿瘤细胞推入已知的死亡程序,如凋亡。铁死亡不同:它是一种依赖铁的过程,由细胞膜中有毒脂质的积累驱动。肝癌细胞特别容易受到此类损伤,因为它们高度依赖抗氧化系统来遏制这些基于脂质的毒性物质。研究团队探讨了罗特林是否能够破坏这些防御,从而迫使肝癌细胞进入铁死亡。
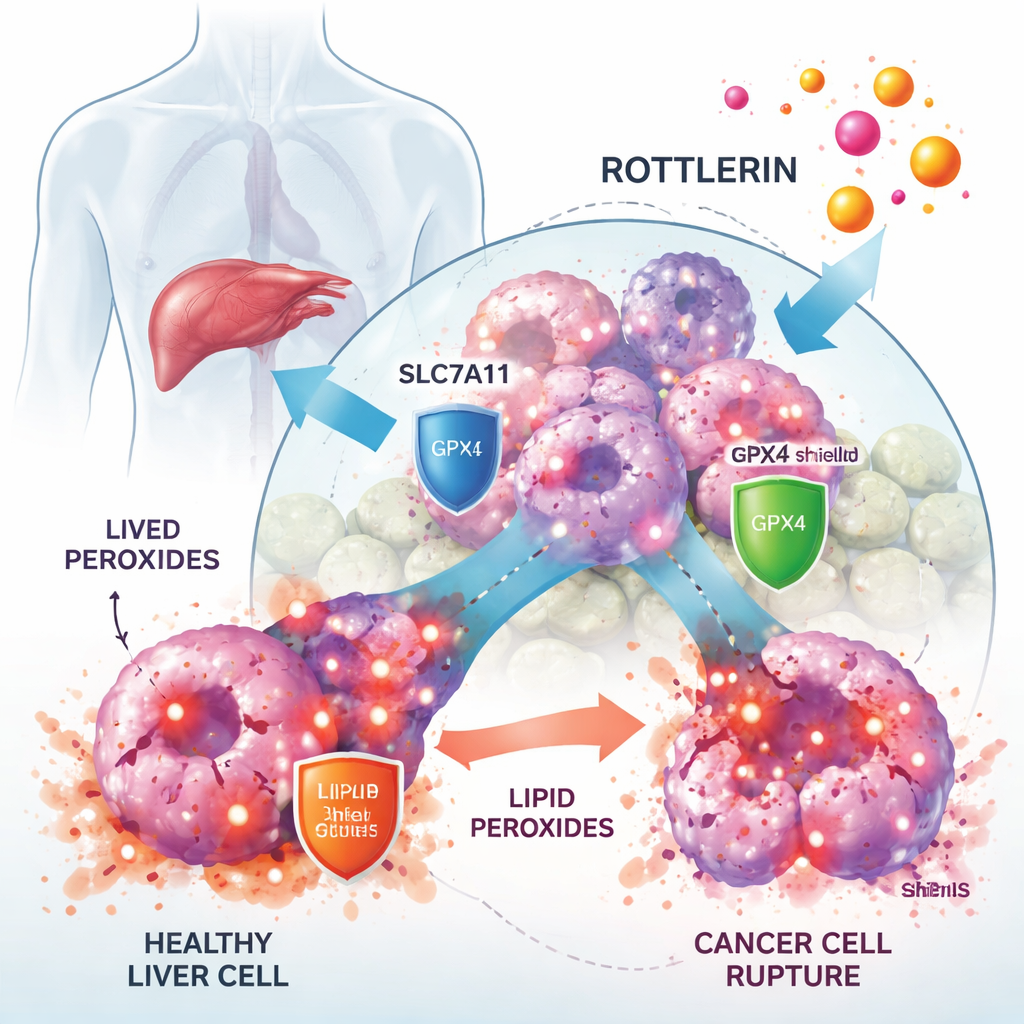
罗特林如何减缓肿瘤生长
在人体肝癌细胞系中,研究者显示罗特林在低微摩尔浓度即可显著抑制癌细胞生长,而与之相比,正常肝相关细胞受影响较小。当加入一种名为Ferrostatin‑1的特异性铁死亡抑制剂时,大部分由罗特林引起的细胞死亡被挽救,这强烈暗示铁死亡是主要的杀伤方式。显微镜观察和生化检测也支持这一点:罗特林处理的细胞积累了大量脂质过氧化物、线粒体发生改变并且抗氧化分子谷胱甘肽减少——这些都是铁死亡的标志。
瓦解细胞的抗氧化屏障
肝癌细胞依赖由转运蛋白SLC7A11和酶GPX4构成的一条关键防御轴生存。SLC7A11输入胱氨酸,胱氨酸是合成谷胱甘肽的构件,而GPX4用谷胱甘肽中和脂质过氧化物以防止膜损伤。研究发现罗特林随着时间使SLC7A11和GPX4的蛋白水平下降。这并非因为细胞停止合成这些蛋白,而是这些蛋白被打上小的“销毁我”标签(泛素)并送入细胞的蛋白降解机器——蛋白酶体。阻断蛋白酶体可以逆转这种丢失,而人为提高细胞中SLC7A11或GPX4的表达则能部分保护细胞免受罗特林的伤害。综上,这些发现表明罗特林作为两条核心铁死亡防线的双重降解剂发挥作用。
增强现有肝癌药物的疗效
许多晚期肝癌患者接受索拉非尼治疗,这是一线标准药物,且本身可诱导铁死亡,但耐药常限制其疗效。作者测试了低剂量、单独作用较弱的罗特林是否能使肿瘤细胞对诱导铁死亡的药物(如索拉非尼和RSL3)更敏感。在细胞培养中,低剂量罗特林与任一药物联合显著增加了癌细胞死亡并使剂量—反应曲线向低剂量移动,表明效力增强。重要的是,即使经典的罗特林靶点蛋白PKCδ在基因水平被下调,这种增敏效应仍然存在,显示关键作用并非通过该激酶,而是通过降解SLC7A11和GPX4来实现。在携带人体肝瘤的小鼠模型中,罗特林与索拉非尼联合治疗比单用索拉非尼更能减缓肿瘤生长,并进一步降低肿瘤中SLC7A11和GPX4的水平。
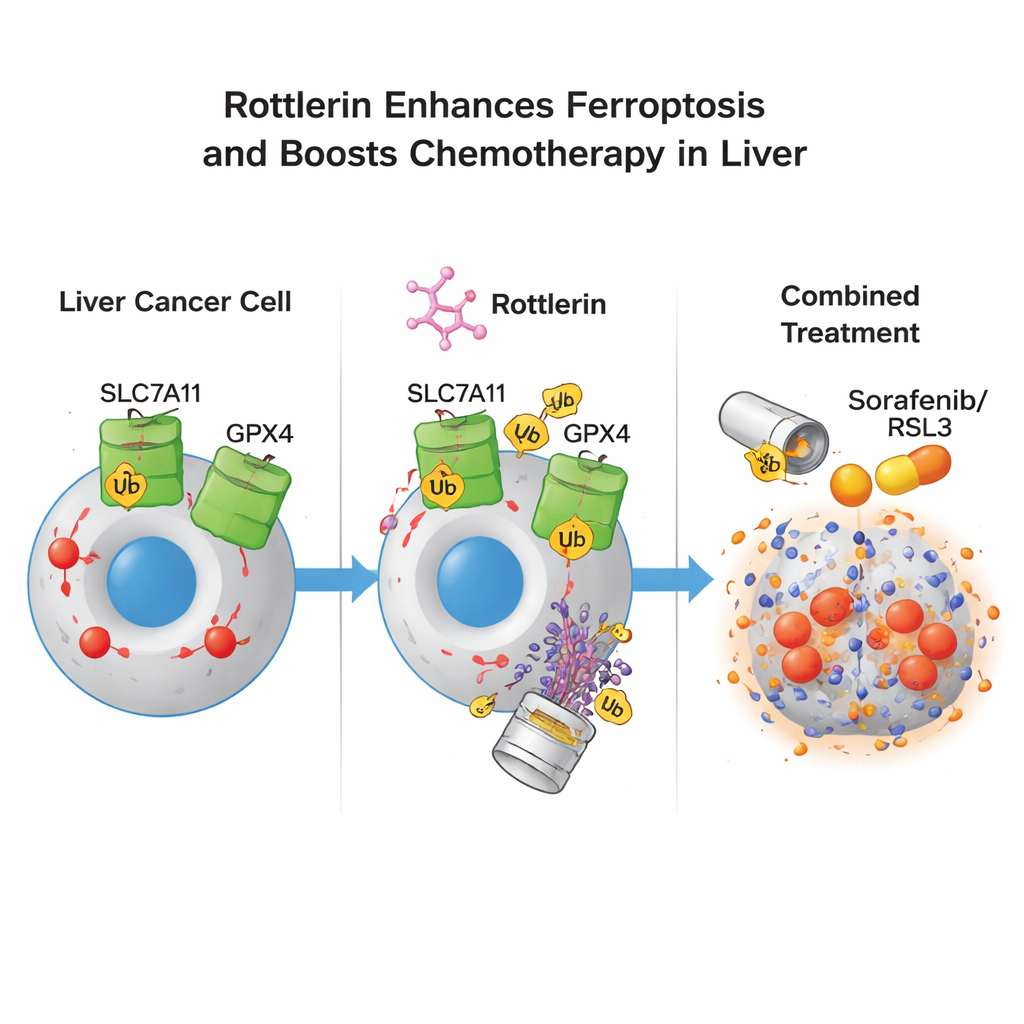
这对未来治疗的意义
对非专业读者而言,结论是:罗特林像一把“双锁开匠”的工具同时破解肝癌细胞的两道关键锁——SLC7A11和GPX4——这两者通常保护细胞免受一波致命的脂质氧化攻击。一旦这些“锁”被移除,癌细胞在与促铁死亡的现有药物联合使用时就更容易经历铁死亡。尽管在将罗特林或相关化合物用于患者之前还需要更多研究,这种双重降解策略为克服使肝瘤难以治疗的适应性防御提供了一个有希望的途径。
引用: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
关键词: 肝癌, 铁死亡, 罗特林, SLC7A11, GPX4