Clear Sky Science · zh
用小分子口服药 NXP800 激活 GCN2 并随后诱导未折叠蛋白反应以延缓骨肉瘤肿瘤生长
将癌细胞的应激转化为弱点
骨肉瘤是一种罕见但侵袭性强的骨肿瘤,多见于儿童和青少年。几十年来的治疗依赖于强烈的化疗和手术,但对于晚期患者的生存率几乎没有改善。本研究探讨了一种名为 NXP800 的新口服药,它旨在利用癌细胞的一个隐蔽弱点:持续的内源性应激。通过将这种应激推过临界点,NXP800 可能迫使肿瘤细胞自我毁灭,同时对大多数健康细胞影响较小。
迫切需要新方案的顽固性骨癌
骨肉瘤通常生长在上下肢的长骨,并能快速转移到肺。标准治疗将多种强效化疗药物与手术切除肿瘤相结合。虽然这种治疗能治愈许多局限性疾病的患者,但对肿瘤复发或诊断时已发生转移的患者,治疗效果仍很差。由于现有药物已接近其疗效极限,研究者正寻找以全新方式攻击骨肉瘤的疗法,理想情况是针对那些将癌细胞与正常组织区分开的特性。
让应激对肿瘤细胞产生作用
癌细胞常处于持续压力之下。它们分裂迅速,消耗大量能量和氧气,并常经历低氧或化疗等恶劣条件。为应对这些压力,癌细胞依赖一些应急系统来帮助正确折叠和处理蛋白质并调整代谢。其中之一被称为“未折叠蛋白反应”,当细胞的蛋白质工厂——内质网过载时会被触发。另一个称为“整合应激反应”,它感知不同类型的应激并减缓蛋白质生成。通常,这些通路有助于癌细胞生存——但如果长时间被过度激活,它们可能从保护细胞转为触发细胞死亡。
NXP800 作用于关键的应激感受器
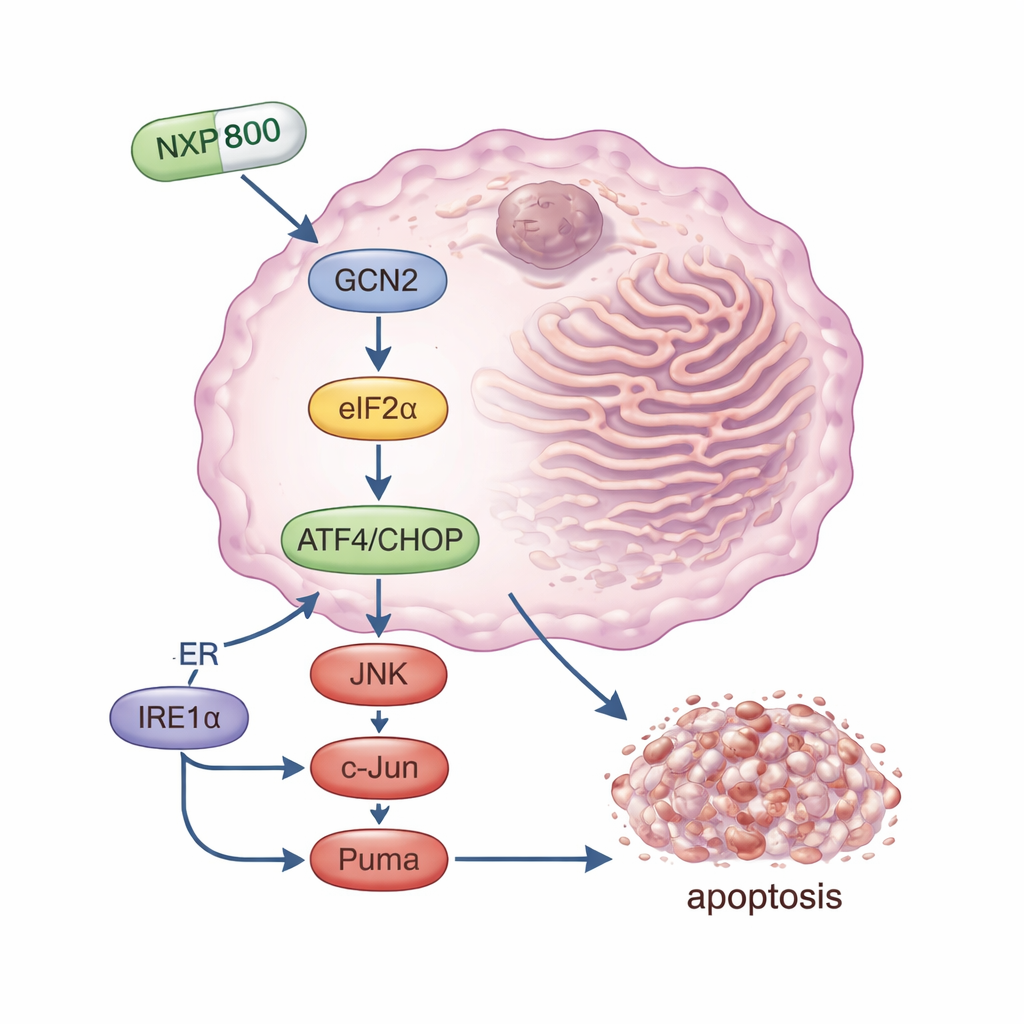
NXP800 是一种口服小分子,最初被开发用于阻断参与癌细胞生存的热休克通路。在本研究中,研究者发现它在骨肉瘤细胞中的主要作用不同:它强烈激活了一种名为 GCN2 的应激感知蛋白。GCN2 一经激活会修饰另一个因子 eIF2α,迅速降低总体蛋白质合成,同时提升特定应激“主开关”的水平,特别是名为 ATF4 的蛋白及其伙伴 CHOP。这些分子共同将细胞推向程序性死亡。研究团队表明,当通过沉默基因或使用另一种抑制剂阻断 GCN2 时,NXP800 就无法有效触发这一连锁反应,癌细胞对该药的敏感性明显降低。这一发现将 GCN2 锁定为 NXP800 在骨肉瘤中的关键靶点。
在肿瘤内部激活多条死亡通路
除了应激网络中 GCN2 这一路径之外,NXP800 还激活了另一条与细胞死亡相关的通路。它启动了名为 IRE1α 的传感器,进而刺激了信号蛋白 JNK 和 c-Jun。该分支已知可促进 Puma 的产生——一种破坏细胞内部生存机制的强效促死分子。在体外实验中,NXP800 抑制了骨肉瘤细胞的生长,使其细胞周期停滞,并激活了标志凋亡(受控细胞死亡)的酶和蛋白质改变。重要的是,正常的与骨相关的干细胞受影响较小,提示该药对已处于可耐受应激边缘的肿瘤细胞具有一定选择性。
从实验室台面到活体模型
为了检验这些细胞学效应能否转化为真实的肿瘤控制,研究者在近胫骨处移植了人源骨肉瘤细胞的小鼠模型并测试了 NXP800。口服接受 NXP800 的小鼠其肿瘤生长明显变慢,到研究结束时肿瘤体积大致仅为未处理小鼠的一半。来自经治动物的肿瘤样本显示出药物作用机制的明显特征:应激标志物 eIF2α 和 ATF4 水平升高,正在分裂的细胞减少,发生凋亡的细胞增多。单独在健康小鼠中进行的安全性试验未见主要器官损伤,肝功能检测也未恶化,支持在所用剂量下具可管理的安全性谱。
这对患者意味着什么
总体而言,这项工作表明 NXP800 能通过刻意过度激活癌细胞自身的应激防御系统直至触发自我毁灭来延缓骨肉瘤生长。通过靶向 GCN2 应激感受器及相关通路,该药提供了一种削弱已对传统化疗产生抗性的肿瘤的新途径。因为 NXP800 已在其他癌症的早期临床试验中接受测试,这些发现提出了将其重新定位用于骨肉瘤的可能性,无论是单用还是与现有药物联合使用。尽管仍需人体试验来确认疗效和安全性,但这项研究提供了有力的原理性证据,说明将细胞应激针对肿瘤可能为这种难治性骨癌的患者开启新的治疗篇章。
引用: Racineau, E., Lallier, M., Postec, A. et al. Activating GCN2 and subsequently the Unfolded Protein Response with the small oral molecule NXP800 delays tumor growth in osteosarcoma. Cell Death Discov. 12, 94 (2026). https://doi.org/10.1038/s41420-026-02941-2
关键词: 骨肉瘤, NXP800, 应激反应, GCN2 通路, 凋亡