Clear Sky Science · zh
针对代谢脆弱点:REV‑ERB 激动剂 SR9009 增强索拉非尼在肝癌中的疗效
为何切断癌细胞能量供给至关重要
肝癌是全球最致命的癌症之一,许多晚期患者仍依赖一种较早期的药物——索拉非尼。尽管索拉非尼能够减缓肿瘤生长,但癌细胞常能适应并产生耐药,从而限制患者的生存期。本研究探讨了一种通过攻击肝癌细胞能源供应来增强索拉非尼疗效的新途径,为未来能够更强力打击肿瘤而不增加严重副作用的治疗提供了方向。
现有肝癌药物的不足
索拉非尼长期以来是无法手术切除肝肿瘤患者的重要治疗手段。新的免疫疗法确实延长了部分患者的寿命,但许多人不符合这些疗法的适应证或对其无反应。对于这些患者,索拉非尼仍然很重要,然而耐药通常在数月内出现。研究人员提出了一个简单但关键的问题:肝癌细胞内部发生了哪些变化使它们逃避索拉非尼的作用,这些变化能否被转化为新的治疗弱点?
癌细胞提升它们的“发电厂”活性
为了解答,团队比较了仍对索拉非尼敏感的肝癌细胞与已经学会在药物存在下存活的耐药细胞。通过大规模 RNA 测序,他们发现耐药细胞大幅提高了与线粒体氧化磷酸化相关基因的活性——这是细胞在其微小“发电厂”线粒体中生成能量的主要方式。其他与应激防护相关的基因(包括与血红素处理相关的基因)也被上调。总体来看,这些变化表明耐药癌细胞通过重塑能量生产和应激防御,而不是简单地忽视药物的原始靶点,从而应对索拉非尼。
第二种药物切断能量供应
研究人员接着使用了 SR9009,一种最初设计为作用于调控代谢的生物钟相关蛋白 REV‑ERB 的实验性化合物。SR9009 已知能干扰线粒体功能,并对肿瘤细胞的毒性大于对正常细胞的毒性。在小鼠和人肝癌细胞中,SR9009 与索拉非尼联用相比于单用任一药物都显著降低了细胞存活率。两药联用几乎将线粒体能量产生压到极低水平,迫使细胞依赖不能完全补偿的备用糖代谢通路。体外实验显示细胞 ATP——这一普适的能量货币——大幅下降,幸存癌细胞形成的克隆显著减少。重要的是,正常成纤维细胞和非癌性肝细胞受影响要小得多,提示该策略可能具有选择性攻击肿瘤组织的潜力。
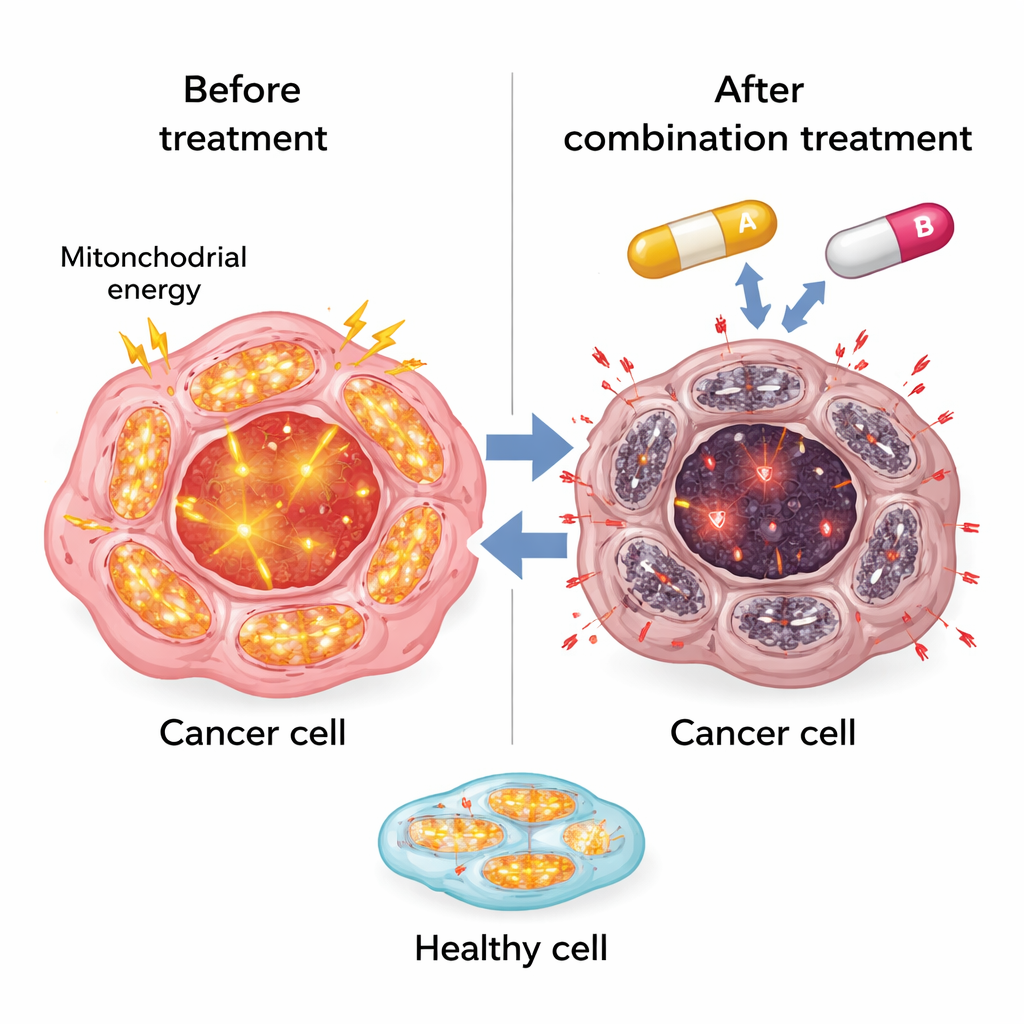
扰乱血红素平衡并引发有毒应激
研究还揭示了第二个脆弱点:耐药细胞如何管理血红素——一种含铁小分子,许多酶(包括线粒体中的酶)依赖它。耐药肝癌细胞高表达 HO‑1(一种分解游离血红素的酶),并增加细胞铁贮存蛋白铁蛋白的水平,似乎借此屏蔽血红素相关的损伤。SR9009 改变了这种平衡。在耐药细胞中,SR9009 增加了游离血红素水平并提高了氧化应激指标,如活性氧和脂质损伤,尤其是与索拉非尼联用时。同时,线粒体蛋白下降,进一步支持了这样一种观点:当细胞的能量“工厂”和应激防御被压垮时,癌细胞会被推向无法逆转的崩溃点。
动物模型中更强的肿瘤控制
为了验证这些效应是否超出细胞培养皿,团队在小鼠中测试了这对药物。在同时带有普通和索拉非尼耐药肿瘤的动物中,只有索拉非尼与 SR9009 的联用能够缩小耐药肿瘤。在另一种由致癌化学物质诱发自发发生的肝癌模型中,将 SR9009 加入减量的索拉非尼后,超过 90% 的结节出现肿瘤缩小,而单用索拉非尼的动物肿瘤大多继续生长。值得注意的是,联用并未增加总体毒性:小鼠体重稳定、血液计数正常,且当加入 SR9009 时肝损伤指标更低,提示对健康肝组织可能具有保护作用。
这对患者可能意味着什么
对于普通读者,关键信息是:这项工作勾画出一种巧妙策略,通过利用肿瘤的适应性来增强现有肝癌药物的效果。索拉非尼耐药细胞部分通过增强它们的“发电厂”和应激控制系统来生存。SR9009 砍掉了这些支持,使癌细胞能量匮乏并被有毒副产物淹没,同时较好地保留了正常细胞功能。尽管 SR9009 本身尚未获批为药物,且这些发现来自临床前模型,但这项研究提供了一条路线图:将标准抗癌药与针对肿瘤特异性代谢的药物配对,可能克服耐药并允许使用更低、更安全的剂量。长期来看,这类联合策略或能为晚期肝癌患者争取更多时间并改善生活质量。
引用: Sabbioni, S., Guerriero, P., Shankaraiah, R.C. et al. Targeting metabolic vulnerabilities: REV-ERB agonist SR9009 potentiates sorafenib efficacy in liver cancer. Cell Death Discov. 12, 86 (2026). https://doi.org/10.1038/s41420-026-02940-3
关键词: 肝癌, 药物耐药, 癌细胞代谢, 联合疗法, 线粒体