Clear Sky Science · zh
来源于BMSC的细胞外囊泡通过circRNA-0010220/β-连环蛋白通路增强骨肉瘤的增殖与转移
为什么这个骨癌故事很重要
骨肉瘤是儿童和青年成人中最常见的骨恶性肿瘤,且常转移至肺部。即使在现代化疗和手术的背景下,许多患者仍面临复发和危及生命的转移。本研究深入探查了骨肉瘤细胞与邻近骨髓干细胞之间隐秘的“对话”,发现了一种帮助肿瘤生长与扩散的微小分子信使——它可能成为新的治疗靶点。
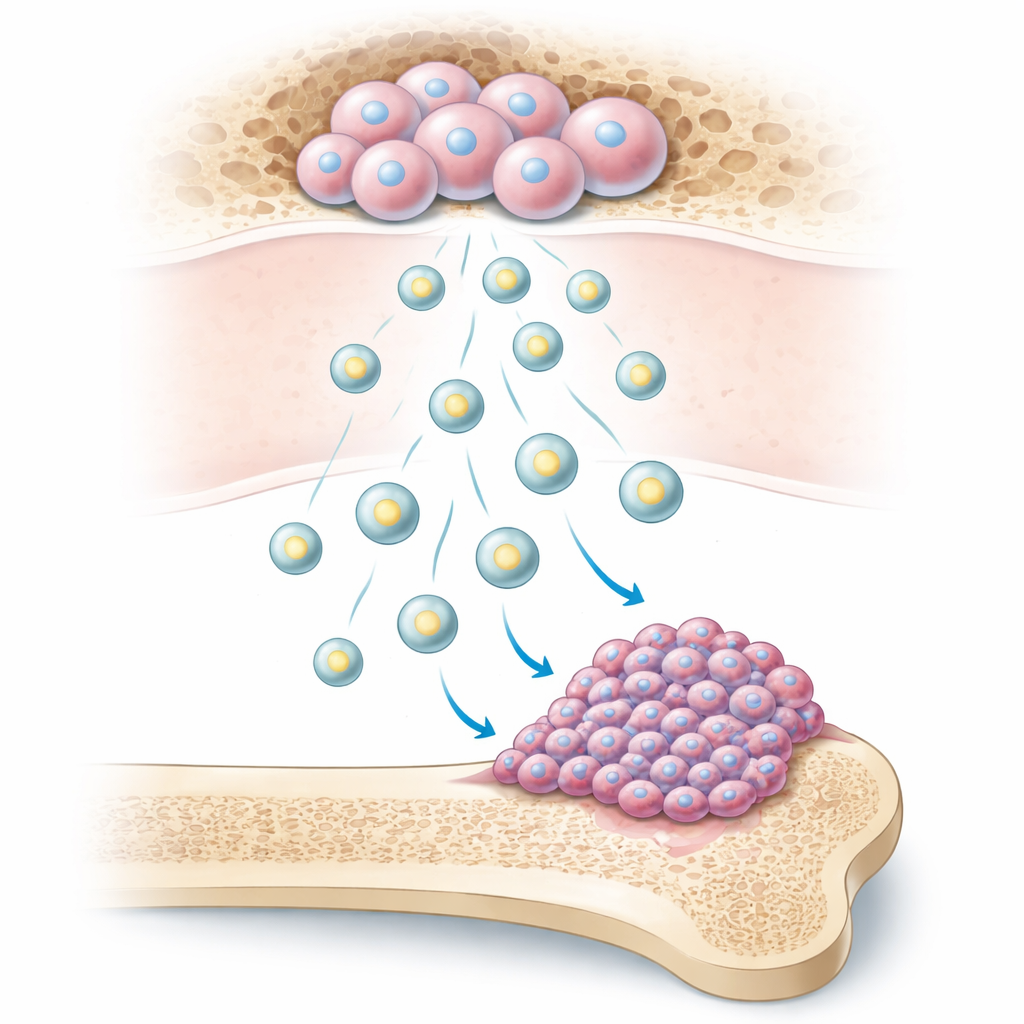
小小“包裹”,却有大影响
我们的骨骼含有骨髓间充质干细胞,这类多能细胞有助于维持与修复骨组织。这些干细胞会释放出微小的、由膜包裹的囊泡,称为细胞外囊泡。研究者表明,骨肉瘤细胞可以大量摄取这些囊泡。吸收后,癌细胞增殖更快、克隆形成更多、在表面迁移更迅速,并在体外穿透屏障的能力增强。在小鼠体内,暴露于这些囊泡的肿瘤体积更大,肺部转移也更多,这表明这些微小囊泡显著增强了肿瘤的侵袭性。
强化癌症的环状信息分子
研究团队接着检查了泌出囊泡中哪些遗传信息分子在改变骨肉瘤细胞方面影响最大。他们聚焦于环状RNA,这是一类新近发现、闭合成环并且异常稳定的RNA分子。测序结果发现一个突出候选,称为circRNA‑0010220,在用干细胞囊泡处理的骨肉瘤细胞及患者肿瘤样本中显著上调。当科学家在干细胞中降低circRNA‑0010220水平时,这些干细胞释放的囊泡在刺激癌细胞生长、迁移和侵袭方面的能力大为减弱——在体外培养和小鼠模型中均是如此。这明确指出circRNA‑0010220是造成有害效应的关键驱动因子。
一个表观遗传制动被关闭
进一步探究中,研究者描绘了该环状RNA如何重塑癌细胞行为。在骨肉瘤细胞内,circRNA‑0010220进入细胞核——细胞的控制中枢。在那里它结合了一种名为EZH2的蛋白,这是一种将化学标记加到组蛋白上的酶,组蛋白是DNA缠绕其上的卷轴样蛋白。circRNA‑0010220与EZH2协同使基因CTNNBIP1的DNA调控区上H3K27me3这一特定标记增多。这种修饰使该区域的染色质高度致密,从而有效沉默了该基因。由于CTNNBIP1通常对一个强大的促生长通路起抑制作用,其被沉默就移除了对失控癌症行为的重要制动。
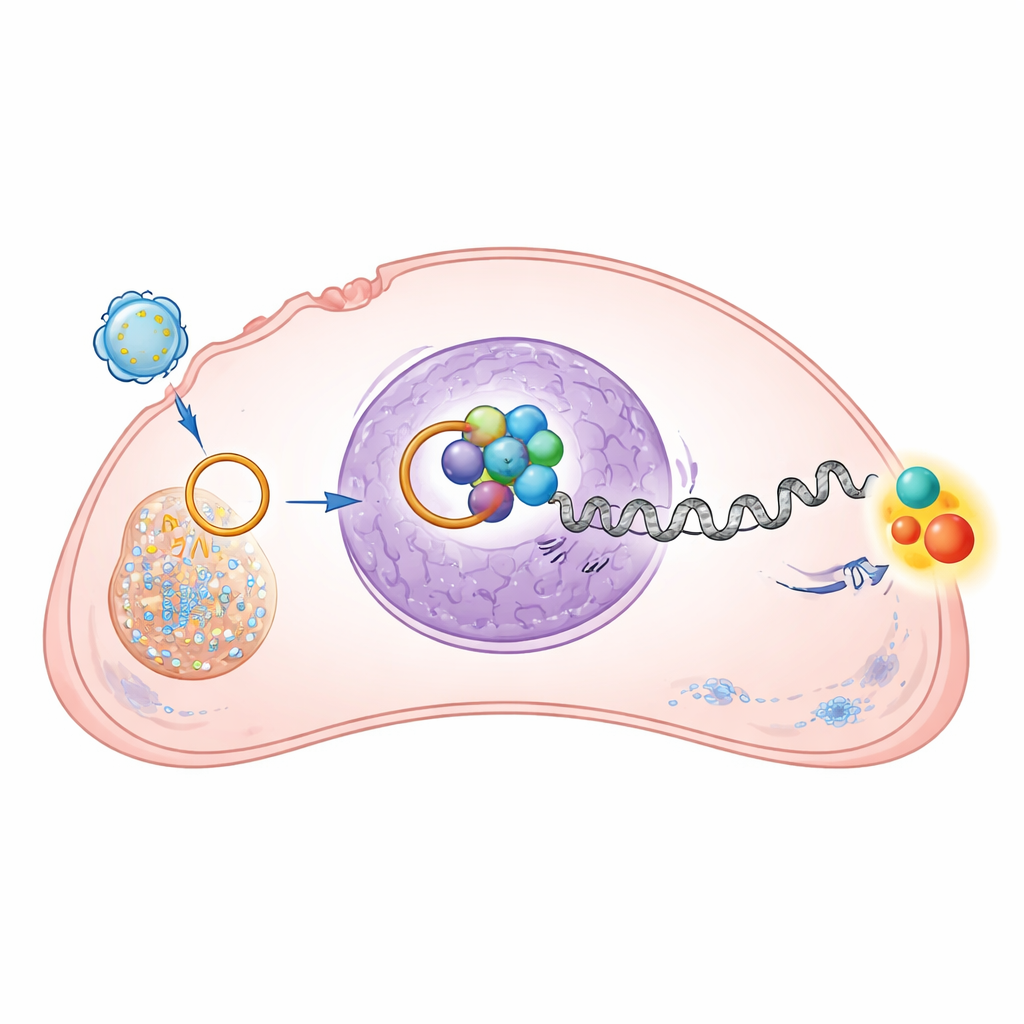
开启强劲的增殖通路
CTNNBIP1抑制Wnt/β‑连环蛋白通路——这是一条众所周知的信号系统,当其过度活跃时会促进细胞分裂、迁移与存活。通过抑制CTNNBIP1,circRNA‑0010220间接提高了骨肉瘤细胞中β‑连环蛋白的水平及其在细胞核内的活性。研究显示,该通路调控的基因——与细胞周期进程、干样特性和侵袭相关——在囊泡携带circRNA‑0010220存在时变得更为活跃。当研究者使用一种特异性抑制β‑连环蛋白的药物时,circRNA‑0010220引起的促生长和促迁移作用在很大程度上被逆转。这证实了该环状RNA通过这一增殖通路来驱动肿瘤进展。
对未来治疗的意义
总体而言,这项工作勾勒出一条完整的事件链:骨髓干细胞将富含circRNA‑0010220的囊泡传递给骨肉瘤细胞;该环状RNA在细胞核中与EZH2协作,对CTNNBIP1实施化学沉默;这解除对Wnt/β‑连环蛋白通路的抑制,最终促进更快的肿瘤生长与扩散。对患者而言,这提示了若干新的治疗切入点:阻断囊泡转运、抑制circRNA‑0010220、干扰其与EZH2的相互作用,或抑制β‑连环蛋白信号,都可能帮助减缓骨肉瘤进展。尽管这些策略需在临床中进一步验证,该研究揭示了骨肿瘤微环境中此前被忽视的对话,并强调了一组可被未来药物瞄准的具体分子目标。
引用: Pan, R., Pan, Y., Ruan, W. et al. BMSC-derived extracellular vesicles enhance osteosarcoma proliferation and metastasis via the circRNA-0010220/β-catenin pathway. Cell Death Dis 17, 376 (2026). https://doi.org/10.1038/s41419-026-08655-8
关键词: 骨肉瘤, 细胞外囊泡, 环状RNA, Wnt β-连环蛋白, 表观遗传调控