Clear Sky Science · zh
DIAPH3 丢失加速小鼠胶质瘤发生
这项脑研究为何重要
胶母细胞瘤是致死性最高的脑癌之一,即便经过手术、放疗和化疗,大多数患者的生存期也只有一年左右。本研究提出了一个基础但关键的问题:脑细胞内哪些早期变化会推动它们变成如此侵袭性的肿瘤?这些肿瘤为何对放疗难以消灭?通过追踪小鼠脑细胞中的单一结构蛋白,研究者揭示了该蛋白丢失如何导致染色体不稳定、加速肿瘤出现,并帮助具有干样特性的癌细胞耐受本应摧毁它们的放射损伤。
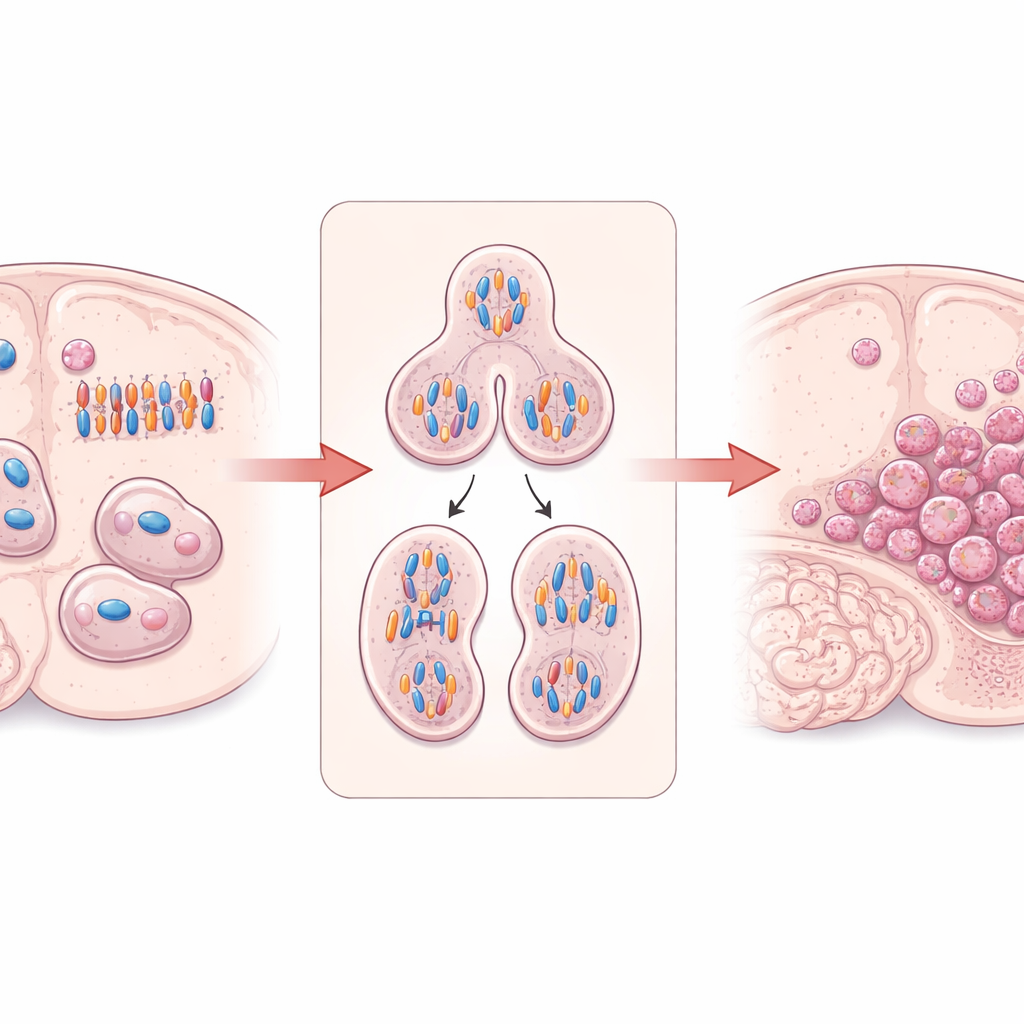
维持有序分裂的“细胞建造者”
研究聚焦于 DIAPH3,这是一种帮助构建和组织细胞内肌动蛋白丝与微管支架的蛋白。在分裂的脑干细胞中,DIAPH3 对形成正确的纺锤体——将复制后的染色体拉开的结构——以及细胞分裂的终末位点(胞质分裂)至关重要。早期研究表明,在发育中小鼠大脑中缺失 DIAPH3 时,分裂细胞常常处理染色体出错,导致异常染色体数目(非整倍体)、细胞周期停滞和细胞死亡。有意思的是,人类 13 号染色体的一小段包含 DIAPH3 基因,常在胶母细胞瘤中被缺失,而较高的 DIAPH3 水平与部分患者更好的生存率相关联,这提示该蛋白可能在大脑中发挥肿瘤抑制作用。
通过工程化小鼠大脑诱发肿瘤
为检验 DIAPH3 缺失是否真正促进脑癌,研究团队构建了可在皮层形成的干细胞中选择性删除两个基因的小鼠:Diaph3 和 Trp53(后者编码著名的基因组守护者 p53)。仅在该区域缺失 Diaph3 的小鼠即便饲养两年也未发生肿瘤,表明 p53 仍能消除高度异常的细胞。相比之下,仅缺失 Trp53 或同时缺失 Trp53 与 Diaph3 的小鼠最终都形成了在显微镜下与人类疾病高度相似的高级别弥漫性胶质瘤。通过反复的超高场 MRI 扫描,研究者发现同时缺失两基因的动物更早出现可检测到的肿瘤,并且到中年期比仅缺失 Trp53 的小鼠更常见到大型胶质瘤,尤其位于嗅球。肿瘤一旦开始生长,其生长速率在各组间相似——变化的是肿瘤出现的时间早晚。
染色体混乱与基因活动重编程
为探究 DIAPH3 缺失为何加速肿瘤发生,团队在肿瘤可见之前对年轻小鼠嗅球的基因表达进行分析。在同时缺失 Diaph3 与 Trp53 的动物中,与仅缺失 Trp53 的突变体相比,有 126 个基因的表达水平发生改变,其中近一半与癌症已有关联。许多改变集中在驱动细胞生长、迁移和血管生成的通路上,包括 VEGF、MAPK、RAS、Rap1 和 cAMP 信号传导,以及 G 蛋白偶联受体网络。这一改变的分子景观表明细胞更早被推向类似癌症的状态。对完全形成肿瘤的全基因组拷贝数分析显示,DIAPH3 缺失并未显著增加小的局灶性 DNA 变动,而是促进了整染色体的大幅获失——正是染色体分离错误所导致的非整倍体表现。
内在 DNA 损伤与更强健的肿瘤干细胞
非整倍体肿瘤细胞携带更多的内在 DNA 损伤,可由核内分布增多的 DNA 断裂标志物 γ‑H2AX 检测到。然而这些肿瘤仍能生长,说明它们已获得耐受此类压力的机制。在既成肿瘤中比较基因表达,研究者发现数百个因 DIAPH3 缺失而改变的基因,包括许多双敲除肿瘤中显著扩增并过度表达的生长因子受体 FGFR2。FGFR2 已知可增强胶质母细胞瘤细胞的 DNA 修复能力,其激活与放疗抗性相关。团队从小鼠肿瘤中分离出胶质瘤干样细胞并测试其对临床相关剂量电离辐射的反应。治疗前,两种基因型的干样细胞频率相似,但照射后,来自 DIAPH3 缺失肿瘤的培养物大约保留了两倍于仅缺失 Trp53 肿瘤的活性干样细胞,显示出更强的放射耐受性。
这对脑癌意味着什么
综上,该研究将 DIAPH3 描绘为帮助脑干细胞以正确染色体数目分裂的守护因子。当 DIAPH3 与 p53 同时缺失时,细胞分裂变得容易出错,整染色体被丢失或获得,DNA 损伤累积。一些细胞并未死亡,而是通过扩增与修复相关的因子(如 FGFR2)来适应,转变为非整倍体的高级别胶质瘤,其干样细胞对放疗异常耐受。尽管小鼠模型无法完全复刻人类胶母细胞瘤的所有特征,这些发现仍支持将 DIAPH3 视为潜在的预后生物标志物以及控制肿瘤起始、基因组稳定性和治疗反应过程网络中的一环——为未来可能让这种毁灭性脑癌对现有治疗更敏感的疗法打开了新途径。
引用: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
关键词: 胶母细胞瘤, 染色体不稳定性, 脑肿瘤干细胞, 放射抗性, 肿瘤抑制基因