Clear Sky Science · zh
在放化疗诱导细胞死亡后幸存的多形性胶质母细胞瘤细胞表现出分叉的糖酵解程序
这项脑癌研究的重要性
多形性胶质母细胞瘤是成人中最致命的脑癌之一,几乎在手术、化疗和放疗后都会复发。本研究提出了一个关键问题:在治疗后幸存并在随后重新点燃疾病的那小部分肿瘤细胞,有何不同?通过跟踪这些细胞随时间处理糖的方式,研究人员揭示了一种隐藏的生存策略,这可能解释了目前治疗为何常常失效——并提示切断肿瘤“生命线”的新途径。
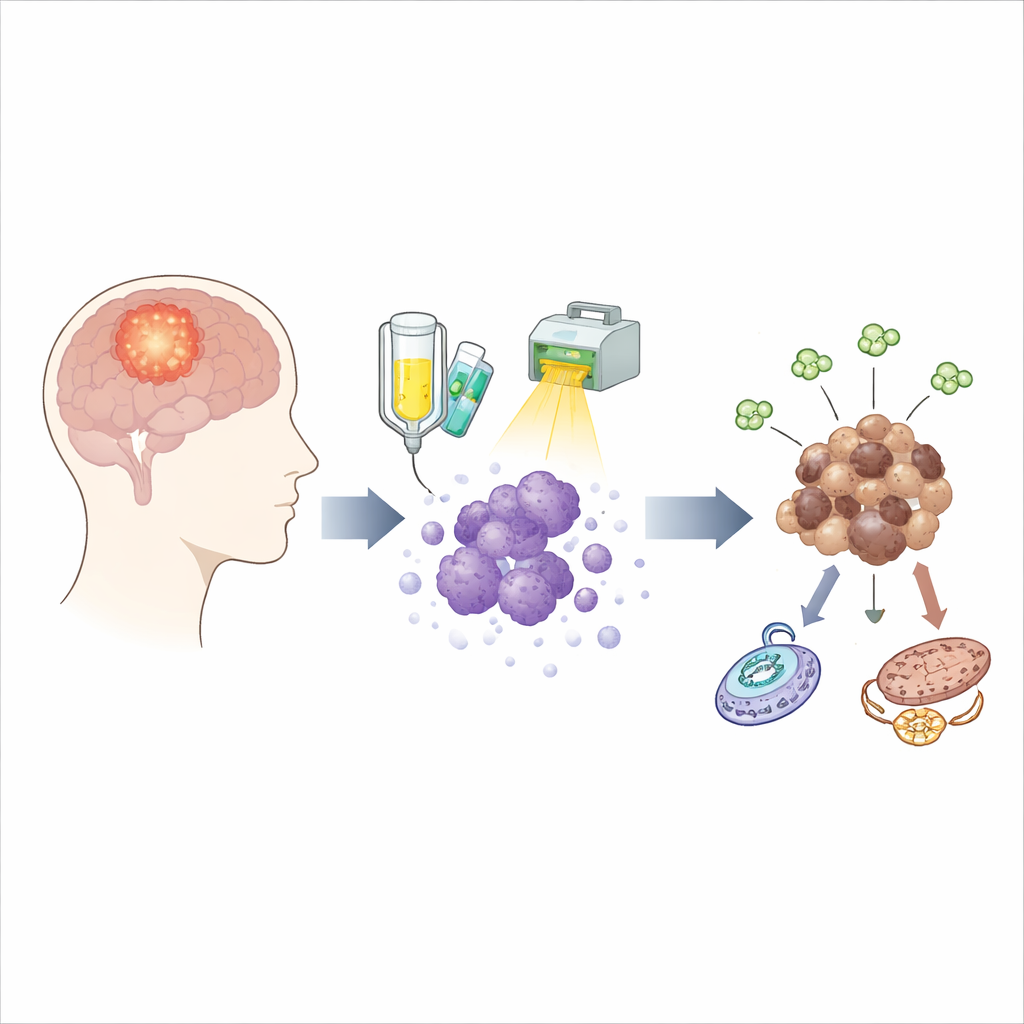
治疗后隐藏的幸存者
多形性胶质母细胞瘤的标准治疗将一种叫替莫唑胺的药物与放疗结合使用。尽管这种组合能杀死大多数肿瘤细胞,但一小部分顽固的细胞仍然存活,几个月后可能播下新肿瘤的种子。为了捕捉这些幸存者的动态,研究团队使用来自十位不同患者的肿瘤细胞,并按接近临床的方案暴露于治疗之下。他们在治疗期间和治疗后多个时间点采样活细胞,并研究了配对的在小鼠体内生长的肿瘤,使他们能够跟踪幸存细胞随时间的变化,而不仅仅是比较复发前后的肿瘤。
肿瘤细胞如何改变其糖代谢方式
大脑组织消耗了机体相当大比例的糖,而多形性胶质母细胞瘤细胞对糖尤其“贪吃”。研究人员发现,随着治疗推进,幸存细胞从周围环境中摄取了更多葡萄糖。然而,巧的是,它们并没有简单地更快地燃烧这些额外的燃料。相反,这些细胞减少了乳酸的产生——乳酸是癌细胞快速糖分解的典型废产物。对关键蛋白的测量显示了明显的分叉模式:负责将糖带入细胞并启动分解的组分上调,而负责后续步骤并生成乳酸的组分下调。这种“分叉”程序意味着糖进入并开始被处理,但通往乳酸的常规出口部分关闭。
将燃料改道用于构建材料和能量工厂
这些被改道的糖去哪儿了?通过使用特殊标记的葡萄糖和先进的代谢物测量,团队显示幸存细胞将大量碳流入两个主要去向。其一是一个旁路——戊糖磷酸途径,它生成构建 DNA 与 RNA 所需的原料。在这些细胞中,许多核苷酸成分及相关基因被增强,表明细胞强烈推动修复与为重新生长做准备。第二个去向是细胞的能量工厂——线粒体。线粒体能量循环的酶增加,且该团队早期工作显示来自糖的燃料更多被输送到这些结构。合在一起,这揭示出一种协调重接线:降低向乳酸的浪费性发酵,增加用于修复、制造生长材料和灵活能量生产的投入。
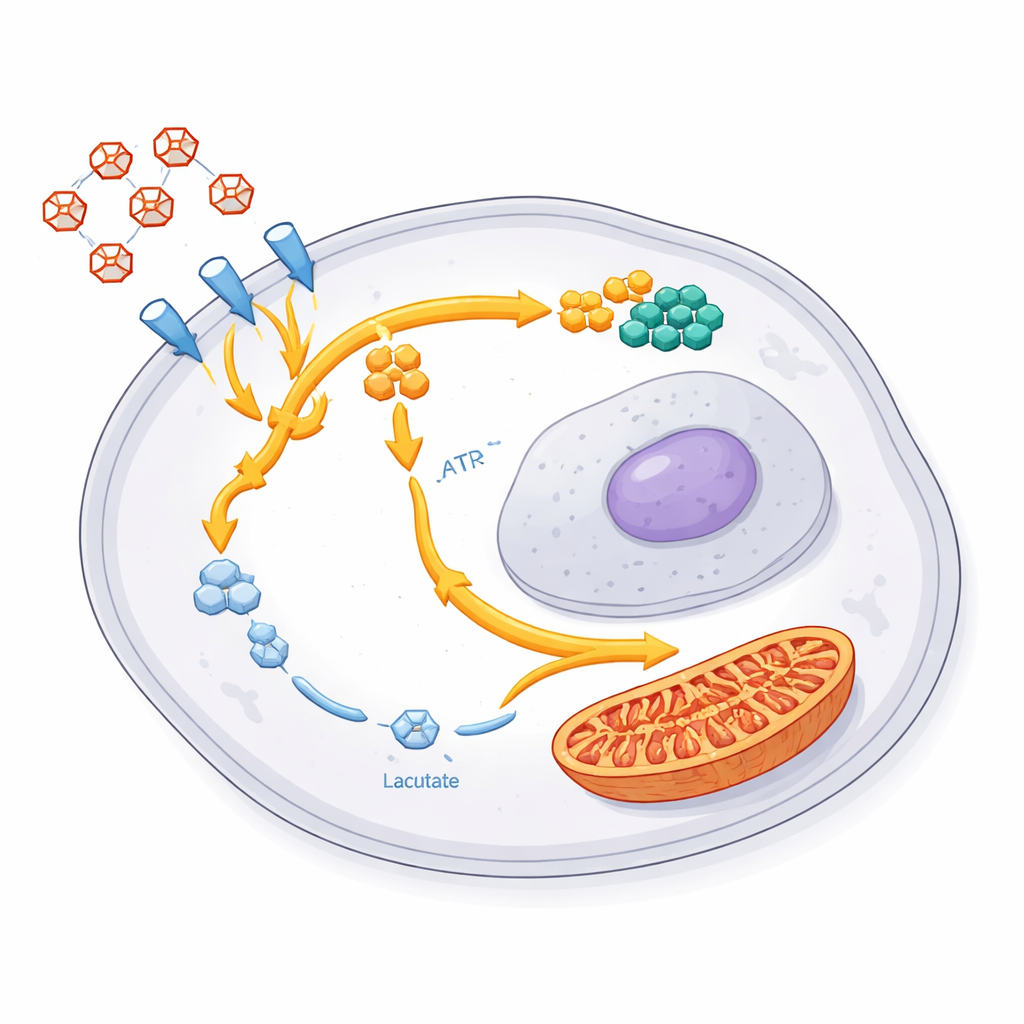
在肿瘤样本与动物模型中共享的生存策略
多形性胶质母细胞瘤在不同患者之间差异很大,这常常使一刀切的治疗方案失效。尽管存在这种多样性,来自十位患者的每一个模型在放化疗后都表现出相同的基本转变:糖代谢早期步骤增加、后期步骤和乳酸输出下降、线粒体活性提高。重要的是,相同的代谢特征也出现在经改良标准疗法处理的患者来源小鼠脑肿瘤中。动物中的复发肿瘤仍保有这种改变的糖代谢程序,表明这不是短暂效应,而是能够逃过治疗并重建肿瘤的细胞的稳定特征。
这对未来治疗的意义
对非专业读者而言,核心信息是:幸存的多形性胶质母细胞瘤细胞并非仅仅“躲避”治疗;它们主动重编程对糖的使用以维持生命。它们摄入更多葡萄糖,避免将其变为废物,而是将其引导用于合成 DNA 的原料和供给线粒体能量——帮助它们修复损伤、维持灵活的干样状态并最终重新生长肿瘤。通过揭示这种共同的代谢生存状态,研究为新的治疗策略提供了方向:针对糖代谢的早期步骤、核酸合成的旁路或这些细胞对线粒体的依赖,可能使标准的放化疗更彻底,减少那些逃脱者重新启动疾病的机会。
引用: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
关键词: 多形性胶质母细胞瘤, 癌症代谢, 葡萄糖利用, 治疗耐受性, 戊糖磷酸途径