Clear Sky Science · zh
由GGCT驱动的代谢协同:将谷氨酰胺转向谷胱甘肽生物合成,同时增强葡萄糖补给以促进肿瘤增殖
这对癌症治疗为何重要
癌细胞生长迅速,为此它们消耗大量燃料,并必须不断保护自己免受自身代谢产生的有毒副产物的伤害。本研究揭示了一种鲜为人知的酶GGCT,如何帮助肝癌和前列腺肿瘤巧妙地重新分配两种常见营养物——谷氨酰胺和葡萄糖,使它们既能为生长提供能量,又能控制称为活性氧的损伤分子。理解这种代谢上的杂耍可能为阻断肿瘤营养或压倒其防御机制开辟新途径。
肿瘤细胞如何在燃料与防护间权衡
肿瘤细胞高度依赖谷氨酰胺,这种氨基酸具有双重作用:它可被分解以供细胞的主要能量循环使用,同时也提供合成强效抗氧化剂谷胱甘肽的构件,用以中和活性氧。作者首先证实,肝肿瘤中的谷氨酰胺水平高于邻近的健康组织,并且在培养皿和小鼠体内,补充更多谷氨酰胺会使癌细胞分裂更快。当谷氨酰胺不足时,细胞生长放缓,关键细胞周期蛋白下降,动物体内肿瘤缩小——部分原因是抗氧化防御减弱、活性氧堆积。
隐藏在明处的代谢开关
通过分析患者样本和大型癌症数据库,团队发现GGCT在肝癌和前列腺肿瘤中持续高表达,且较高的GGCT水平预示着更差的预后。在肿瘤样本和培养细胞中,GGCT水平随着谷氨酰胺浓度同步上升,提示肿瘤可能通过该蛋白“读取”谷氨酰胺可用性。研究者理清出一条调控链:谷氨酰胺维持促增长因子c-Myc的活性,c-Myc抑制一种小型调控RNA miR-29b-3p;当miR-29b-3p水平低时,GGCT不受抑制而积累。在谷氨酰胺短缺时,这条链条反转,miR-29b-3p上升,GGCT的转录信息被更快降解,酶水平下降。
将谷氨酰胺重定向并吸引更多葡萄糖
为探明GGCT在细胞内的实际作用,作者降低或提升其表达,并测量细胞行为及数百种代谢物。沉默GGCT使细胞在分裂周期停滞,克隆体缩小,并显著降低谷胱甘肽同时增加活性氧;添加化学抗氧化剂可部分挽救生长。在显微镜下,线粒体变得异常延长且耗氧效率下降,即便细胞试图通过增强糖酵解(一号葡萄糖分解步骤)来补偿。详细的代谢谱分析显示,丧失GGCT时中央能量循环的中间体下降,而过表达时这些中间体上升。
追踪碳原子的去向
团队随后追踪带标记的谷氨酰胺和葡萄糖原子在肿瘤代谢中的流向。过表达GGCT时,更多标记谷氨酰胺不进入能量循环,而是被导入新合成的谷胱甘肽,支持抗氧化防御。与此同时,标记葡萄糖对能量循环的贡献增加,以补偿被转向的谷氨酰胺。缺乏正常酶活性的GGCT突变体无法驱动这些转变或促进增殖,表明GGCT的催化功能至关重要。重要的是,补充额外丙酮酸或调整进入能量循环的途径能恢复细胞能量水平,但不能降低活性氧,这表明GGCT主要通过调控谷胱甘肽维持氧化还原平衡,而非仅通过改变能量供应。
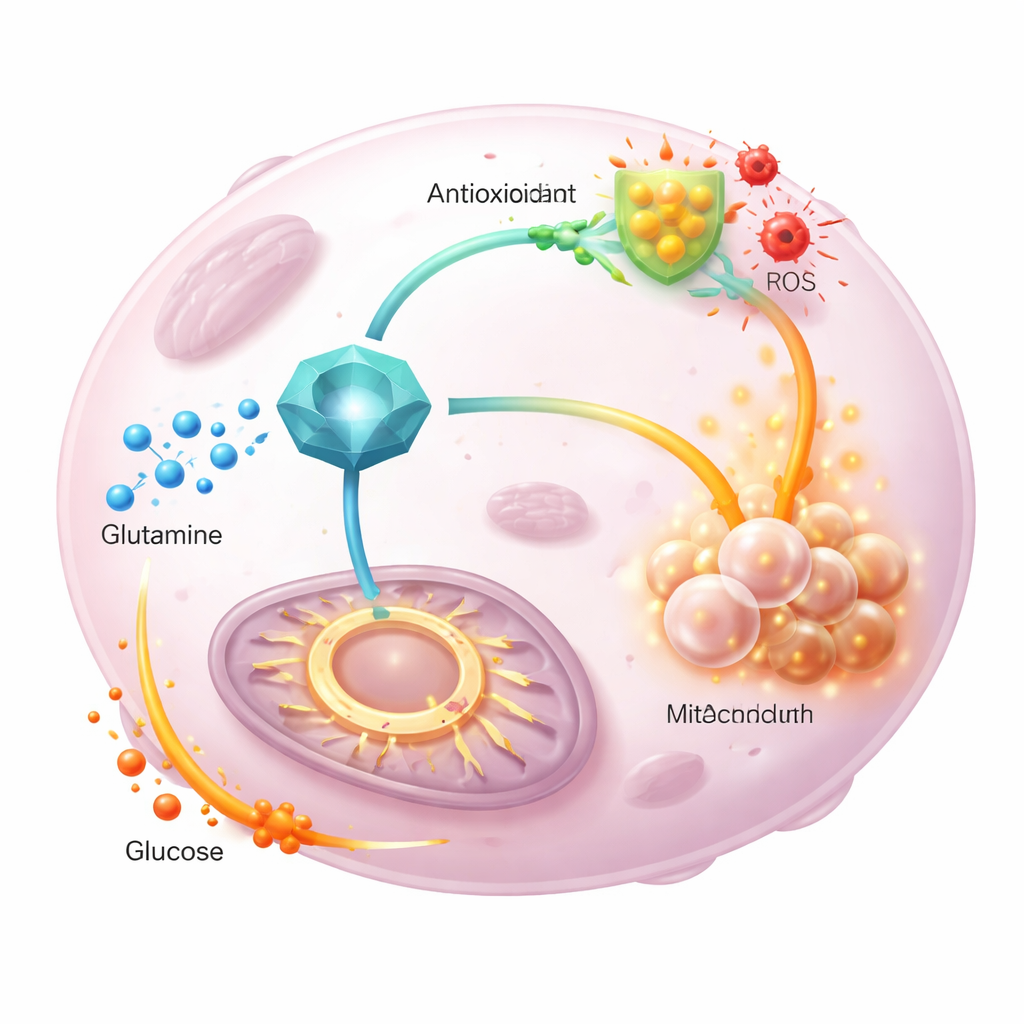
对未来疗法的意义
总体而言,这些发现将GGCT定位为一个核心协调者,使肿瘤能够分配谷氨酰胺的双重职责:将更多谷氨酰胺引向抗氧化产物的合成,同时将葡萄糖拉入能量循环以维持细胞分裂。在动物模型中,敲低GGCT减慢肿瘤生长、降低谷胱甘肽并增加氧化应激,这些效应可被抗氧化药部分逆转。对于普通读者而言,结论是某些癌症通过将GGCT作为代谢开关来生存;使该开关失效的药物可能同时削弱肿瘤对氧化损伤的防御并扰乱其灵活利用营养的能力,从而使标准治疗更有效。
引用: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
关键词: 癌症代谢, 谷氨酰胺, 谷胱甘肽, 氧化应激, GGCT酶