Clear Sky Science · zh
脂肪生成性易位重编程将高EMT胰腺导管腺癌细胞转变为停分裂的类脂肪细胞状态并限制转移
将侵袭性癌细胞变成无害脂肪
胰腺癌是最致命的癌症之一,很大程度上因为它早期扩散且对常规治疗耐受性强。本研究探讨了一个截然不同的思路:与其尝试毒杀或饥饿肿瘤细胞,不如设法诱导最危险的胰腺癌细胞转变为不再分裂或迁移的类脂肪细胞?该工作描述了研究人员如何将高度侵袭性的胰腺癌细胞推进到一种稳定的、类似脂肪细胞的状态,从而在小鼠中减慢肿瘤生长并减少转移,提示了一种控制这种毁灭性疾病的新途径。
为何胰腺癌如此难以阻止
胰腺导管腺癌是胰腺癌的主要类型,预后极差:诊断后五年生存率仅约八分之一。问题的一部分在于,该癌症中许多肿瘤细胞处于一种称为上皮-间质转化(EMT)的可变形态状态,使它们更具迁移性、侵袭性并对药物更具抵抗力。尝试阻断驱动这一状态的众多信号所带来的收益有限。与此同时,胰腺及其肿瘤呈现出出人意料的倾向——积累脂肪细胞,这引发了一个问题:是否可以利用这种隐藏的细胞身份可塑性。作者的推理是,如果富含EMT的胰腺癌细胞已经处于易于变化的准备状态,也许可以将它们重新引导为一种安静的、类脂肪的身份,而不是侵袭性的身份。
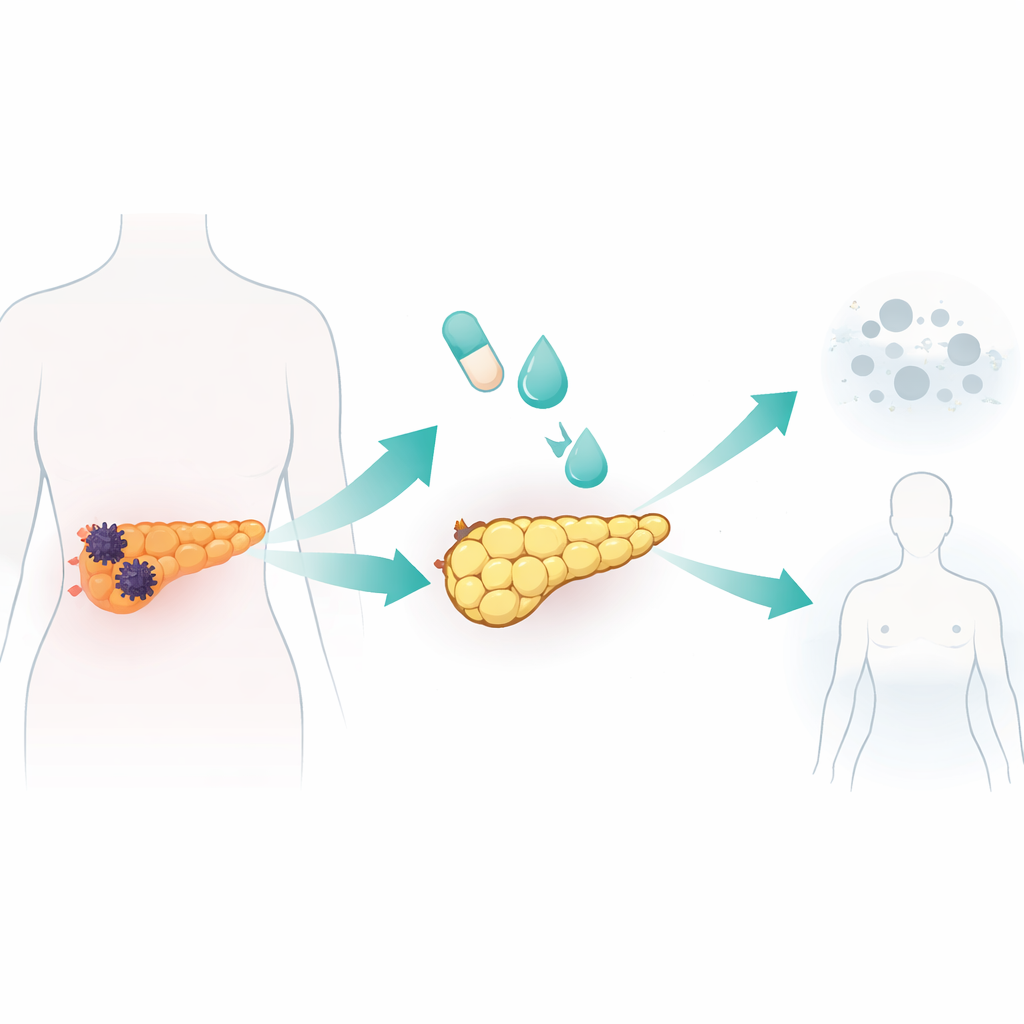
在实验室中将癌细胞重编程为类脂肪细胞
研究团队在七条人类胰腺癌细胞系和一条正常胰腺细胞系上测试了一种标准的脂肪细胞形成组合物,此组合物在早期脂肪生物学和乳腺癌研究中已有使用。该混合物结合了胰岛素和类固醇与罗格列酮(一种激活脂肪生物学主调控因子的药物),外加一种称为BMP2的信号蛋白以解锁细胞可塑性。其中一条癌细胞系AsPC-1对处理尤其敏感。在十天内,这些细胞变得更大、更圆,并充满脂滴,这是脂肪细胞的典型特征。它们启动了成熟脂肪细胞典型的基因和蛋白表达,并显示出强劲的脂质代谢,包括分泌脂联素和在刺激下分解储存脂肪。至关重要的是,这些被转化的细胞停止增殖,在细胞周期早期停滞,且迁移与侵袭能力远低于未处理的癌细胞。
在细胞深层关闭癌症程序
为了了解分子层面的变化,研究人员分析了转化细胞的染色质构型和基因活动。他们发现染色质普遍收紧、基因表达整体下降,这些都是非分裂细胞的特征。支持EMT、侵袭和转移的基因,包括基质降解酶和关键EMT调控因子,均被强烈抑制,而与脂肪相关的基因则被上调。总体基因特征从间质型、高度迁移性身份转向与成熟脂肪细胞密切相似的表型。与细胞生长和对主要EMT驱动因子TGF-β的反应相关的信号被削弱,而与脂质处理和细胞黏附相关的路径被增强。这些变化表明细胞不仅仅是减速,而是从根本上重新指定了身份。
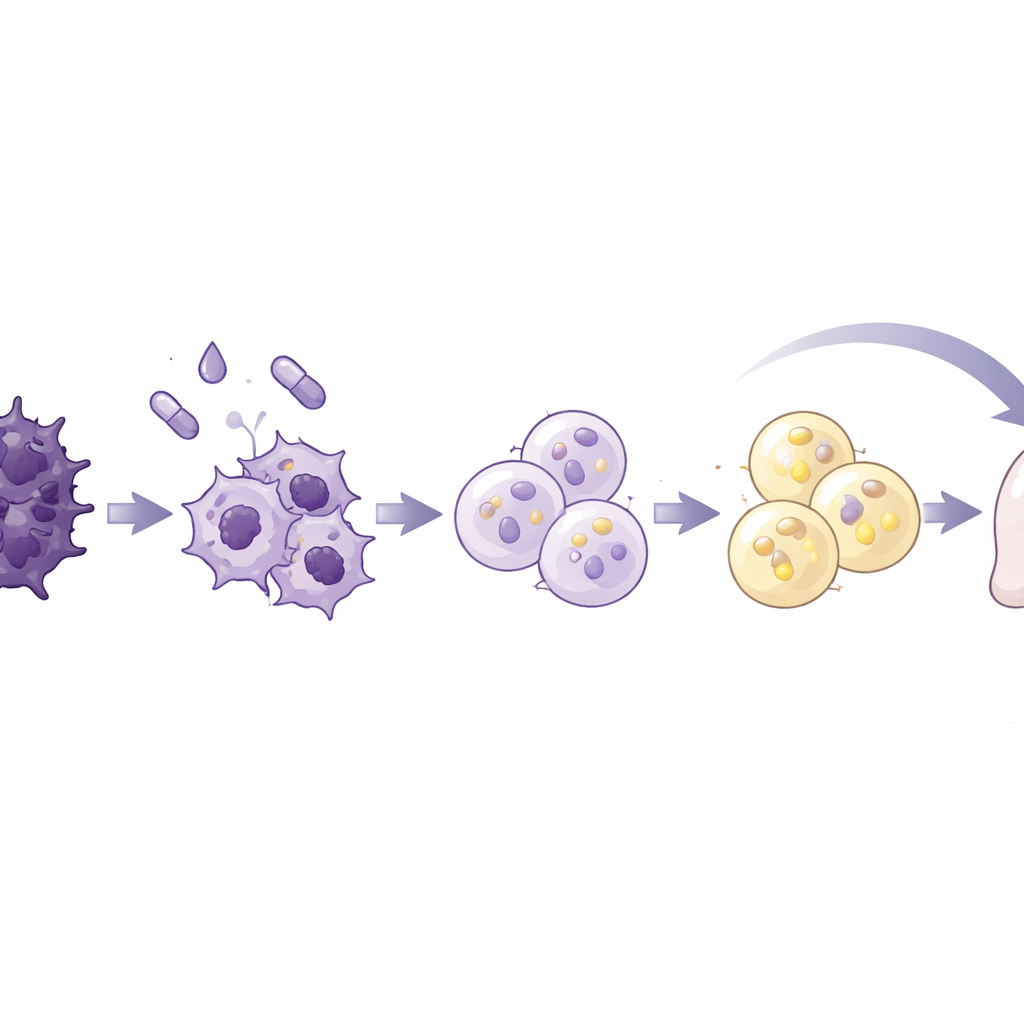
在小鼠体内检验该策略
接着,科学家们询问这种强制性的类脂肪转化是否能在活体动物中帮助控制肿瘤。研究者将人类胰腺癌细胞植入小鼠的胰腺或脾脏,以模拟原发肿瘤和肝转移。接受罗格列酮和BMP2处理的小鼠胰腺肿瘤更小,肿瘤内脂滴更丰富、脂肪细胞标志物更强,同时EMT和侵袭相关基因水平较低。在转移模型中,治疗并未改变早期肿瘤播种,但随着时间推移,与未处理动物相比,肝脏肿瘤负担扩张被延缓。重要的是,邻近的正常胰腺组织没有明显的脂肪细胞转化,且肿瘤中的类脂肪状态在停药后至少持续了一个月,提示具有一定的持久性和特异性。
这对未来癌症护理意味着什么
这项研究支持了一个颇具挑衅性的概念:对于高度可塑、富含EMT的胰腺癌,或许可以“转化而非杀灭”,将危险、游走的肿瘤细胞重定向为稳定的、非分裂的类脂肪细胞,从而降低其扩散能力。尽管这是处于细胞和小鼠模型的早期研究,且并非所有胰腺癌对该方法同样敏感,但它开辟了一条通过改变细胞身份而非单纯阻断生长信号的新治疗途径。未来,此类易位分化策略可能与靶向药物或免疫疗法结合,以将胰腺癌维持在更安静、更可控的状态,降低致命转移的风险。
引用: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
关键词: 胰腺癌, 细胞可塑性, 易位分化, 上皮-间质转化, 类脂肪细胞