Clear Sky Science · zh
上皮性卵巢癌腹膜网膜转移对精氨酸的依赖揭示了治疗弱点
这对女性健康为何重要
上皮性卵巢癌是影响女性的致死性癌症之一,原因在于它通常在悄无声息地扩散到腹腔之后才被发现。这些游走的癌细胞常常落脚于一块覆盖在肠道上的富脂组织,称为网膜。本研究揭示了网膜转移灶的一个隐性弱点:它们异常依赖于膳食氨基酸精氨酸。通过追踪转移细胞如何利用精氨酸来修复损伤的DNA并抵御压力,研究者提出了可能通过限制精氨酸或阻断其通路来饿死转移灶或切断其逃生路径的新治疗策略。
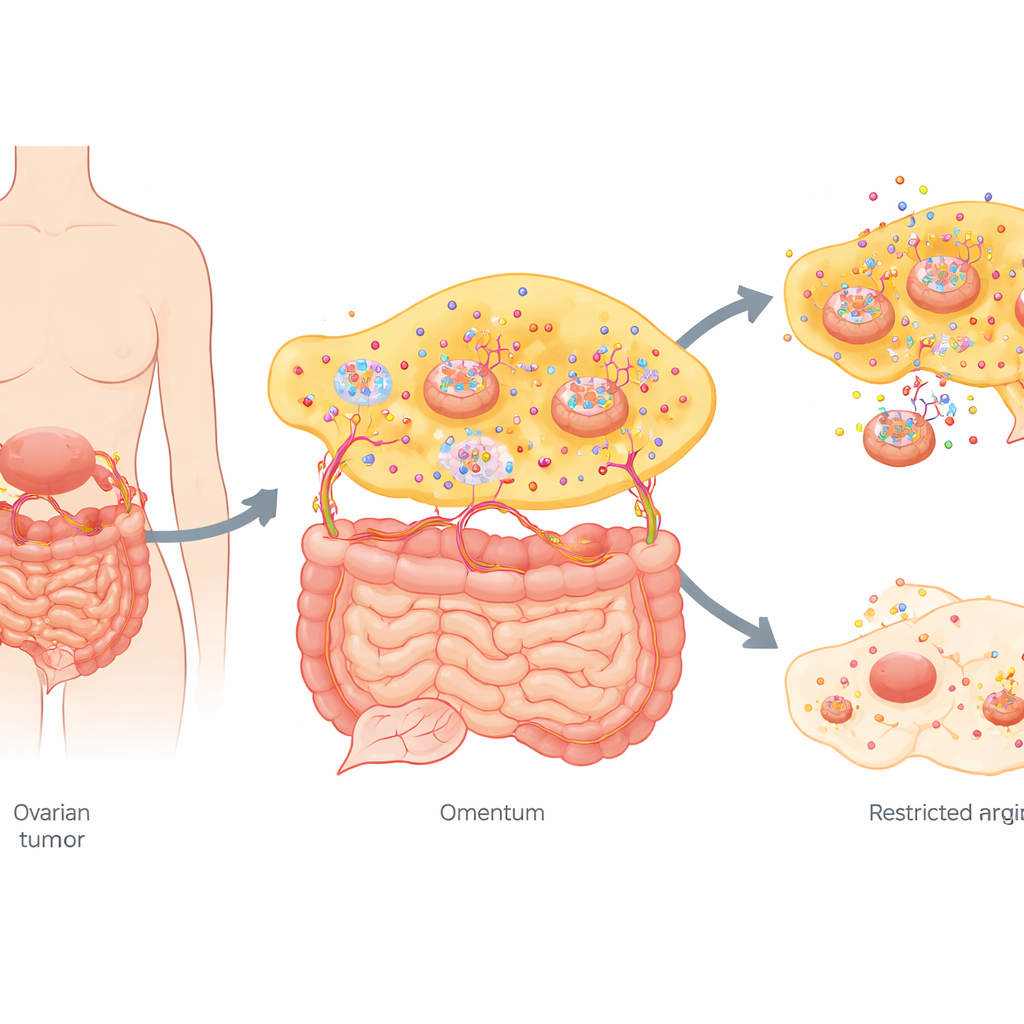
在特殊生态位中对养分饥渴的癌症
晚期卵巢肿瘤常在腹腔内播撒微小病灶,尤其是在富含脂肪的网膜上。研究团队比较了来自尚未接受治疗女性的原发卵巢肿瘤与配对的网膜转移灶。对数百种小分子的广泛检测显示,转移灶的代谢“指纹”与原发肿瘤显著不同。在多种变化中,最突出的是:网膜转移灶积累的精氨酸远高于原发肿瘤。与此同时,细胞内合成精氨酸所需的酶表达下调,而用于外源精氨酸摄取的转运蛋白表达上调,表明转移细胞已变得依赖来自外部环境的精氨酸。
通过切断精氨酸供应来饿死肿瘤
为检验这种对精氨酸的依赖是否具有实际意义,研究者使用了卵巢癌小鼠模型。当带瘤小鼠被置于无精氨酸饮食时,既有原发卵巢肿瘤又有弥漫性腹部转移灶均明显缩小。成像显示肿瘤信号减弱、转移灶数量和大小减少、腹腔积液减少,并且与正常饮食组相比存活期更长。在体外培养中,缺乏精氨酸时人类卵巢癌细胞增殖变慢、迁移和侵袭能力下降。将精氨酸浓度提高到与患者转移灶中相当或更高的水平则相反,促进细胞生长和迁移。过表达精氨酸转运蛋白进一步增强了这些侵袭性行为,强调了肿瘤在精氨酸充足时的生长优势。
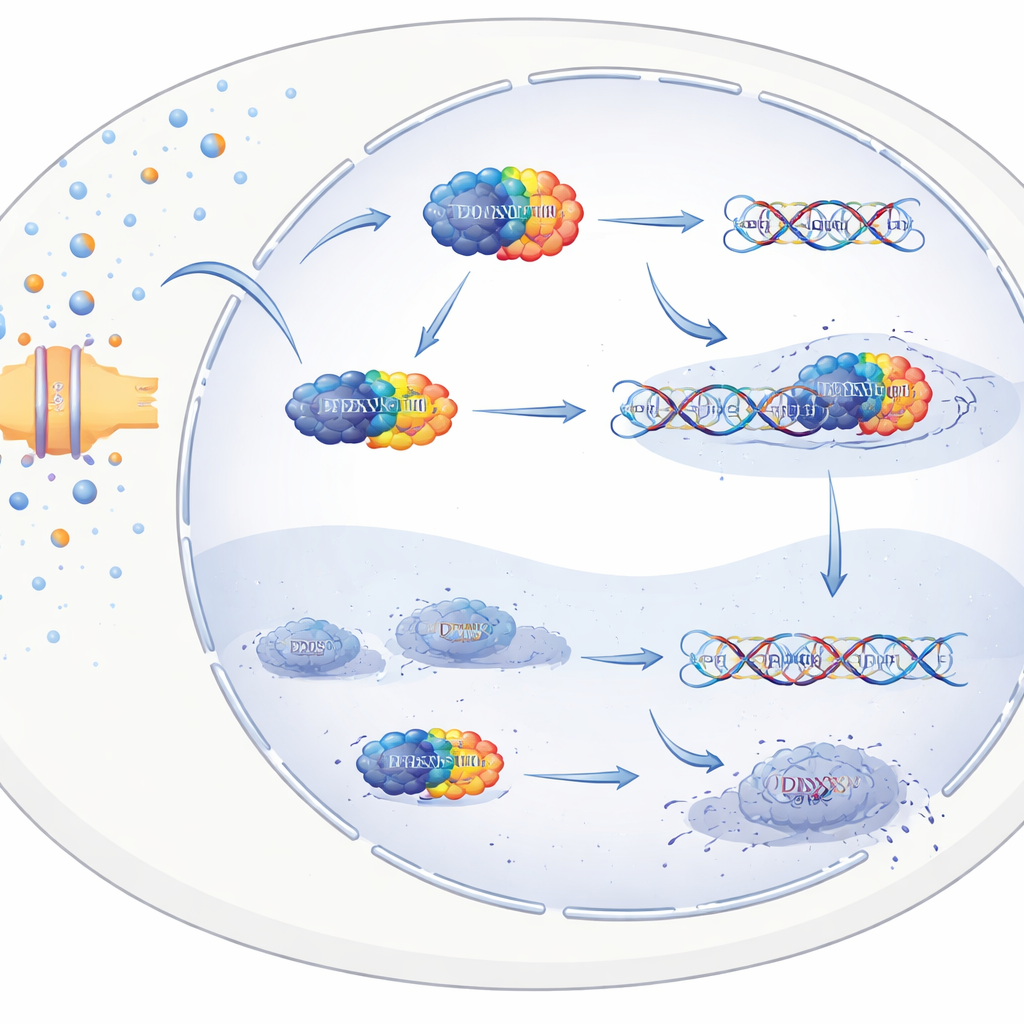
精氨酸如何帮助癌细胞修复DNA
接下来科学家们探究了精氨酸在分子层面如何支持转移。研究者用化学“诱饵”捕获与精氨酸直接结合的蛋白,鉴定出许多与RNA处理相关的蛋白,并聚焦于一种名为DDX3X的蛋白。这种蛋白在转移灶中含量高于原发肿瘤,且与患者预后较差相关。体外实验和计算模拟表明,精氨酸能停靠在DDX3X的特定区域并改变其细胞内定位。在高精氨酸环境下,精氨酸干扰了将DDX3X导出到细胞质的信号,使其在细胞核内积累。一旦进入细胞核,DDX3X与DNA结合并增强参与DNA损伤反应通路的基因活性,特别是感知DNA断裂并协调修复的ATM–CHK2–p53轴。
在危险环境中生存
网膜中的转移细胞面对强烈的氧化应激,并显示出比原发肿瘤更多的DNA损伤,这本应威胁它们的存活。研究发现富含精氨酸的转移灶同时具有更高水平的DNA修复活性标志物。当向暴露于化疗或氧化应激的细胞补充精氨酸时,DNA断裂被更有效修复,死亡细胞减少。去除DDX3X或阻断其下游的ATM或CHK2蛋白会抹去这种保护效应。换言之,精氨酸使转移性卵巢癌细胞能够感知其营养环境,并通过DDX3X启动强大的DNA修复程序,帮助它们在敌对的网膜生态位以及抗癌治疗中存活。
将营养渴求转化为治疗机会
鉴于患者长期限制精氨酸可能存在困难,作者也探索了基于药物的策略。在小鼠中,用酶降解血液中的精氨酸或直接用小分子抑制DDX3X均能放慢肿瘤生长、减少转移并延长存活期。将精氨酸耗竭与DDX3X抑制联合使用效果更佳,阻断DDX3X还可使顺铂耐药的卵巢癌细胞对化疗重新敏感,在小鼠中缩小耐药肿瘤。总体而言,这些结果表明卵巢癌的网膜转移灶在代谢上对外源精氨酸上瘾,并通过DDX3X将其用于维持DNA修复和生存。针对这一精氨酸–DDX3X–DNA 修复回路,无论是限制精氨酸供应还是抑制DDX3X,都可能为预防或治疗转移性卵巢癌并克服药物耐受性开辟新途径。
引用: Tian, J., Lei, T., Du, Y. et al. Arginine dependency in omental metastasis of epithelial ovarian cancer reveals a therapeutic vulnerability. Cell Death Dis 17, 354 (2026). https://doi.org/10.1038/s41419-026-08606-3
关键词: 卵巢癌, 精氨酸代谢, 癌症转移, DNA 损伤修复, DDX3X