Clear Sky Science · zh
CBX2 相分离助力同源重组修复并导致卵巢癌耐药
这项研究为何重要
卵巢癌是女性中致死率最高的癌症之一,很大程度上因为许多肿瘤对化疗失去反应。该研究揭示了高级别浆液性卵巢癌使用的一种隐藏生存策略:它们在细胞核内构建微小的类液滴,能够加强 DNA 修复,帮助肿瘤细胞抵御常规药物造成的损伤。研究还指出已有的一种口服药物伊布替尼,可能成为针对依赖这种基于液滴修复系统的肿瘤的治疗手段。
修复 DNA 过于“出色”的肿瘤细胞
大多数强效抗癌药通过严重破坏 DNA 使肿瘤细胞无法分裂而发挥作用。然而在高级别浆液性卵巢癌中,许多肿瘤变得擅长修补这些损伤,从而对铂类化疗和 PARP 抑制剂产生耐药性。作者聚焦于一种名为 CBX2 的蛋白,它识别 DNA 包装上的化学标记,并且在卵巢肿瘤中表达高于正常组织。在患者数据库和组织样本中,CBX2 水平更高的肿瘤更可能对铂类治疗产生耐药并更早复发,尤其是在这种侵袭性卵巢癌亚型中。
细胞核内的液滴:增强修复的“工作台”
CBX2 具有在细胞核内形成致密液滴状聚集体的非同寻常能力,这一过程被称为相分离。这些液滴像微小的液体工作台,能够富集特定蛋白。通过比较正常 CBX2、缺失 CBX2 或无法形成液滴的突变体,研究人员表明 CBX2 液滴是肿瘤细胞修复断裂 DNA 的核心。当去除 CBX2 时,染色体断裂增多,DNA 损伤信号积累,两条主要的双链断裂修复通路均被削弱。恢复正常 CBX2 能够恢复这些修复功能,但不能形成液滴的变体则不能恢复,尽管它仍能结合 DNA。 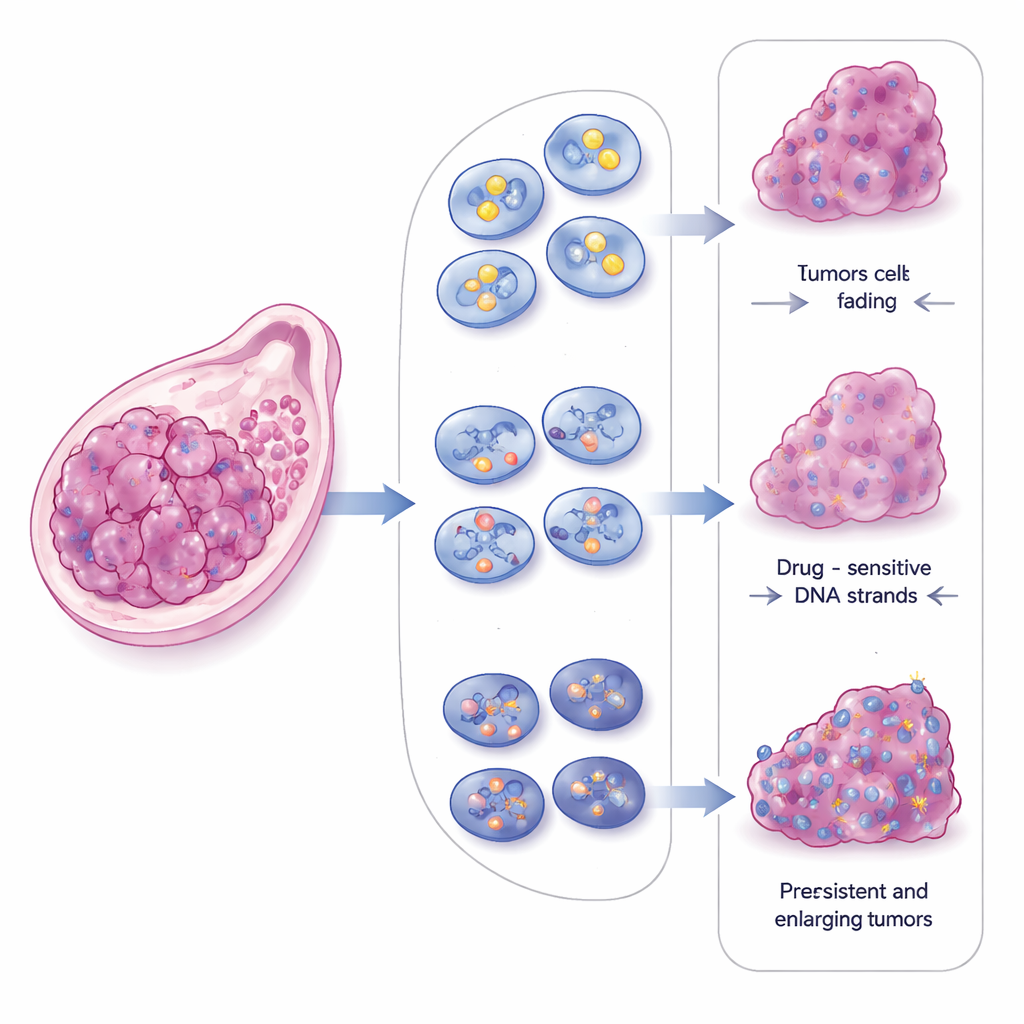
CBX2 液滴如何组织修复团队
进一步研究中,团队检测了在有或没有 CBX2 液滴时,哪些修复蛋白会附着到 DNA 上。他们发现 CBX2 液滴有助于招募损伤应答中的关键成员,包括 PARP1、53BP1、BRCA1 和 RAD51——这些蛋白决定断裂的修复方式并执行修复。活细胞成像显示两类 CBX2 液滴:一种是可移动的液态形态,能动态与受损染色质混合;另一种是密集、类固体的形态,不会混合。只有可移动的液滴与 DNA 损伤焦点和主要修复蛋白重叠,这表明这种流动相是功能性支架,精确地聚集并组织修复机器到需要的位置。
用现有药物把优势变成弱点
鉴于 CBX2 液滴让肿瘤细胞在 DNA 修复方面具有优势,作者进一步探讨是否可以将这种增强的修复能力作为靶点。他们在有或没有功能性 CBX2 液滴的细胞上筛选了化合物库,发现伊布替尼——一种已被批准用于某些血液肿瘤的口服药——对依赖 CBX2 浓缩体的细胞表现出特殊毒性。伊布替尼并不阻止液滴形成,但它选择性地削弱了这些细胞依赖的高保真修复通路。在动物模型中,含有 CBX2 液滴的肿瘤在伊布替尼治疗下缩小,并且来自患者高 CBX2 水平肿瘤培养的三维类器官对该药更敏感,而低水平的类器官则不然。 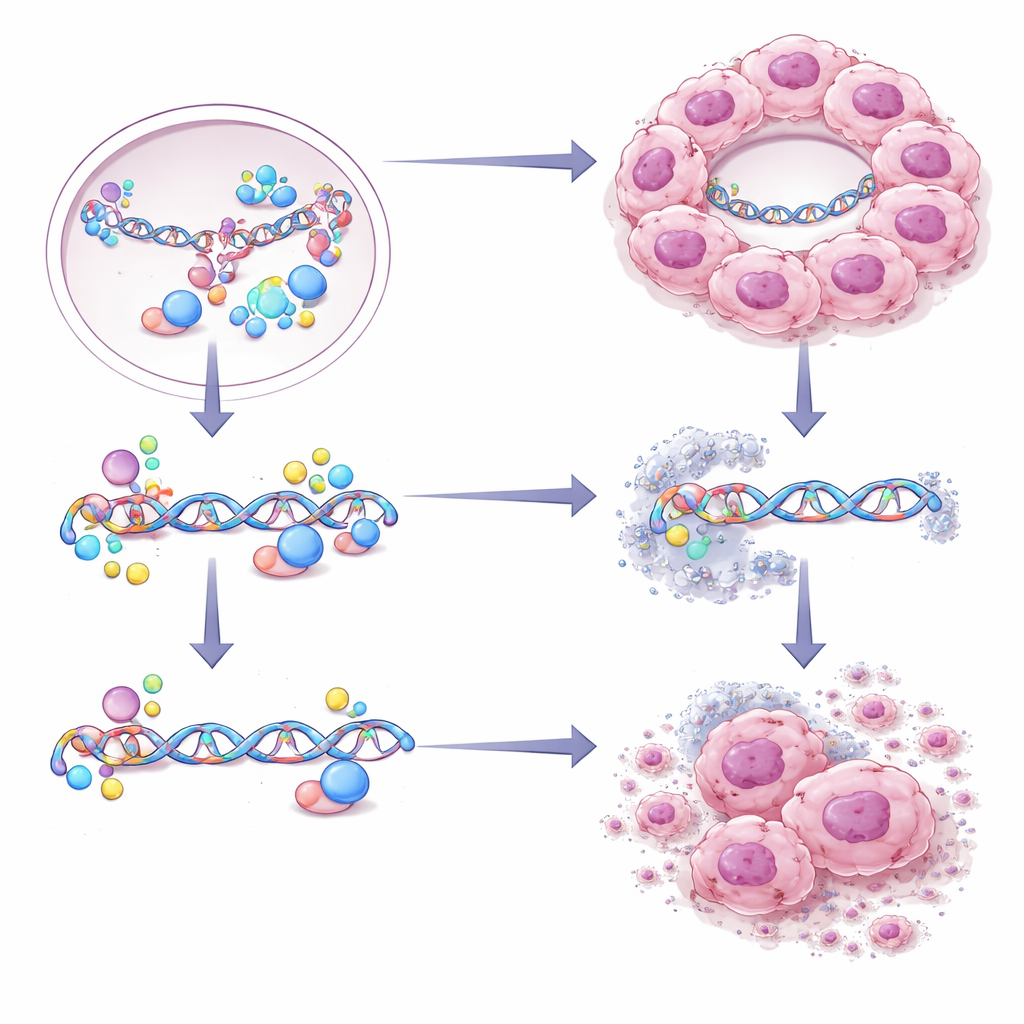
这对患者可能意味着什么
对患者而言,这项研究提出了两个重要观点。首先,肿瘤组织中 CBX2 液滴的存在与分布模式,可能有助于预测对铂类化疗和 PARP 抑制剂的反应:缺乏 CBX2 的患者预后最好,CBX2 弥散分布者居中,而具有明显 CBX2 浓缩体的患者预后最差。第二,相同的液滴模式可能标识出可能从伊布替尼获益的患者,将一种血液肿瘤药物重新用于难治的卵巢癌亚型。本质上,这项工作表明,保护肿瘤 DNA 的结构同时也可能暴露新的阿喀琉斯之踵——为更个体化和更有效的治疗提供了潜在途径。
引用: Sun, S., Huang, L., Ma, Y. et al. CBX2 phase-separation contributes to homologous recombination repair and drug resistance in ovarian cancer. Cell Death Dis 17, 366 (2026). https://doi.org/10.1038/s41419-026-08605-4
关键词: 卵巢癌, 药物耐药, DNA 修复, 相分离, 伊布替尼