Clear Sky Science · zh
黑色素瘤外泌体miR-708-5p促进巨噬细胞M2极化与癌症转移
皮肤癌如何智胜免疫系统
黑色素瘤是一种危险的皮肤癌,但它并非单靠自身生长和扩散。它劫持邻近的免疫细胞,将原本对抗肿瘤的细胞变成助纣为虐的帮手。本研究揭示了一种被黑色素瘤细胞通过小囊泡输出的微小遗传信使,这种信使重编程名为巨噬细胞的免疫细胞,营造出一个有利于癌细胞生长与转移的“避风港”。
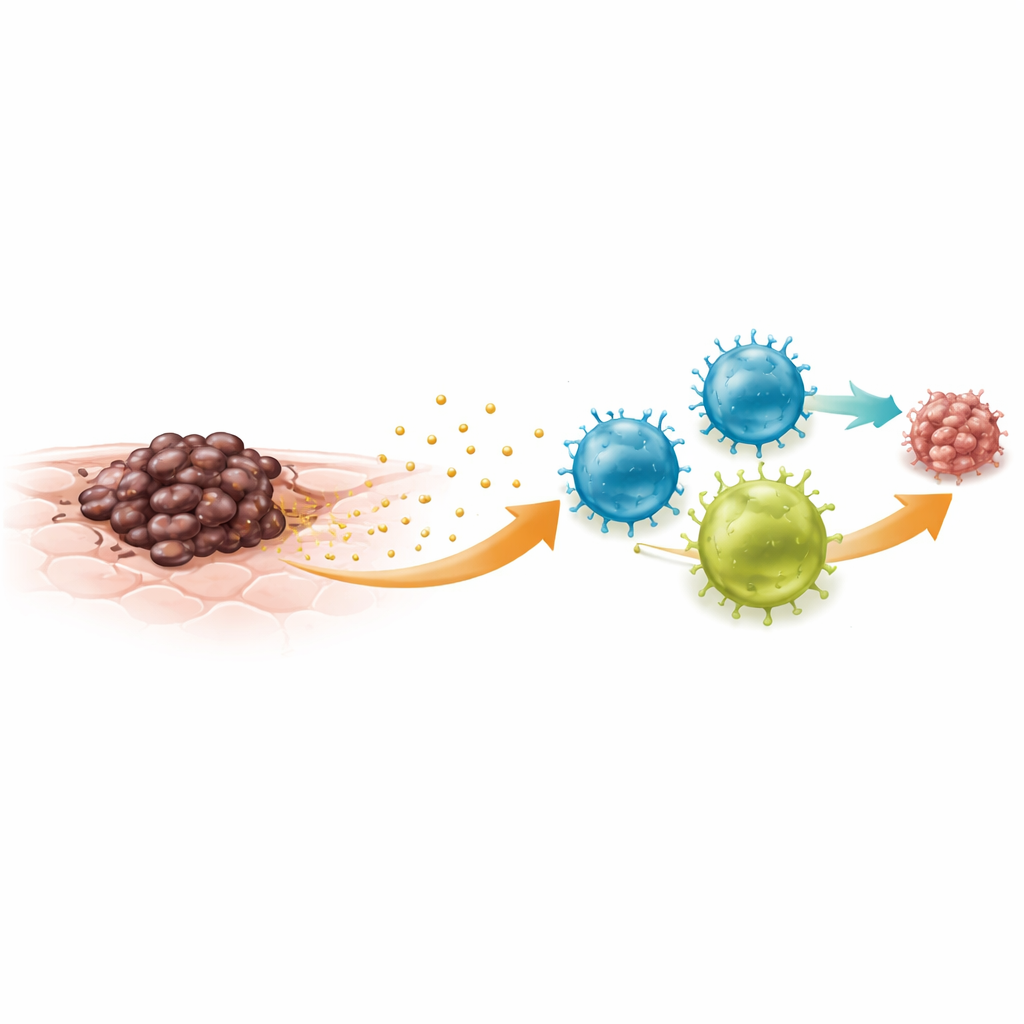
肿瘤友好的免疫帮手
巨噬细胞通常在体内巡逻,吞噬病原体和受损细胞。然而在肿瘤中,它们可以呈现两类广义状态:一类具有攻击性并抗肿瘤,另一类偏向抚慰与创伤修复,抑制免疫攻击并帮助组织重塑。包括黑色素瘤在内的许多肿瘤中富含第二种即“肿瘤友好”型巨噬细胞。肿瘤中这类巨噬细胞数量多的患者常面临更快的病情进展和更差的预后。理解黑色素瘤如何将巨噬细胞推向这种支持性角色,可能为阻止疾病提供新的策略。
微小囊泡传递强有力的信息
研究者关注的是外泌体——细胞释放的纳米级囊泡,可携带蛋白质与遗传物质到远处目标。当将黑色素瘤细胞与人巨噬细胞共培养时,巨噬细胞被诱导向肿瘤支持型状态转变。阻断外泌体释放明显减少了这种转变,表明外泌体是关键信使。进一步分析显示,来源于黑色素瘤的外泌体富含一种名为miR-708-5p的小型调控RNA。当巨噬细胞摄取这些外泌体后,其细胞内该microRNA水平升高,尽管巨噬细胞自身的生物合成机械并未改变,说明信号直接来源于肿瘤细胞。
将巨噬细胞从防御者改造成同谋
通过人为提高或阻断巨噬细胞内的miR-708-5p,研究团队证明这一单一microRNA足以改变它们的行为。miR-708-5p水平升高会增强肿瘤支持型表型的典型特征,包括吞噬癌细胞能力下降以及更多抑制性分子(如IL-10和TGF-β)的释放。这些被重编程的巨噬细胞反过来使黑色素瘤细胞在体外试验中生长更快、迁移更活跃并更容易穿透屏障。在小鼠体内,受此类条件化巨噬细胞包围的黑色素瘤肿瘤长得更大并产生更多肺转移,证实了这种改变的免疫支持在活体中具有重要意义。
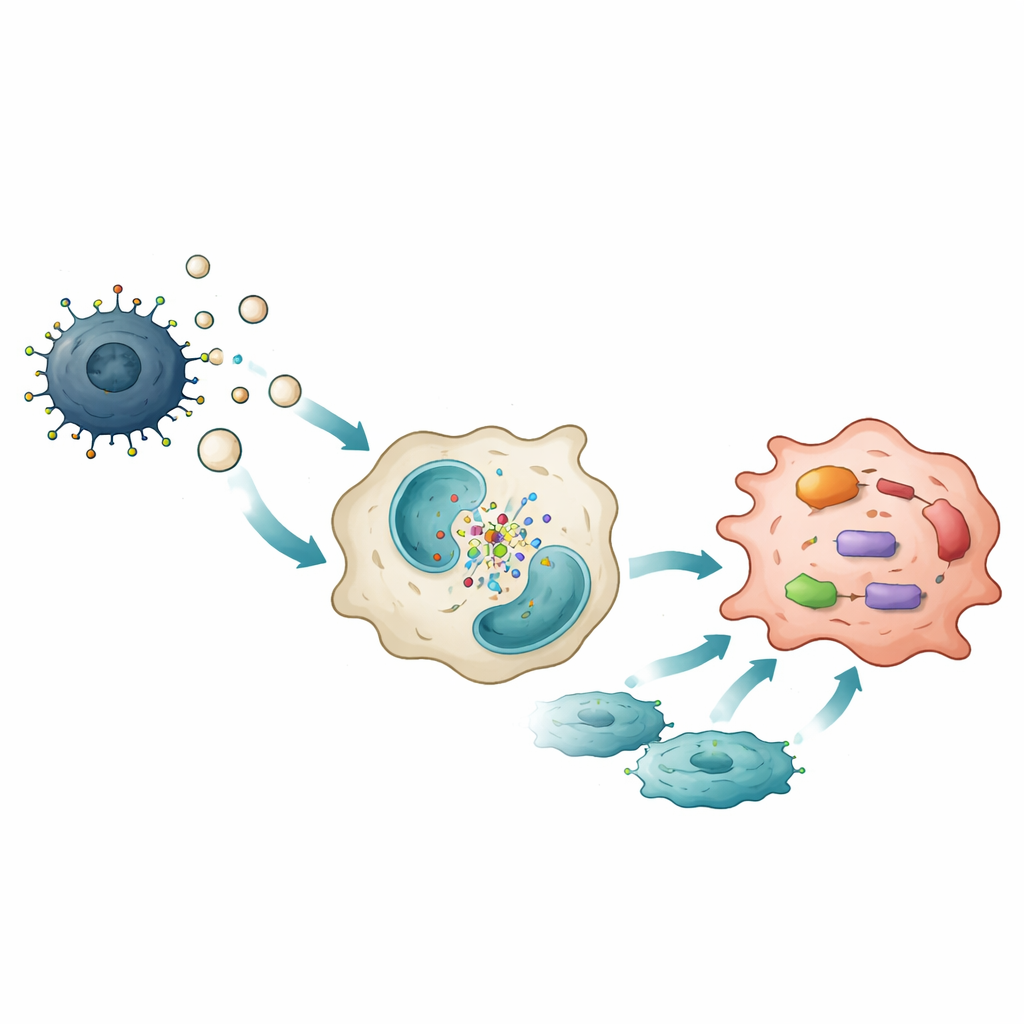
一个隐藏的靶点开启生长信号
为弄清miR-708-5p如何发挥作用,研究者在巨噬细胞中寻找其被抑制的基因,确认了一种名为FOXN3的蛋白是其主要靶点。在正常情况下,FOXN3有助于抑制细胞内一个重要的生长调控通路——PI3K/AKT/mTOR通路。当miR-708-5p水平上升时,FOXN3水平下降,该通路被激活,推动巨噬细胞朝肿瘤支持型表型转变。在巨噬细胞中恢复FOXN3可逆转这种转变并削弱其促进黑色素瘤细胞生长与扩散的能力。与此同时,研究团队发现黑色素瘤细胞似乎将miR-708-5p排出体外,因为将其保留在细胞内实际上会减慢肿瘤细胞分裂并增加细胞死亡,这揭示了肿瘤抛弃内部制动器并利用它来操控邻近免疫细胞的巧妙方式。
将癌症伎俩转化为治疗线索
这项工作表明,黑色素瘤细胞通过与结合伙伴SFRS1协作,将miR-708-5p装入外泌体并输出到周围巨噬细胞,从而翻动由FOXN3控制的开关,激活生长信号并促成一个有利于肿瘤的免疫环境。对非专业读者而言,结论是:黑色素瘤既能抛弃一种对自身不利的分子,又能将其武器化以削弱免疫系统。由于miR-708-5p和FOXN3处于这一通信回路的核心,针对巨噬细胞中该microRNA的阻断或恢复FOXN3活性的治疗策略,可能有助于重新唤醒免疫防御并减缓黑色素瘤进展。
引用: Xu, M., He, B., Zhou, X. et al. Melanoma exosomal miR-708-5p promotes macrophage M2 polarization and cancer metastasis. Cell Death Dis 17, 346 (2026). https://doi.org/10.1038/s41419-026-08597-1
关键词: 黑色素瘤, 肿瘤微环境, 外泌体, 巨噬细胞, 微小RNA