Clear Sky Science · zh
来自前列腺癌细胞对巨噬细胞的反馈机制,由STAT1强化,调控肿瘤进展和放疗耐受性
这项研究为何重要
放疗是治疗前列腺癌的重要手段,但许多肿瘤会逐渐失去反应性,导致疾病复发或转移。本研究揭示了前列腺癌细胞与邻近免疫细胞(巨噬细胞)之间一种被隐藏的化学“对话”,这种对话有助于肿瘤在放疗下存活。解析这一环路,研究者指出了若干新的药物靶点,可能使放疗对晚期前列腺癌患者更有效。
不同方式燃烧糖的癌细胞
像许多肿瘤一样,前列腺癌细胞依赖一种改变了的糖代谢方式,即有氧糖酵解。它们并不通过氧气完全分解糖,而是选择一种更快但效率较低的途径,产生大量乳酸。研究组在肿瘤细胞内鉴定出一种蛋白STAT1,作为开启这种嗜糖状态的关键开关。STAT1 提高了驱动糖酵解的三种核心酶的活性,增加了葡萄糖摄取和乳酸产生。在细胞培养和小鼠模型中,STAT1 水平较高的肿瘤生长更快、对放疗更具耐受性,而阻断糖酵解则削弱了这些侵袭性特征。 
肿瘤代谢废物如何重塑免疫细胞
乳酸常被视为代谢“废物”,但在肿瘤微环境中它更像一种信号分子。研究者表明,前列腺癌细胞释放的乳酸通过一种名为MCT1的膜转运蛋白被巨噬细胞摄取。乳酸进入细胞后激活了称为NFκB的内在报警系统,促使巨噬细胞向一种被称为M2的辅助状态转变。M2型巨噬细胞往往不会攻击癌细胞,而是压制免疫反应并支持肿瘤生长,例如促进血管生成。当科学家们在癌细胞中阻断糖酵解、抑制乳酸产生或阻止乳酸进入巨噬细胞时,这些免疫细胞便从支持肿瘤的M2状态转向更具防御性的表型。
巨噬细胞向肿瘤反馈生长信号
故事并不止于巨噬细胞性格的改变。乳酸在巨噬细胞内激活NFκB后,巨噬细胞开始产生并分泌一种强效的信号分子MCP-1。该分子扩散回前列腺癌细胞并与表面受体CCR2结合。该结合在癌细胞内激活另一条通路,涉及JAK蛋白和STAT1。换言之,最初驱动过度糖代谢的STAT1,会再次被一条最终追溯到它所促成的乳酸的信号所激活。当研究者向前列腺癌细胞添加MCP-1时,糖酵解增强,细胞增殖和迁移能力提高,且对放疗诱导的DNA损伤修复更为高效。阻断CCR2或JAK可以阻止这些效应。
自我强化的生存回路
综合来看,结果揭示了癌细胞与巨噬细胞之间的自我强化回路。前列腺癌细胞内的STAT1增强糖分解并增加乳酸释放。这些乳酸被巨噬细胞摄入,激活NFκB并促使其进入支持肿瘤的M2状态,同时诱导MCP-1生成。MCP-1再返回癌细胞,激活CCR2和JAK/STAT1通路,进一步强化糖酵解和放疗耐受性。动物实验显示,阻断CCR2或JAK的药物,尤其与放疗联合使用时,可减缓肿瘤生长并减少M2巨噬细胞的存在,凸显了针对该环路的临床前景。 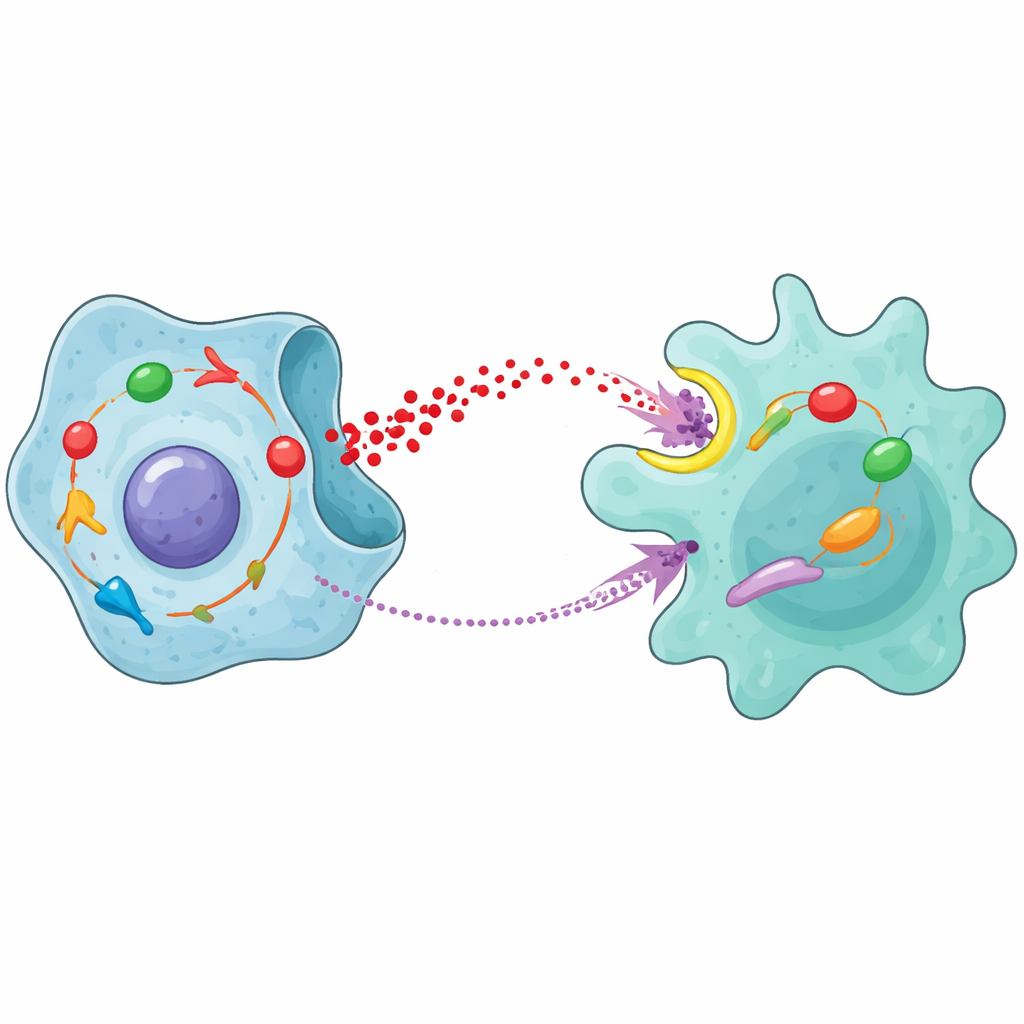
对患者意味着什么
对普通读者来说,关键观点是前列腺肿瘤与某些免疫细胞形成了一种化学伙伴关系,帮助肿瘤在放疗下幸存。肿瘤细胞改变了糖的利用方式,产生的乳酸将邻近巨噬细胞重新编程为盟友而非敌人。被重新编程的细胞又发回信号,使肿瘤更顽强、更难以消灭。通过在乳酸处理、MCP-1信号或下游JAK/STAT1通路等环节中断这一回路,未来的治疗或能削弱肿瘤的防御,使放疗更有效,为难治性前列腺癌患者带来新的希望。
引用: Chen, JY., Xue, YT., Lin, B. et al. A feedback mechanism from prostate cancer cells to macrophages, reinforced by STAT1, regulates tumor progression and resistance to radiotherapy. Cell Death Dis 17, 282 (2026). https://doi.org/10.1038/s41419-026-08577-5
关键词: 前列腺癌, 放疗耐受性, 肿瘤微环境, 巨噬细胞, 乳酸代谢