Clear Sky Science · zh
HNRNPH1通过调节细胞周期基因的剪接驱动胶质母细胞瘤进展
这项脑癌研究为何重要
胶质母细胞瘤是最致命的脑癌之一,部分原因在于其细胞分裂迅速同时还能避免自我毁灭。该研究揭示了肿瘤细胞内一种鲜为人知的分子如何帮助它们维持有序分裂,而不至于瓦解。通过揭露这一隐蔽的支持系统,研究为未来可能将胶质母细胞瘤细胞推至崩溃并阻止肿瘤生长的策略指明了新方向。
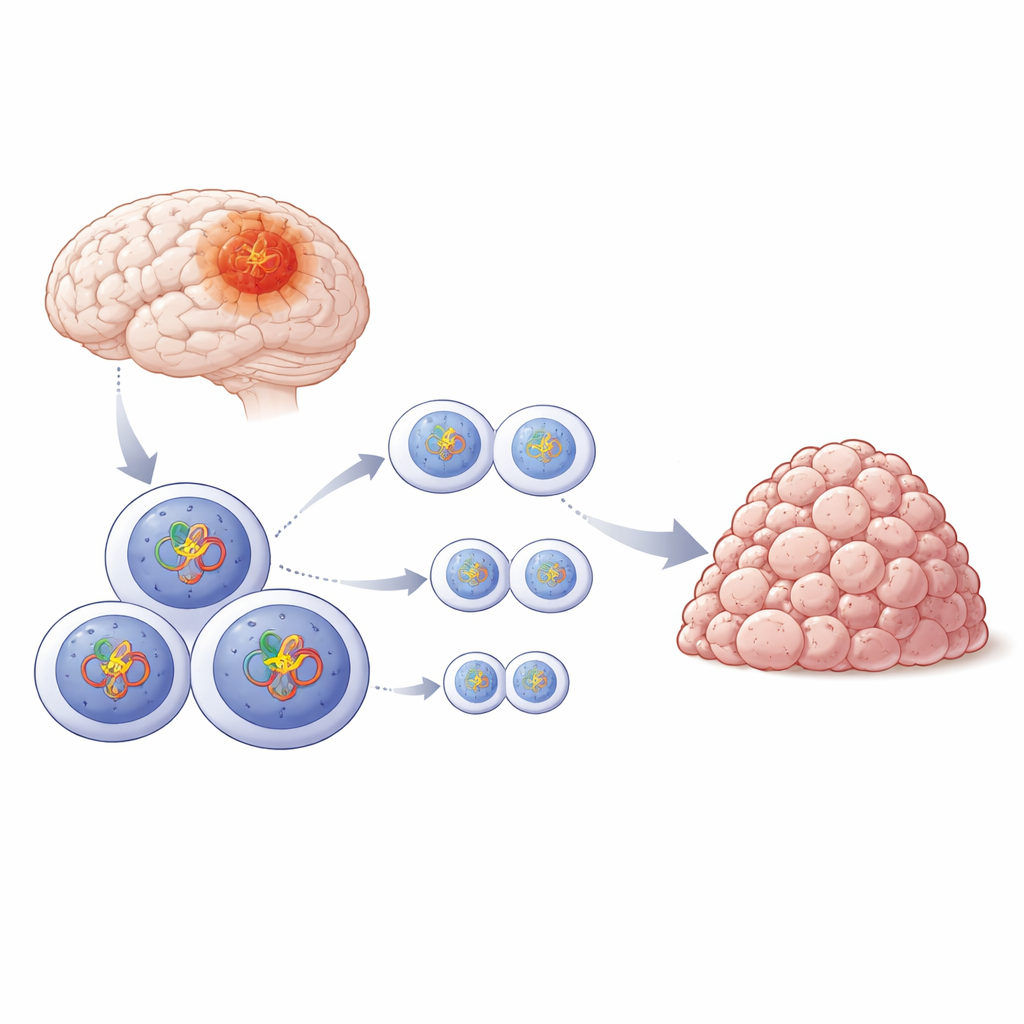
肿瘤细胞内的隐秘帮手
研究人员聚焦于胶质母细胞瘤,这是一种通常对手术、放疗和化疗具有抵抗性的侵袭性脑瘤。癌细胞通常携带许多驱动其分裂的DNA突变,但在每次细胞周期中复制和分离染色体仍然依赖完好的机制。如果这些机制失灵,细胞可能通过一种称为“有丝分裂灾难”的过程死亡。研究团队探究了哪些分子参与者帮助胶质母细胞瘤细胞在基因组受损的情况下仍能维持这一脆弱的分裂过程。
遗传信息的交通指挥官
他们将注意力集中在一种名为HNRNPH1的蛋白上,该蛋白属于一类结合RNA(从DNA拷贝出的短暂信息)的分子家族。这些蛋白调控原始RNA转录本在被剪切和拼接以生成蛋白前的处理方式——即剪接过程。通过分析大量病人数据集和肿瘤样本,科学家们发现HNRNPH1在胶质母细胞瘤组织中的表达远高于正常脑组织。单细胞和空间表达图谱显示,它在类似未成熟且快速分裂的肿瘤细胞以及肿瘤中富氧、高增殖的区域中特别丰富,而在缺氧、受压的区域则明显较低。
HNRNPH1如何维持细胞分裂秩序
为了观察去除HNRNPH1的后果,团队使用基因编辑和RNA沉默工具在培养的胶质母细胞瘤细胞中降低该蛋白的水平。这引发了数千个基因活动的巨量变化,尤其强烈影响那些控制G2/M检查点——细胞分裂前的最后质量控制步骤的基因。研究发现HNRNPH1能直接结合若干关键分裂调节因子的RNA蓝本,包括帮助染色体正确分离的蛋白。当HNRNPH1缺失时,这些RNA被错误剪接或产量降低,导致维持有序有丝分裂所需的蛋白数量减少。
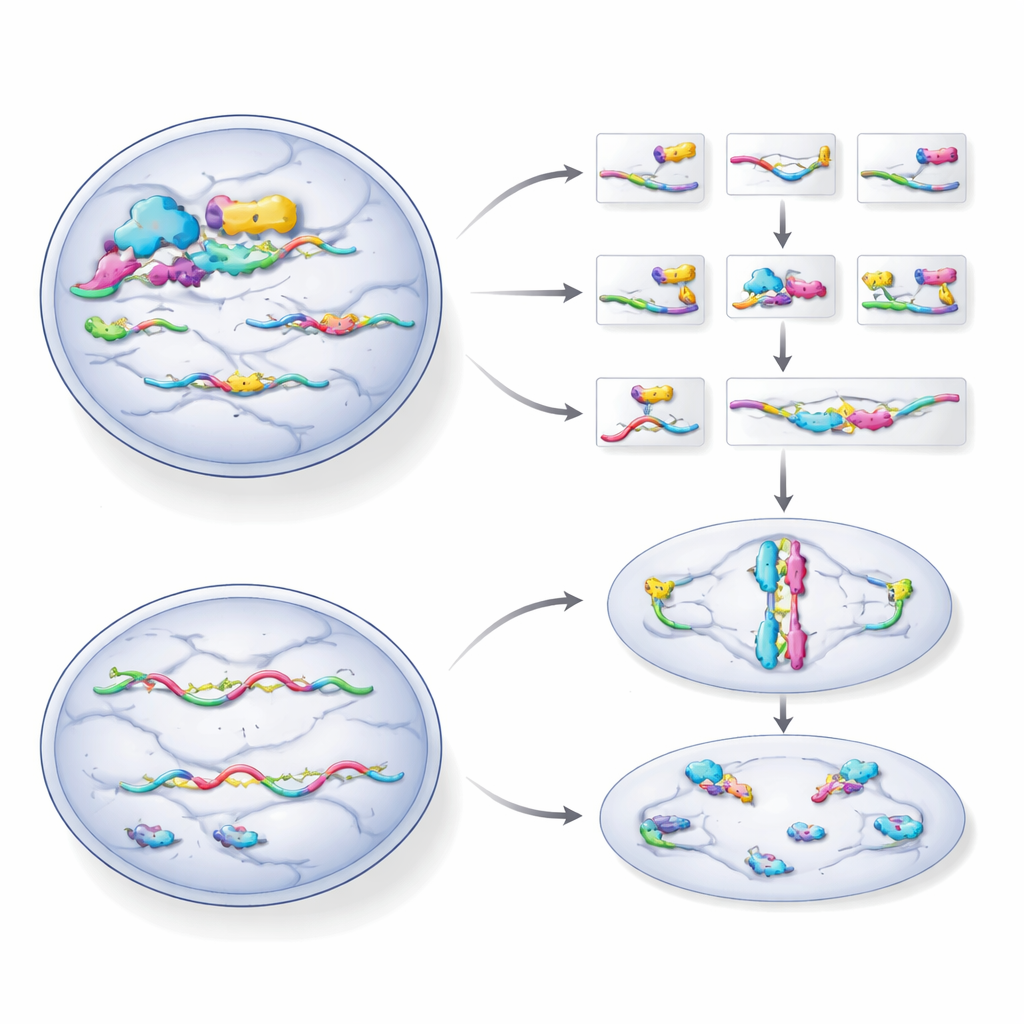
帮手消失时,细胞分裂受挫
缺乏HNRNPH1的细胞生长减慢,在细胞周期后期积累,并出现核增大、形态异常或碎裂的现象——这些都是分裂出问题的典型标志。在显微镜下,处于正常有丝分裂过程中的细胞减少,其用于拉开染色体的内部支架也被破坏。团队还发现HNRNPH1引导另一种调节因子UHRF2的剪接,使其RNA在生成型和缺陷型之间切换。没有HNRNPH1时,更多UHRF2信息被错误编辑,功能性蛋白量下降,进一步扰乱细胞周期控制。
来自活体肿瘤的证据
随后科学家在小鼠模型中测试了HNRNPH1的重要性。他们将人类胶质母细胞瘤细胞(正常或被工程化降低HNRNPH1表达)植入小鼠脑内。接受对照细胞的小鼠很快长出大肿瘤并较早死亡。而接受HNRNPH1敲低细胞的小鼠,肿瘤形成明显更小或延迟,存活期更长。然而,最终长大的肿瘤恢复了HNRNPH1的活性,这表明无法恢复该蛋白的细胞处于明显劣势,无法维持肿瘤生长。
对未来治疗的意义
总体而言,该研究表明胶质母细胞瘤细胞依赖HNRNPH1来正确处理一组控制细胞分裂的遗传信息网络,从而使它们能够增殖而不会立即自我毁灭。对于非专业读者而言,这种蛋白可以被视为在幕后编辑者,保持癌细胞“说明书”的可读性。破坏HNRNPH1或其控制的特定剪接事件,可能使肿瘤细胞在分裂时更易出现致命错误,为一种潜在的新疗法途径打开可能性——将肿瘤推过其容忍极限,同时可与现有治疗互为补充。
引用: Villa, G.R., Alimonti, P., Toker, J.S. et al. HNRNPH1 drives glioblastoma progression by regulating the splicing of cell cycle genes. Cell Death Dis 17, 352 (2026). https://doi.org/10.1038/s41419-026-08576-6
关键词: 胶质母细胞瘤, 细胞周期, RNA剪接, 肿瘤生物学, 脑肿瘤