Clear Sky Science · zh
疫苗相关激酶2抑制揭示胰腺癌谷胱甘肽代谢的脆弱性
这对胰腺癌为何重要
胰腺癌是最致命的癌症之一,部分原因在于标准治疗往往无效。本研究揭示了某些胰腺肿瘤的一个隐性弱点:依赖于一种细胞“护盾”来抵御有毒氧副产物。通过弄清楚何时该护盾脆弱,以及一个名为VRK2的癌基因如何强化它,研究人员提出了在尽量不伤害正常组织的情况下选择性毒杀癌细胞的新思路。
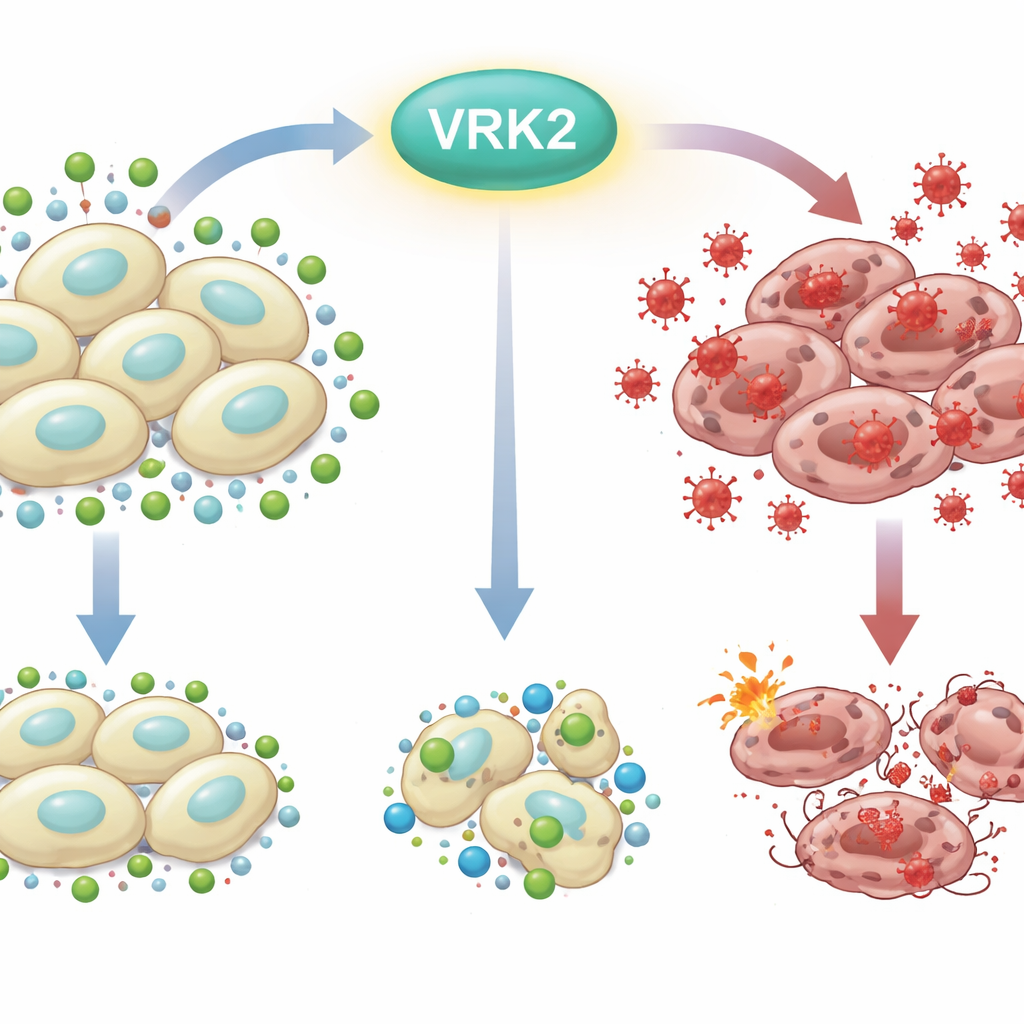
细胞的“生锈”问题
每个细胞都在持续与由活性氧物种引起的“内部生锈”作斗争——这些活性氧是高度反应性的氧形式,会损伤DNA、脂质和蛋白质。为生存,细胞使用化学防御,其中谷胱甘肽是最重要的护盾之一。胰腺癌细胞在恶劣环境中生长迅速,严重依赖代谢策略来维持充足的谷胱甘肽。破坏该有害氧化剂与保护性抗氧化剂之间的平衡可以将癌细胞推向死亡边缘。
发现一个隐蔽弱点
研究人员首先关闭了VRK2——一个先前与胰腺癌不良预后相关的促癌基因——然后测试了281种针对代谢的化合物。他们发现缺失VRK2的细胞对阻断谷胱甘肽生成的药物异常敏感。在这些缺乏VRK2的细胞中,谷胱甘肽水平下降,而活性氧上升,导致细胞死亡。补充额外的抗氧化剂或类似谷胱甘肽的分子能拯救这些细胞,证实了关键弱点确实在于它们解毒氧化应激的能力受损。
VRK2如何帮助癌细胞加固护甲
接着,团队探问为何VRK2会改变谷胱甘肽代谢。他们把目标锁定在一个名为SLC7A11的转运蛋白上,该蛋白位于细胞外膜,负责运输半胱氨酸(二硫键形式为半胱氨酸硫氢化合物的硫代物——注:文中指半胱氨酸的二聚体半胱氨酸/胱氨酸),为合成谷胱甘肽提供原料。出人意料的是,VRK2并不改变细胞总体生产SLC7A11的量;相反,它控制该转运蛋白能否成功到达细胞表面。在VRK2活跃的健康细胞中,SLC7A11从内质网转运到高尔基,然后到达膜。VRK2通过化学修饰一个名为Sec24C的货物分选蛋白来增强这种转运,Sec24C有助于把SLC7A11装入运输囊泡。当VRK2缺失或被抑制时,SLC7A11滞留在细胞内部,表面可用的转运蛋白减少,谷胱甘肽护盾随之削弱。
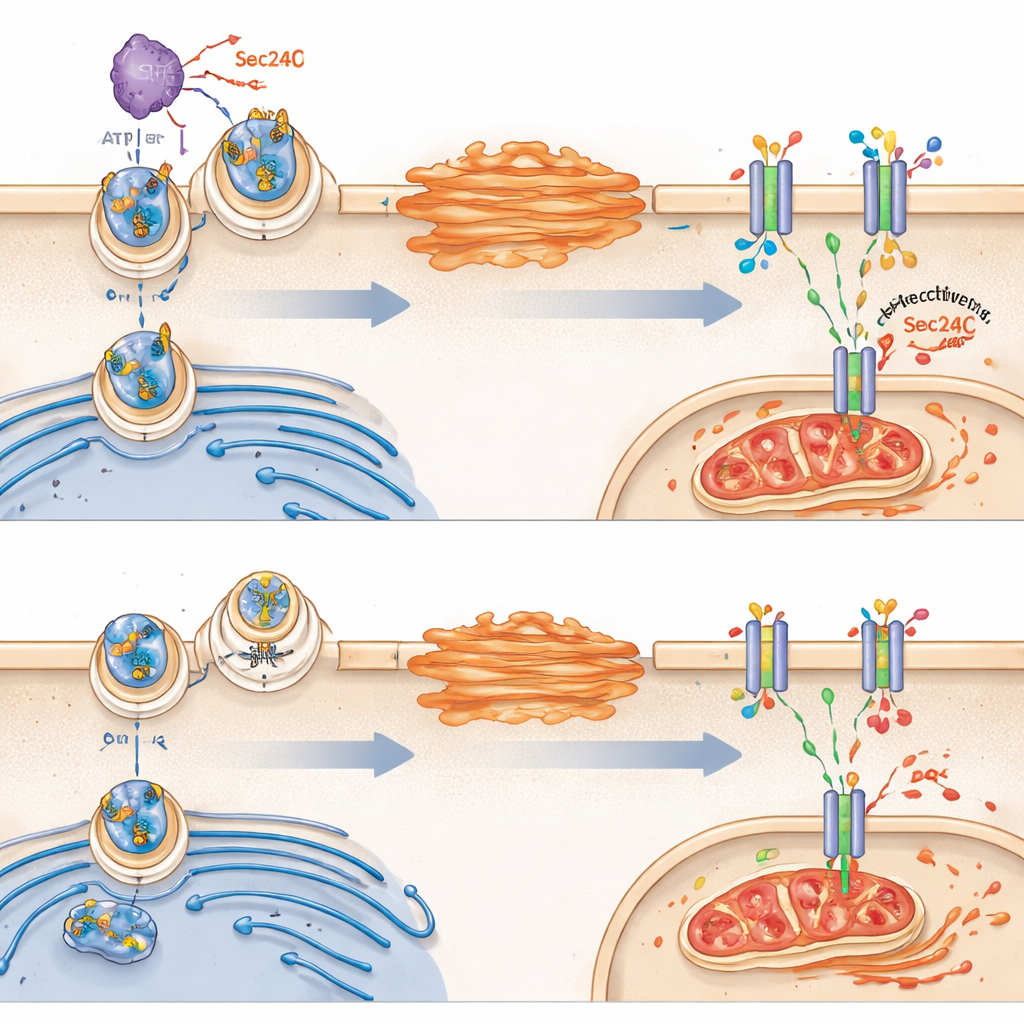
从破损护盾到铁死亡
没有足够的膜上SLC7A11,缺乏VRK2的细胞难以摄取胱氨酸并维持谷胱甘肽水平。这使它们尤其易受一种依赖铁的细胞死亡形式——铁死亡(ferroptosis)的影响,其特征是细胞膜脂质的失控氧化和线粒体损伤。研究表明,切断谷胱甘肽合成的药物在缺乏VRK2的细胞中诱发了铁死亡的标志性变化,包括畸形的线粒体和脂质氧化产物的积累。阻断铁死亡(而非其他类型的细胞死亡)能保护这些细胞,强调了它们的致命弱点是无法遏制氧化损伤。
指导个体化治疗选择
最后,研究人员将研究推进到动物模型和来自患者的新鲜细胞来源。低VRK2水平的肿瘤在使用靶向谷胱甘肽的药物治疗后缩小,而高VRK2表达的肿瘤则大多抵抗该药物。然而,当对高VRK2肿瘤同时使用VRK2抑制剂时,这些肿瘤重新对谷胱甘肽抑制敏感。这表明VRK2水平可以将患者划分为不同组别:一类肿瘤天然易感于针对谷胱甘肽的治疗,另一类则可能受益于先抑制VRK2再攻击谷胱甘肽代谢的两步策略。
这对患者意味着什么
简而言之,这项工作表明一些胰腺癌通过利用VRK2来维持其抗氧化护盾以求生存。去除VRK2后,该护盾变薄;在此基础上再去除谷胱甘肽,癌细胞将在氧化应激下崩溃。因此,测定肿瘤中的VRK2水平可能帮助医生判断谁最有可能从破坏谷胱甘肽代谢的药物中获益,谁可能首先需要一步针对VRK2的治疗。尽管仍需更多人体试验,但该研究为这一迫切需要更好疗法的癌症描绘了一条清晰的代谢学个体化治疗路径。
引用: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
关键词: 胰腺癌, 谷胱甘肽代谢, VRK2, 铁死亡, SLC7A11