Clear Sky Science · zh
PD-1通过调节TCR和CD28信号保护增殖的人类T细胞免受过早的再刺激诱导细胞死亡
为何阻止免疫系统的“误伤”至关重要
我们的免疫系统依赖大量迅速增殖的T细胞来对抗感染和癌症。但这种爆发式增长也存在风险:如果过多的T细胞在体内长时间处于活跃状态,可能损伤健康组织或诱发自身免疫性疾病。本研究探讨了一种著名的T细胞“刹车”分子PD‑1,如何帮助正在扩增的人类T细胞避免因自身过度活化而过早死亡。理解这种平衡对于更安全的癌症免疫治疗以及预防有害的免疫过度反应至关重要。
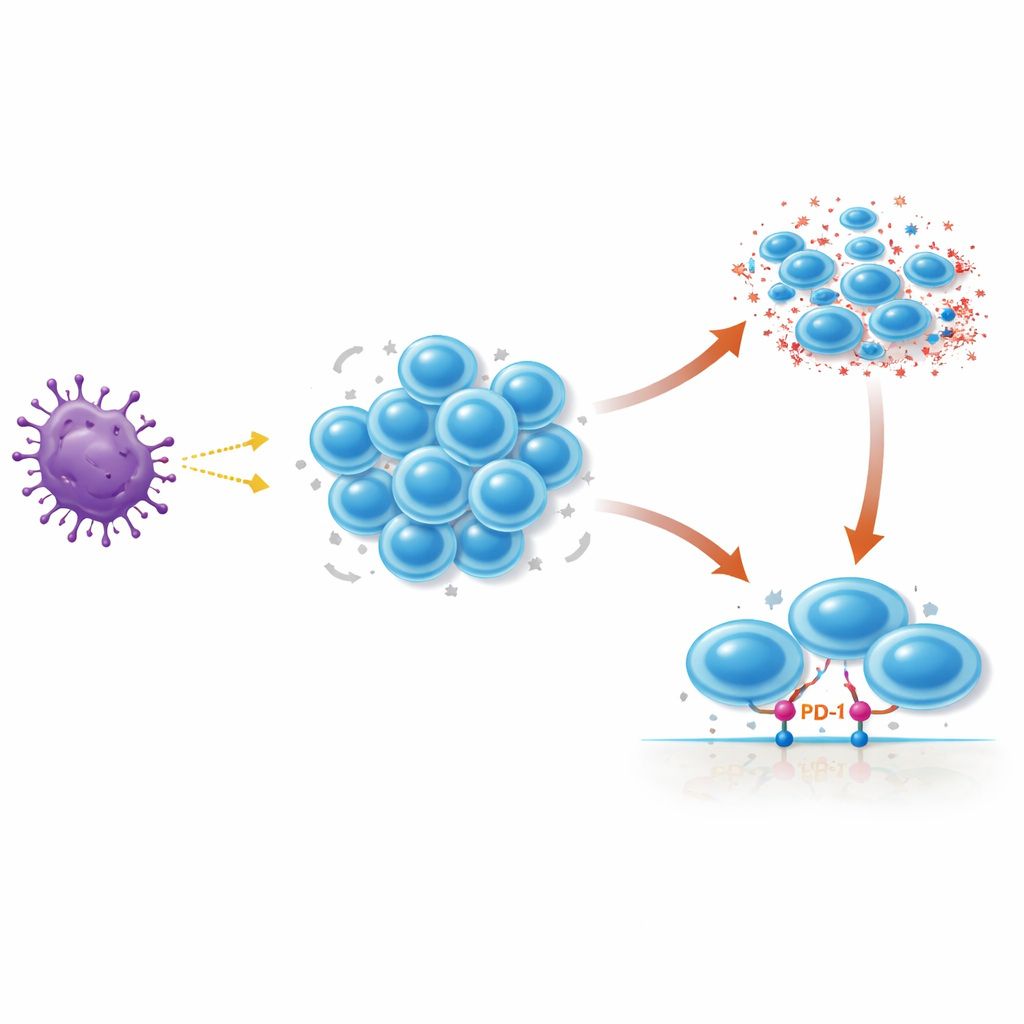
一个必须精确计时的内置自毁程序
一旦T细胞识别到威胁,它们会分裂形成大量同质的作战克隆。为防止这种反应失控,T细胞内存在一套内置的自毁程序,称为再刺激诱导细胞死亡(RICD)。当已经被激活的T细胞通过其主要感受器——T细胞受体(TCR)再次受到强烈刺激时,RICD可以被触发以杀死该细胞。这有助于在威胁清除后缩减细胞数量,并避免发生T细胞过度增殖性疾病。然而,在反应早期,T细胞需要时间扩增,使得这一自毁通路不会过早占主导地位,而这种时机在人体内如何被调控尚不完全清楚。
免疫刹车的意外保护作用
PD‑1因是癌症治疗中“检查点”药物的靶点而闻名,阻断它可以重新唤醒肿瘤内功能衰竭的T细胞。传统上PD‑1被视为削弱T细胞活性的分子,但在人类T细胞首次遇到刺激时,PD‑1会迅速被上调,并在其早期扩增阶段维持中等水平。本研究中,研究人员从健康供者分离出人类CD4和CD8 T细胞,在体外激活并随时间追踪PD‑1及其配体PD‑L1的表达。他们发现PD‑1和PD‑L1在激活后几天内达到高峰——正值T细胞大量增殖之时——随后随着细胞成熟而下降。当团队在重复刺激期间阻断PD‑1或PD‑L1时,更多T细胞死亡,表明正常的PD‑1信号实际上保护这些扩增中的细胞免受过早的RICD。
PD‑1如何重塑细胞表面的“对话”
为更精确地探究这种保护作用,科学家构建了人工的“代理”抗原呈递微珠,这些微珠包被有激活信号(模拟T细胞受体和其主要协助分子CD28),并在部分情况下带有PD‑L1。当扩增中的T细胞用携带PD‑L1的微珠重新刺激时,与对照微珠相比,细胞丢失明显减少,早期和晚期凋亡的标准标志物也回落到基线附近。这种存活提升取决于PD‑L1的含量以及PD‑L1是否与激活信号紧密相邻,类似天然免疫突触的紧密组织结构。有趣的是,当CD28与T细胞受体同时参与时,保护效应最为显著,表明PD‑1同时收束了两条激活通路。缺乏PD‑1时,CD28会使细胞更容易发生RICD,但加入PD‑L1可以消除这种额外的敏感性。
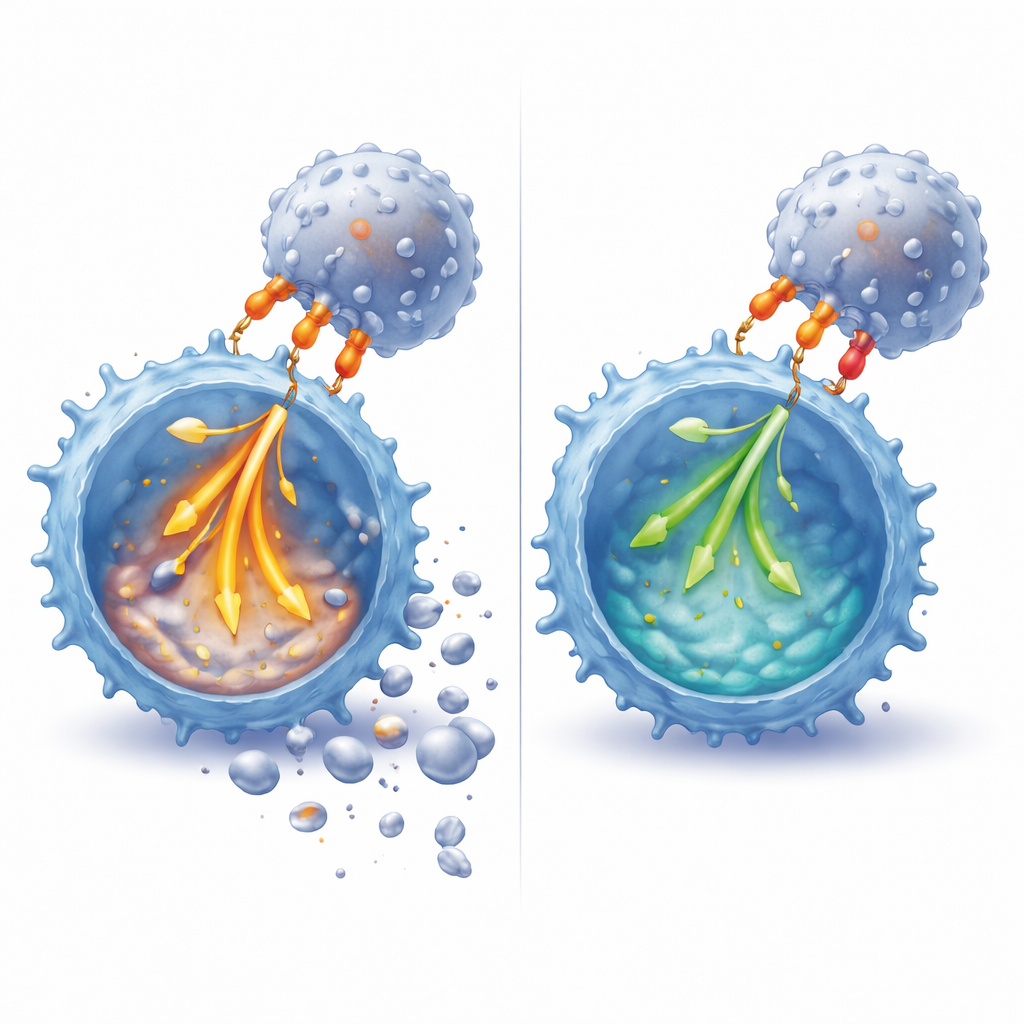
降低信号强度并倾向存活分子
在细胞内检测时,研究人员发现PD‑1的参与削弱了再刺激后的一系列早期信号事件。关键传导蛋白上的磷酸化标记——包括与受体直接相关的组分和一个名为ERK的中心中继酶——在有PD‑L1存在时显著减少。这种钝化在同时激活CD28时尤为明显,呼应了该情形下对RICD影响更大的观察结果。PD‑1信号还影响细胞周期,使更多细胞滞留在G1“检查点”阶段,而不是被推动进入DNA复制期,而后者已知会提高对死亡信号的敏感性。在蛋白水平上,PD‑1使促死与促存活分子的平衡发生倾斜:它抑制了FAS配体(一种关键的T细胞杀伤触发因子)的诱导,并有助于维持survivin(一种支持T细胞存活与受控分裂的因子)。
这些发现对治疗和免疫健康的意义
总体而言,结果显示PD‑1并非简单地关闭T细胞,而是一种微调器,保护新激活的人类T细胞在扩增期间不被过早淘汰。通过减弱TCR和CD28两者的重复信号强度,并偏向促存活分子而非促死亡触发因子,PD‑1允许在自毁程序完全启动前形成既强劲又受控的T细胞“军队”。对患者而言,这意味着阻断PD‑1的药物——尽管是肿瘤学中的强效工具——也可能使部分T细胞更易受到RICD的影响,从而改变正常的免疫平衡或促成副作用。未来的治疗以及诸如CAR‑T细胞的细胞疗法,可能受益于有意调节PD‑1及相关通路,以在保留足够的持久高效T细胞的同时,仍能防止有害的免疫过度活跃。
引用: Lee, K.P., Elster, S., Epstein, B. et al. PD-1 protects expanding human T cells from premature restimulation-induced cell death by modulating TCR and CD28 signaling. Cell Death Dis 17, 272 (2026). https://doi.org/10.1038/s41419-026-08530-6
关键词: PD-1信号, T细胞存活, 免疫检查点, 激活诱导的细胞死亡, 癌症免疫治疗