Clear Sky Science · zh
骨髓瘦素-LEPR 信号通路重构线粒体氧化代谢,从而赋予急性髓性白血病化疗耐药性
为什么骨髓中的脂肪对白血病治疗很重要
许多人知道体脂会影响糖尿病和心血管疾病,但很少有人意识到隐藏在骨骼内部的脂肪也可能影响血液肿瘤对治疗的反应。本研究探讨了由脂肪细胞产生的一种激素——瘦素,如何帮助急性髓性白血病(AML)细胞抵御常规化疗。理解这一隐蔽的保护机制可能为让现有药物对患者更有效提供新的思路。
一种使化疗处于不利地位的激素
研究者首先研究了新确诊成人AML患者的骨髓样本。他们测定了骨髓中瘦素的水平,并观察患者在接受常用化疗药物阿糖胞苷(cytarabine)后清除白血病细胞的情况。骨髓瘦素水平较高且白血病细胞上瘦素受体表达较高的患者更不易对治疗产生反应,生存期也更短。即便在考虑了其他风险因素后,瘦素仍然是化疗疗效不佳的强烈预示。这提示脂肪来源的激素并非仅仅反映病情严重性,而是与耐药性存在主动关联。
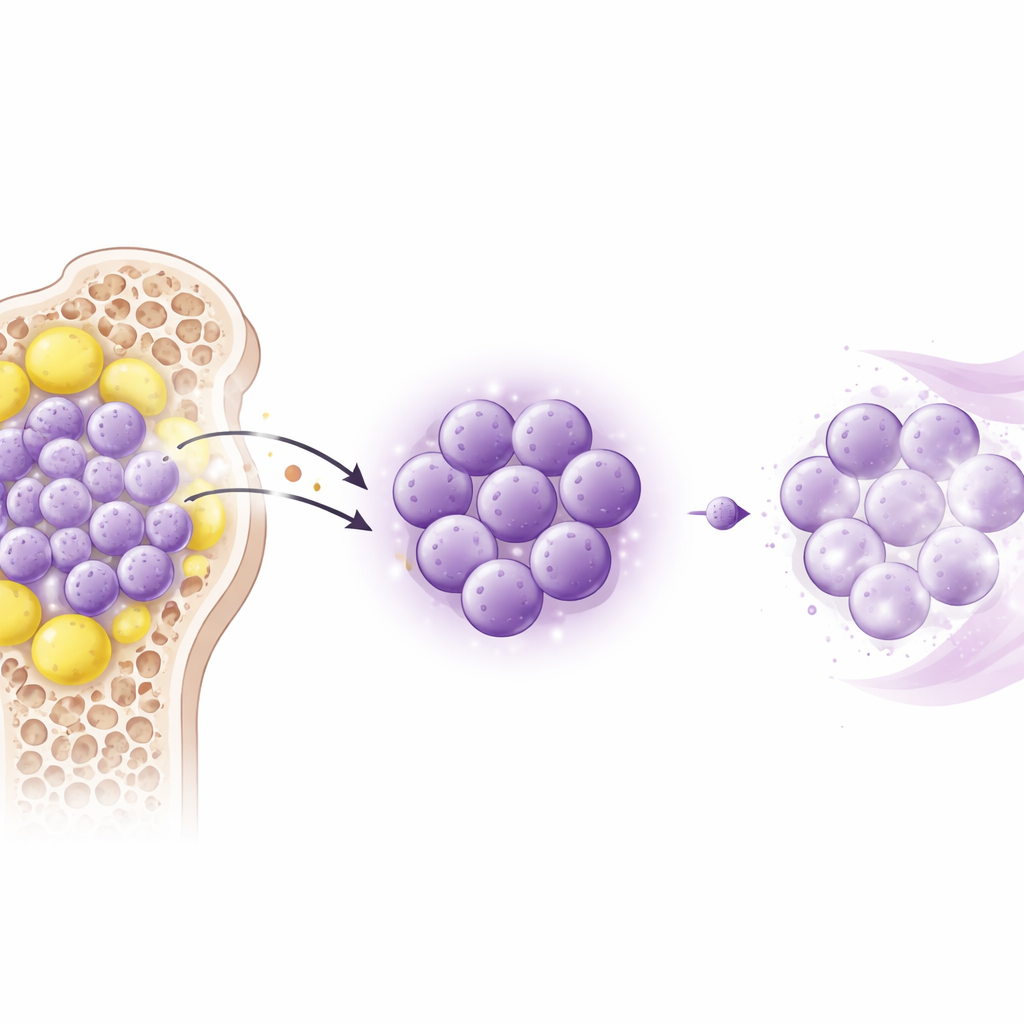
动物模型揭示了隐秘的保护屏障
为验证瘦素是否真正引起药物耐受,研究团队转向了两种高度模拟人类疾病的AML小鼠模型。小鼠分别接受单独阿糖胞苷、阿糖胞苷加外源瘦素,或阿糖胞苷与一种阻断瘦素受体的小肽联用。补充瘦素会缩短存活时间、使脾脏和肝脏肿大,并使白血病细胞在化疗下仍能侵入这些器官。相比之下,阻断受体本身并不会单独减缓白血病生长,但显著增强了阿糖胞苷的疗效,缩小受累器官并降低白血病负荷。这些发现表明,瘦素的主要作用不是直接加速癌细胞增殖,而是在化疗作用下使白血病细胞更难被清除。
为细胞的能量中枢增压
进一步研究显示,瘦素如何改变白血病细胞的代谢。他们发现瘦素激活细胞内的一条信号链,称为 JAK2/STAT3,这反过来提升了线粒体的活性——线粒体是产生能量的微小“发电厂”。在小鼠白血病细胞和人类AML细胞系中,瘦素增强了线粒体关键组分复合体 I 的活性并增加了整体氧化代谢。这一变化在粒线体内产生了更多的活性氧(ROS)。矛盾的是,这种持续低度的活性分子上升并未直接杀死细胞,反而触发了一种适应性反应:白血病细胞增强了抗氧化防御,例如谷胱甘肽和解毒酶,从而建立起强大的内部防护网。
当应激变成护甲
团队证明,这种防护网是化疗耐药的核心。瘦素处理的白血病细胞总体抗氧化能力更强,对阿糖胞苷和另一种药物柔红霉素(daunorubicin)不那么敏感。通过基因编辑去除瘦素受体会削弱该抗氧化网络,降低保护性分子水平,并使细胞在没有瘦素存在的情况下也更易受治疗影响。额外实验还确认,尖锐的线粒体应激爆发也能触发类似的保护程序,而清除这些活性分子则会破坏防护网并恢复药物敏感性。重要的是,阻断 JAK2/STAT3 信号通路或直接阻断瘦素受体可防止复合体 I 的激活,降低线粒体应激信号,瓦解抗氧化屏障,从而使化疗重新有效。
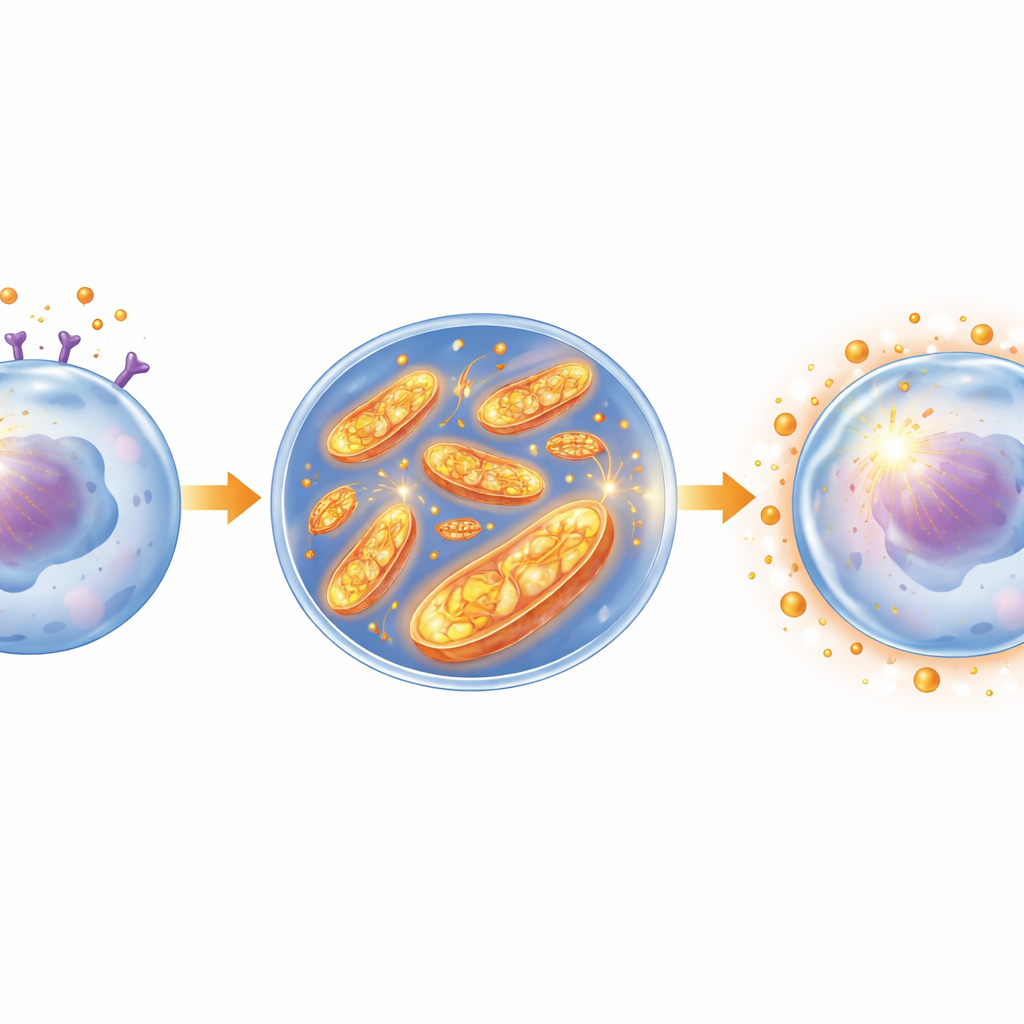
把弱点变成新的治疗切入点
对患者而言,这项研究传递的信息是:白血病细胞可以利用邻近脂肪细胞分泌的激素来逃避化疗。骨髓脂肪产生的瘦素与白血病细胞表面的受体结合,将它们的线粒体改造为高能量输出状态,并利用由此产生的低水平应激来激活抗氧化安全网。该安全网保护细胞免受化疗药物带来的更严重损伤。通过阻断瘦素受体或其下游信号,临床上或可去除这种保护,让现有化疗按预期发挥作用,而不必单纯提高药物剂量。由此,更好地理解骨髓脂肪与白血病细胞的“对话”有望直接转化为为AML患者带来更持久缓解的策略。
引用: Liao, X., Dai, W., Xu, X. et al. Marrow leptin-LEPR signaling rewires mitochondrial oxidative metabolism to confer chemoresistance in acute myeloid leukemia. Cell Death Dis 17, 249 (2026). https://doi.org/10.1038/s41419-026-08528-0
关键词: 急性髓性白血病, 瘦素, 化疗耐药, 线粒体, 氧化应激