Clear Sky Science · zh
ISG化防止STING被自噬降解并促进肺癌抗肿瘤免疫
为何保护细胞警报对肺癌很重要
我们的免疫系统配备了微小的警报开关,可在出现异常时提醒身体,例如病毒感染或肿瘤生长。其中一种名为STING的警报,有助于将“沉默”的肿瘤变成免疫系统可以攻击的目标。但在许多肺癌中,肿瘤细胞内的STING含量会随时间下降,这会削弱那些试图激活该警报的新型抗癌药物的疗效。本研究揭示了STING消失的原因,并展示了一种使其稳定的方法,为使免疫疗法在对当前疗法反应不佳的患者中更有效开辟了途径。
细胞如何感知内部危险
当DNA片段出现在细胞内不该出现的地方,通常意味着病毒感染或癌细胞受损。细胞使用一种称为cGAS–STING的检测系统来识别这类错位的DNA。一旦被激活,STING会触发一系列信号,导致I型干扰素等强效免疫信使的产生。这些信使召集包括自然杀伤细胞和杀伤性T细胞在内的多类防御者,去攻击被感染或恶变的细胞。然而,在许多肿瘤,尤其是晚期肺癌中,STING水平异常偏低,削弱了这一内部警报系统,帮助癌细胞隐匿。
拯救STING的保护标签
细胞内的蛋白质不断被标记、转运和降解。作者聚焦于一种特定的分子标记,称为ISG化(ISGylation),即将小蛋白ISG15连接到其它蛋白上。他们发现,将ISG15附加到STING的四个特定位点,相当于为其披上一层保护盾。这层盾阻止STING被细胞的“回收”机械吞噬——即通常用于清除废旧或过剩成分的自噬过程。在肺癌细胞中,当STING无法获得这些ISG15标签时,它会更快被清除,其警报信号减弱,下游的免疫反应——包括干扰素产生——急剧下降。 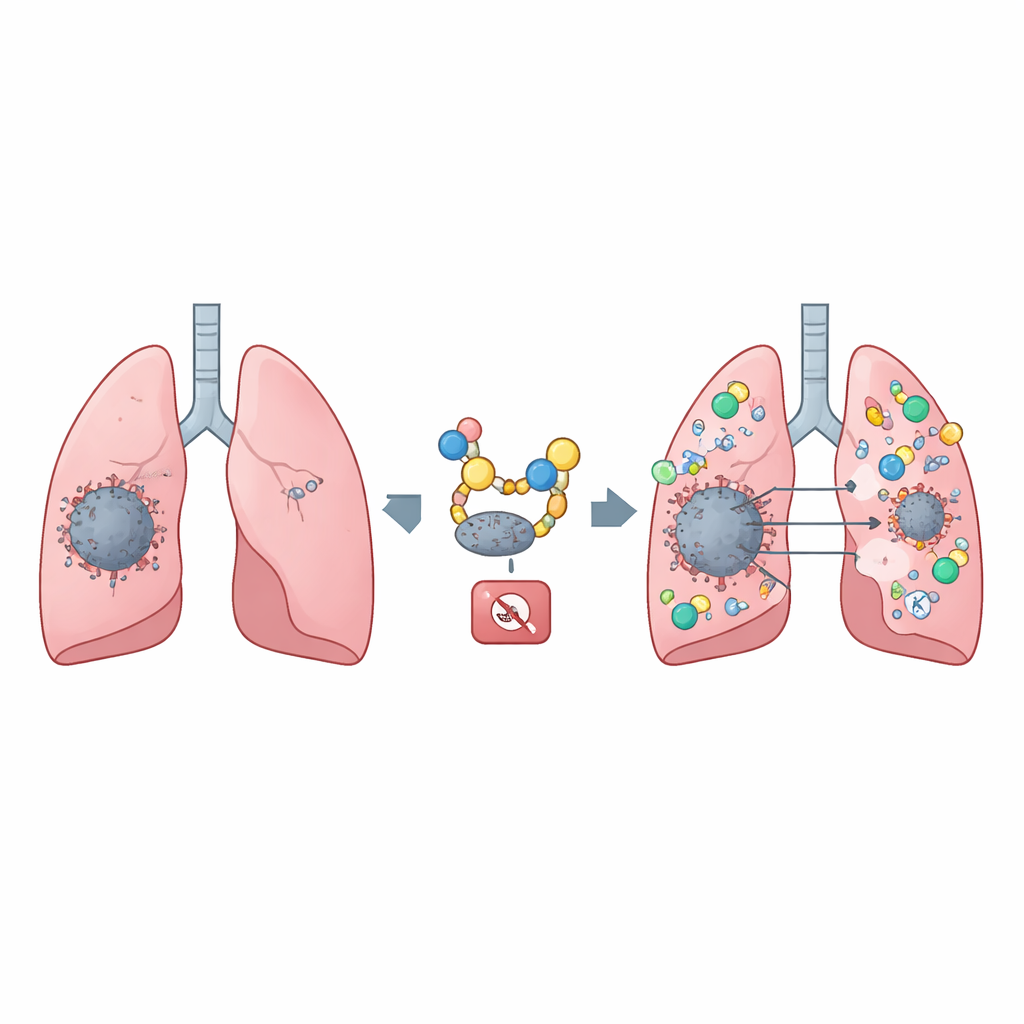
阻断细胞“碎纸机”
研究团队接着探查是哪类分子移除了这种保护性标记。他们鉴定出一种酶——USP18,能剪掉STING上的ISG15,使其暴露于自噬降解之下。在细胞实验和小鼠肺肿瘤模型中,USP18水平较高会导致STING减少、免疫细胞浸润肿瘤减少以及肿瘤生长更快。人类肺癌样本也呈现类似趋势:肿瘤中常见USP18升高而STING降低,且USP18较高的患者通常预后较差。这些模式表明USP18像一个细胞内的碎纸机开关,在癌症中错误地关闭了STING警报。
增强免疫攻击的药物组合
由于像USP18这样的酶可以被小分子阻断,研究者筛选了数千种化合物,并锁定丹参酮IIA磺酸盐(Tanshinone IIA sulfonate,TST)作为直接的USP18抑制剂。在体外,TST阻止USP18从STING上剥离ISG15,延长了STING在细胞内的寿命并增强其信号传导。在携带肺肿瘤的小鼠中,TST减缓了肿瘤生长。当研究团队将TST与另一种直接激活STING的药物diABZi联合使用时,效果尤为显著:肿瘤更明显缩小,免疫细胞——尤其是自然杀伤细胞和杀伤性T细胞——大量浸润肿瘤。该组合产生的免疫攻击比单独任何一种治疗都更强且更持久。 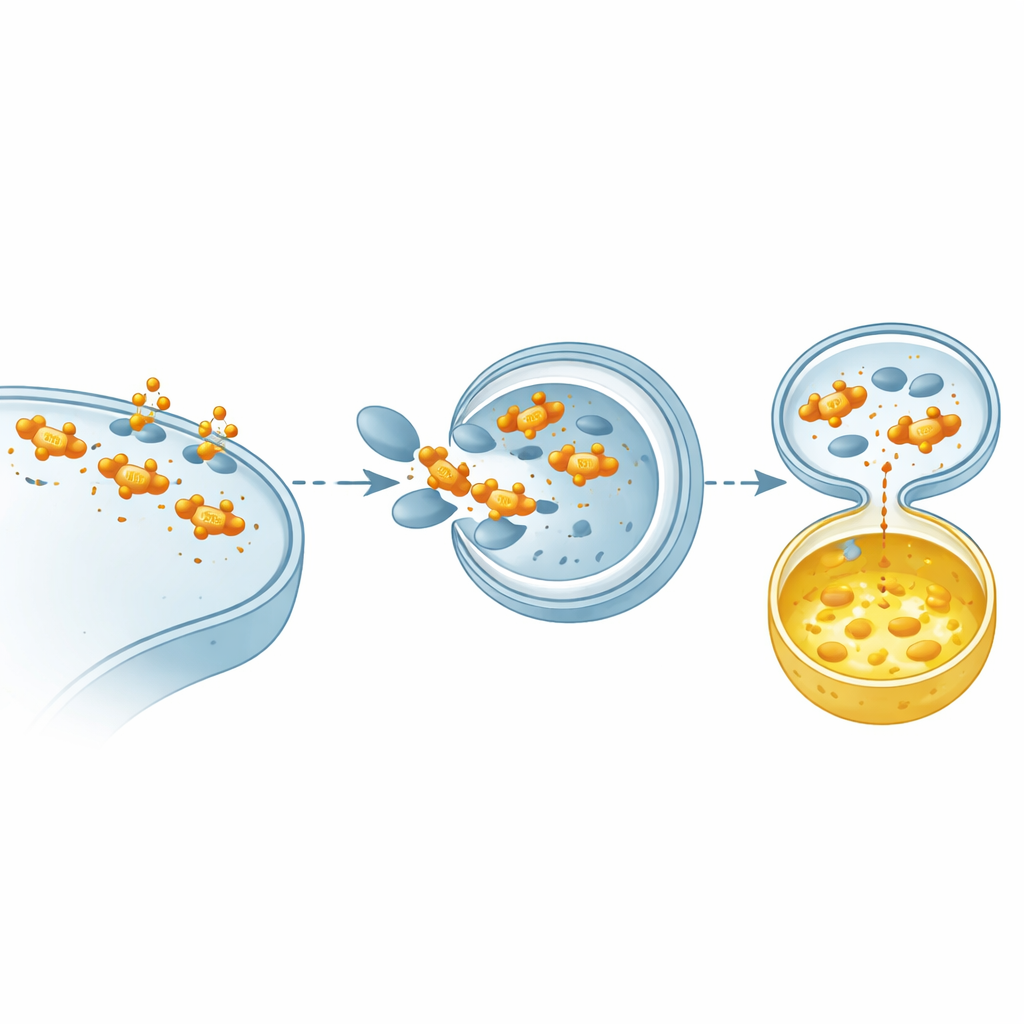
这对未来肺癌治疗意味着什么
简而言之,这项工作表明肺肿瘤常通过两种方式使关键的内部警报STING沉默:不仅减少其产生,还加速其降解。一种天然的保护标签ISG15可防止STING被卷入细胞的回收系统,而USP18则移除该标签、促进STING丧失。通过鉴定出一种阻断USP18并维持STING的药物,并将其与激活STING的药物配合使用,研究勾勒出一种策略:将沉默、低STING的肿瘤转变为免疫系统容易识别的显性靶标。对于那些目前对基于STING的疗法反应不佳的患者,稳定STING本身可能就是将微弱反应转变为强大且持久抗肿瘤攻击的关键。
引用: Cao, D., Huang, B., Fu, X. et al. ISGylation prevents autophagic degradation of STING and promotes antitumor immunity in lung cancer. Cell Death Dis 17, 271 (2026). https://doi.org/10.1038/s41419-026-08527-1
关键词: STING通路, ISG化, 肺癌免疫治疗, USP18抑制, 自噬