Clear Sky Science · zh
核肌球蛋白1将基因组结构与小鼠脂肪组织重塑、代谢性炎症和肥胖相连接
细胞骨架为何关系到体内脂肪
肥胖常被归咎于饮食与活动量,但在细胞深处,DNA的打包与读取方式也会影响体重。该研究揭示了一种微小的马达蛋白——核肌球蛋白1(NM1),它在细胞核中协助组织DNA,出乎意料地参与脂肪细胞的形成、能量储存和炎症触发。通过研究缺失该蛋白的小鼠,研究人员发现了基因的物理架构与异常内脏脂肪及代谢问题之间的直接联系。
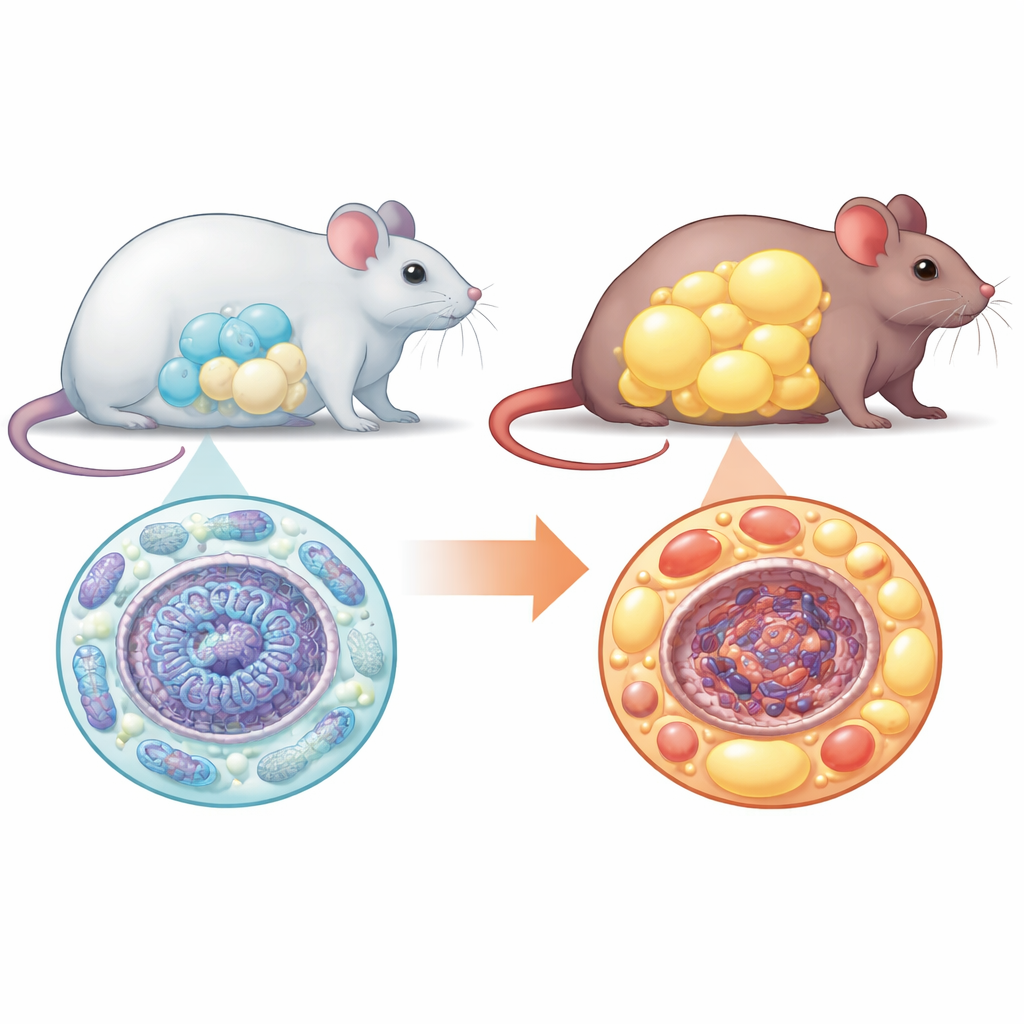
从干细胞到脂肪细胞
脂肪细胞来源于多能的前体细胞——间充质干细胞。正常情况下,这些前体细胞会增殖、改变能量利用方式,并成熟为许多个体积较小、功能良好的脂肪细胞,以安全储存多余热量。研究团队发现,缺失NM1时,这一有序过程被打乱。他们在体外培养来自正常与NM1缺失小鼠的干细胞并促使其分化为脂肪细胞,结果显示在缺失NM1的情况下,完成分化的细胞显著减少。那些完成成熟的细胞明显比正常细胞更大,脂滴充盈,但在基因和蛋白水平缺失健康脂肪细胞的常见特征。这种“细胞总数减少但个体变大”的模式是组织不健康脂肪的标志。
基因包装如何塑造脂肪细胞行为
NM1在细胞核内工作,帮助维持某些DNA区段的开放性,使重要基因能够被激活。为理解其缺失如何改变细胞行为,研究人员将开放染色质的图谱与有无NM1细胞的基因表达数据叠加比对。他们发现许多参与脂肪细胞形成、脂肪滴处理和线粒体维护的基因在缺失NM1时既失去可及性也降低了表达。与此同时,一些与生长和信号通路相关的基因变得更加开放且表达上调。这表明NM1像一位关键的交通指挥:它帮助维持开放与闭合DNA区块的平衡,使正确的基因网络驱动健康的脂肪细胞发育与代谢。
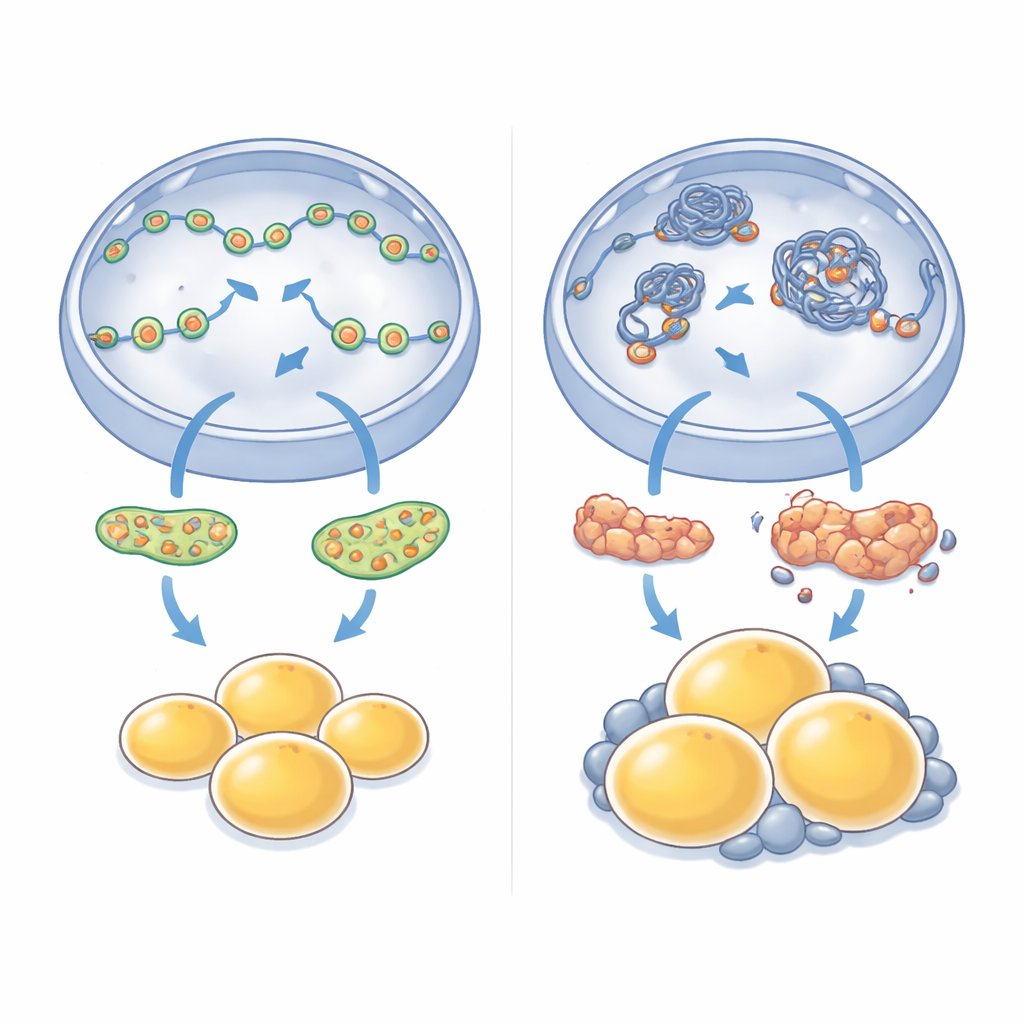
局部改变如何演变为全身增重
失去这一单一核内马达的后果并未仅局限于培养皿中的细胞。缺失NM1的小鼠随着时间推移比其正常的同窝小鼠更为肥胖,尽管它们并未摄入更多食物。影像与组织分析显示体内脂肪明显堆积,尤以腹部内脏器官周围为著,且这些部位的单个脂肪细胞异常增大。当研究者测量这些内脏脂肪中上调或下调的基因时,发现广泛的变化:涉及能量利用、胰岛素信号和组织重塑的通路被重编程。与脂肪细胞生长与扩张相关的基因常被上调,而若干控制健康脂肪细胞形成的关键基因则被抑制,这与培养中干细胞观察到的缺陷相呼应。
发炎的脂肪与受扰的能量引擎
除了体积增大外,NM1缺失小鼠的脂肪组织还表现出炎症和代谢压力的迹象。细致的通路分析显示由干扰素-γ和肿瘤坏死因子等分子驱动的免疫信号被强烈激活,这些信号已知会促进胰岛素抵抗和代谢疾病。与此同时,那些维持平稳、能效高的脂肪组织的调控因子被抑制。该研究还将NM1的缺失与线粒体受扰联系起来——线粒体是细胞的能量引擎。通常负责线粒体质量控制以及在高效氧化与快速糖酵解之间切换的基因发生紊乱,提示在NM1缺失时,脂肪细胞采用了更低效、更易受应激的能量策略。
小鼠与人类之间的共同信号
为探查这一核内马达通路在人体中是否也重要,作者检查了来自人类内脏脂肪的大型遗传数据集。他们聚焦于人类的同源基因MYO1C,并查看调节邻近基因活性的变异网络。他们发现许多在小鼠中出现的主题——细胞骨架调控、免疫信号和代谢调节——也出现在以MYO1C为中心的人类基因网络中。若干在NM1缺失小鼠脂肪中改变的基因也嵌入这些人类网络,并且与脂肪组织重塑和代谢有关。这种跨物种的重叠表明类似的核内机制可能影响人类的肥胖风险。
这对肥胖与代谢健康意味着什么
综上所述,这项工作表明NM1不仅仅是核内的一个帮手;它是将DNA组织形式与脂肪细胞如何生长、储能并与免疫系统交流联系起来的中心枢纽。当NM1缺失时,脂肪前体细胞的基因开关被错误设置,线粒体功能受损,脂肪细胞是扩大而非增殖,内脏脂肪变得发炎——这一组合类似于肥胖与胰岛素抵抗中见到的不健康脂肪表现。对普通读者而言,信息是:DNA及其核内辅助因子的物理排列可以使组织倾向于健康或有害的脂肪扩张。像NM1及其人类对应物MYO1C这样的蛋白,未来可能成为从内部重塑脂肪组织的治疗靶点,为更精确地应对肥胖相关疾病提供新途径。
引用: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
关键词: 脂肪生成, 染色质, 线粒体, 内脏脂肪, 代谢性炎症