Clear Sky Science · zh
M2 巨噬细胞通过调控 PKM2 核转位促进三阴性乳腺癌的淋巴转移
这项研究为何重要
对于被诊断为三阴性乳腺癌的人来说,最令人担忧的问题之一是癌症会扩散到附近的淋巴结——这是向全身转移迈出的关键一步。本研究深入探讨了本应保护我们的某些免疫细胞如何反而帮助此类乳腺癌侵入淋巴系统,并确定了一个可被药物靶向的分子“开关”,以减缓或阻止这种扩散。
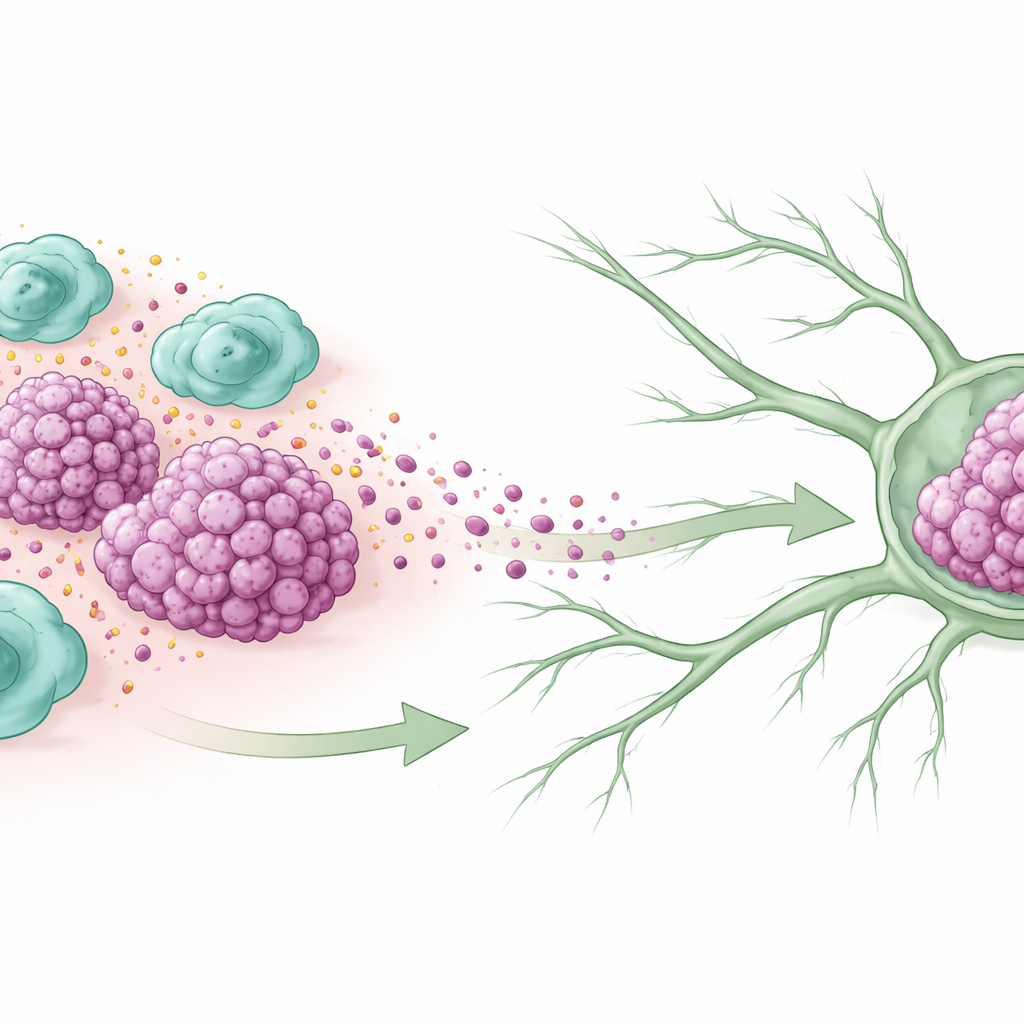
由保护者变为同谋的免疫细胞
在许多肿瘤内,称为巨噬细胞的免疫细胞大量聚集。其中一些会进入一种类似修复伤口、具有滋养功能的状态,称为 M2 状态,而在癌症环境中,这种状态常常最终帮助肿瘤而非对抗它。研究人员检查了三阴性乳腺癌患者的组织,发现已侵及淋巴结的肿瘤中含有更多的 M2 型巨噬细胞。肿瘤中这些细胞越多的患者,肿瘤往往越大、侵袭性越强、存活期越短,表明这些“友军误伤”的免疫细胞与癌症恶化密切相关。
为癌细胞构建新的淋巴“通道”
癌细胞通常不是偶然到达淋巴结;它们常沿新形成的淋巴管迁移,淋巴管是从组织排出液体的微小通道。本研究发现,富含 M2 巨噬细胞的肿瘤中也交织着更多这样的淋巴管。在体外培养中,当乳腺癌细胞与 M2 巨噬细胞共培养时,它们释放的信号促使人类淋巴内皮细胞形成管状网络并更快迁移,模拟了新淋巴通道的生长。在小鼠中,先暴露于 M2 巨噬细胞的癌细胞在肿瘤内产生了更多淋巴管并更频繁地转移到附近淋巴结,证实这些免疫细胞积极帮助构建癌细胞的逃逸路线。
癌细胞内隐秘的信号链
研究团队接着探查 M2 巨噬细胞发送了哪些化学信号以推动肿瘤向淋巴转移发展。他们锁定了一个已知分子——TGF-β,发现 M2 巨噬细胞分泌该分子的量更高。该信号使乳腺癌细胞上调两种促生长因子 VEGFC 和 VEGFD 的产生,它们是淋巴管生长的强效驱动因子。关键的是,研究者表明癌细胞内的代谢酶 PKM2 在此过程中充当了核心开关。在 TGF-β 刺激下,PKM2 不仅增强细胞的糖代谢机制,还被化学修饰并转移到细胞核内,在那里它帮助激活 VEGFC 和 VEGFD 的基因表达。若缺失 PKM2 或阻断其进入细胞核,癌细胞产生的这些促淋巴生长信号会大幅减少,其诱导淋巴管形成的能力也随之下降。
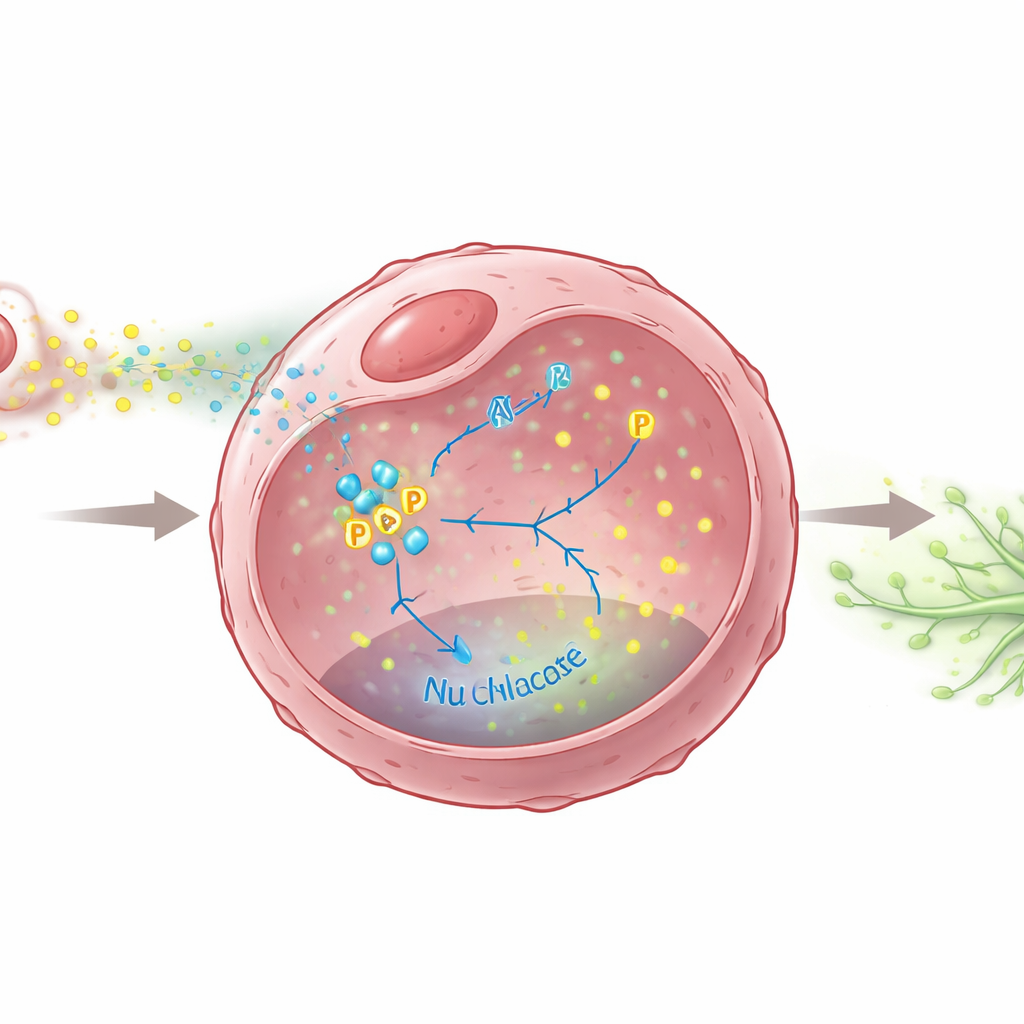
测试可能抑制扩散的刹车
鉴于 PKM2 处于改变代谢与促转移信号之间的关键节点,科学家们测试了抑制其活性是否能减缓淋巴转移。他们使用了紫草酮(一种干预 PKM2 激活和核进入的化合物)。在细胞实验中,紫草酮显著降低了 VEGFC 和 VEGFD 的水平,并削弱了癌细胞分泌物诱导淋巴管生长与迁移的能力。在小鼠模型中,紫草酮处理减少了淋巴结转移的数量和体积,并降低了肿瘤内淋巴管的密度,同时对动物未见明显毒性。这些发现表明,阻断 PKM2 既可能剥夺癌细胞某些代谢优势,又能削弱其重塑淋巴网络以利于自身扩散的能力。
对患者的意义
总体而言,该研究提出了一个清晰的事件链:三阴性乳腺肿瘤中的 M2 巨噬细胞分泌 TGF-β,促使癌细胞内的 PKM2 转变为一种双重作用——既促进高糖代谢,又在细胞核内激活 VEGFC 和 VEGFD。这些因子随后刺激淋巴管的生长,成为癌细胞到达淋巴结及更远处的通道。通过将 PKM2 确定为这一链条中的关键枢纽,该工作提出了新的预测和潜在治疗淋巴转移的方法,特别适用于肿瘤中显示出高水平 M2 型巨噬细胞、PKM2 或 VEGFC/D 的患者。尽管尚需更多人体试验,但靶向该通路或可帮助将淋巴系统从癌症的高速公路重新变为阻碍其扩散的屏障。
引用: Yang, Y., Ye, H., Zhong, D. et al. M2 macrophages promote lymphatic metastasis by regulating PKM2 nuclear translocation in triple-negative breast cancer. Cell Death Dis 17, 262 (2026). https://doi.org/10.1038/s41419-026-08524-4
关键词: 三阴性乳腺癌, 淋巴结转移, 肿瘤相关巨噬细胞, PKM2, 淋巴生成