Clear Sky Science · zh
SETD2介导的组蛋白H3赖氨酸36三甲基化在肠道干细胞中塑造表观遗传景观以协调脂质代谢并减缓细胞衰老
随着年龄增长,肠道干细胞为何重要
在我们肠道黏膜深处,微小的干细胞持续不断地工作以更新帮助消化和吸收营养的组织。随着年龄增长,这些干细胞会逐渐疲惫,导致肠道更易受病害侵袭、愈合变慢。本研究探讨了位于包装DNA的蛋白上的微妙化学标记如何维持肠道干细胞的“年轻”状态,这些标记的丧失如何扰乱细胞内的脂肪燃烧,以及精心选择的药物或如何在未来减缓这种衰退。
在苛刻环境中的衰老细胞
肠道内表面是体内更新最快的组织之一。位于小窝(称为隐窝)底部的干细胞分裂以替换每隔几天就要更新的数十亿细胞。这项持续的工作需要稳定的能量供给,其中很大一部分来自脂肪分解。同时,这些干细胞受“表观遗传”密码控制——即存在于组蛋白上的化学标记决定哪些基因被激活或沉默。作者关注了其中一种标记,即由酶SETD2生成的H3K36三甲基化,并探讨这一标记的改变是否有助于解释肠道干细胞随年龄衰退的原因。
随年龄褪色的保护性标记
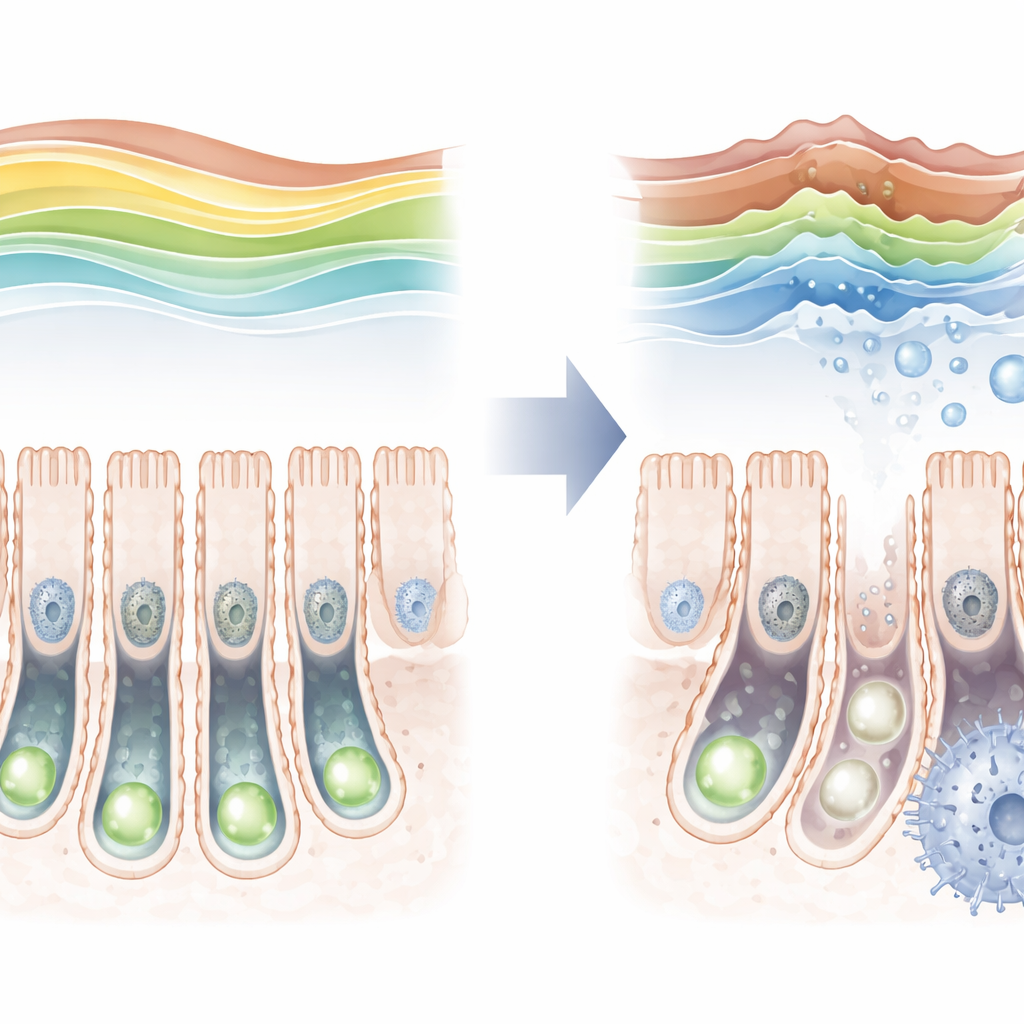
通过检查不同寿命阶段的小鼠肠道,研究者发现H3K36三甲基标记并非静止不变:出生后不久相对较低,在年轻成年期达到峰值,而在老年再次下降。随着该标记在老年动物中减少,干细胞内的衰老标志增加,暗示两者之间存在联系。为更直接检验这一点,团队构建了仅能在肠道干细胞中删除SETD2的小鼠。删除该酶后,保护性标记几乎消失,干细胞分裂频率下降,并且难以产生全套分化的肠道专门细胞类型。
表观遗传变化如何扰乱脂肪燃烧
这一单一组蛋白标记的丧失在干细胞内部引发了一连串变化。基因活性测量显示,许多与细胞周期和DNA复制相关的基因被下调,而与应激和衰老相关的基因被上调。值得注意的是,最强的信号指向脂质处理的紊乱:通常支持脂肪酸氧化(受控燃烧脂肪以获取能量)的基因被抑制,脂质开始在隐窝内积累。代谢物分析证实长链脂肪酸的累积,表明常规脂质处理通路出现衰败。与此同时,细胞核内DNA的物理包装发生改变,许多区域变得更易接触或更紧闭,从而重塑了细胞容易使用的基因集合。
染色质重塑因子与走向衰老的进程
为理解这些DNA包装变化的起因,作者绘制了全基因组范围内的开放染色质区域和一系列其他组蛋白标记。当H3K36三甲基化丧失时,大段DNA获得了“活性”标记并变得更易接近,尤其是在与代谢和衰老相关的基因附近。该转变的关键参与者是SWI/SNF染色质重塑复合体,其核心亚基为SMARCA4。在缺失SETD2的干细胞中,SMARCA4水平上升,该复合体似乎帮助打开驱动衰老程序的区域。当研究者通过基因手段或靶向抑制剂降低SMARCA4活性时,干细胞在体外形成健康类肠道结构的能力部分恢复,衰老标志下降——这表明过度的重塑推动这些细胞走向疲惫的衰老状态。
唤醒能量通路以拯救干细胞
鉴于脂肪燃烧受损成为核心问题,团队测试了增强该通路是否能抵消干细胞衰老。他们使用一种激活PPARα的药物,PPARα是脂肪酸氧化的主要调控因子。在由SETD2缺失干细胞培养的类器官中,该处理增加了生长,恢复了有活力干细胞特征的芽状结构,并减少了脂质积累。在活体小鼠中,相同的干预部分补充了干细胞库,降低了衰老标志,并使肠隐窝中的脂质积累趋于正常。这些发现将脂肪酸氧化置于表观遗传控制与干细胞健康之间的关键环节。
这对健康老化的意义
综合来看,这项工作表明由SETD2沉积的特定组蛋白标记有助于维持肠道干细胞中平衡的表观遗传景观。当该标记消退时,染色质出现异常重塑,脂肪燃烧通路失调,脂质积累,细胞走向衰老,削弱了肠道的修复系统。通过抑制过度活跃的重塑机制或用靶向药物恢复脂质代谢,或有可能在晚年保持干细胞功能和肠道健康。虽然这些发现基于小鼠,但它们与人类肠道疾病中观察到的模式相呼应,提示精细调控的代谢疗法未来或能帮助抵抗我们自身肠道干细胞的年龄相关衰退。
引用: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
关键词: 肠道干细胞, 表观遗传学, 脂肪酸氧化, 细胞衰老, SETD2