Clear Sky Science · zh
由ADSCs分泌的与Lamp2a相关的RNA阻断ENO1–乳酰化–糖酵解反馈并抑制三阴性乳腺癌细胞恶性行为
这对患者的重要性
三阴性乳腺癌是侵袭性较强的乳腺癌类型之一,缺乏激素或生长因子靶点,这些靶点使其他亚型更容易治疗。本研究揭示了这些肿瘤如何重构能量利用以在低氧环境中生存,并描述了一种针对这种代谢重编程的创新攻击方式。对读者而言,它展示了理解癌症代谢如何促成新型、高度靶向的疗法,这些疗法与传统化疗有本质不同。
这些肿瘤如何为自己提供能量
许多癌症严重依赖一种快速但效率低下的能量生成方式,即糖酵解,该途径将糖转化为副产物乳酸。通过分析患者样本、公共基因数据库和多种乳腺癌细胞系,研究者表明三阴性肿瘤比其他乳腺癌更依赖糖酵解。该途径中的关键酶ENO1在这些肿瘤中含量特别高,并且与更差的生存率相关。在体外培养的三阴性细胞中减少ENO1水平后,细胞从糖酵解向更正常的线粒体能量代谢转变,增殖减慢,侵袭和成瘤能力下降。
癌细胞内部的危险反馈回路
进一步研究发现,乳酸本身会强化ENO1并将癌细胞锁进恶性循环。乳酸可以通过所谓的乳酰化过程对蛋白质进行化学修饰。在三阴性细胞中,额外的乳酸增加了ENO1的乳酰化,反过来增强了该酶的活性和稳定性,进一步加速糖酵解并产生更多乳酸。在低氧条件下(实体瘤的典型环境),这一回路变得更强,帮助癌细胞抵抗凋亡并继续增殖。使用小分子抑制剂阻断ENO1活性或降低乳酸生成可以削弱该回路,抑制糖酵解,并在小鼠中减缓肿瘤生长。
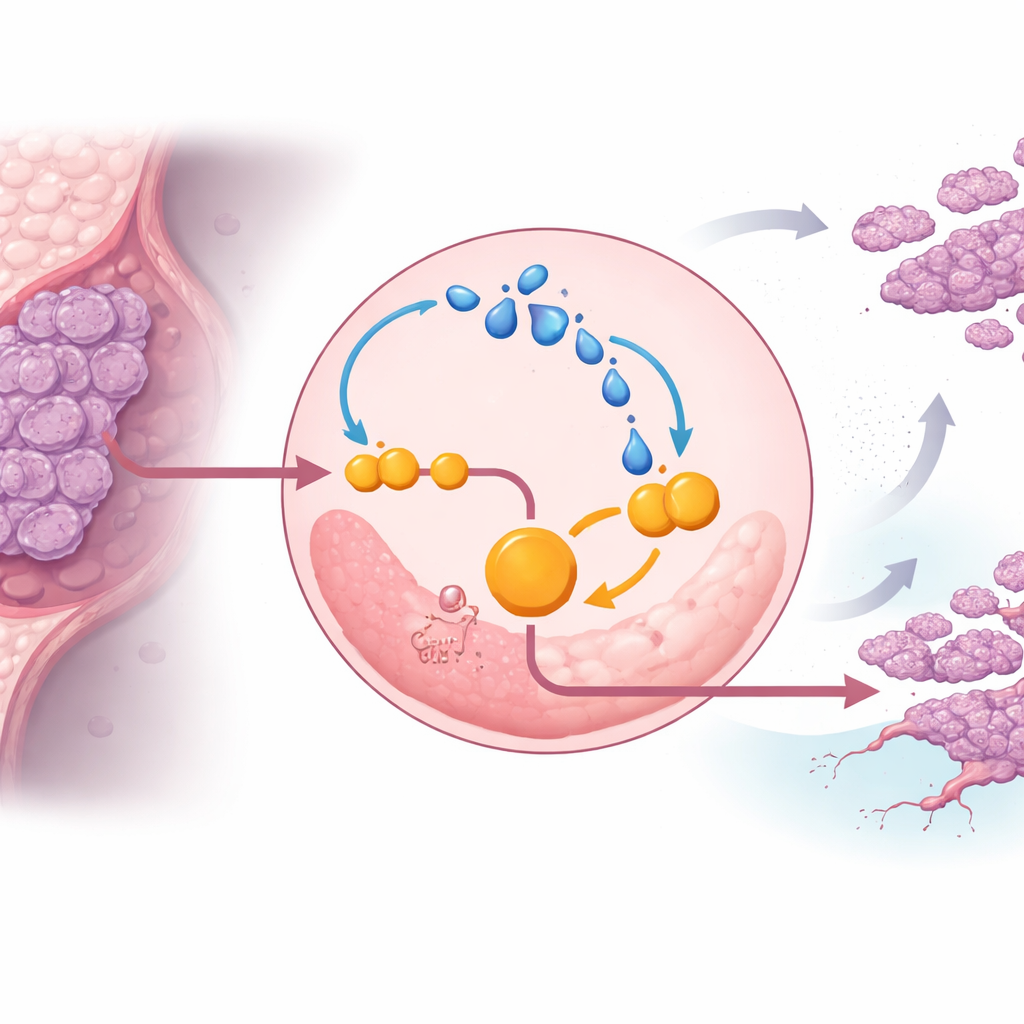
保护ENO1的分子开关
研究确定了ENO1上的一个特定控制点,使该回路成为可能。一种被称为EP300的蛋白对ENO1的多个赖氨酸位点添加乳酸基标记,其中一处位点K262尤为关键。当该位点突变以致无法被乳酰化时,ENO1会被迅速运送到细胞的回收中心——溶酶体,并被降解。失去这一保护性修饰后,三阴性细胞的糖酵解驱动性及在动物模型中形成肿瘤和转移的能力大幅下降。这将ENO1在K262位点的乳酰化指认出为一个保护该酶免于降解并维持癌细胞改变代谢的分子开关。
标记ENO1以促其降解的新方法
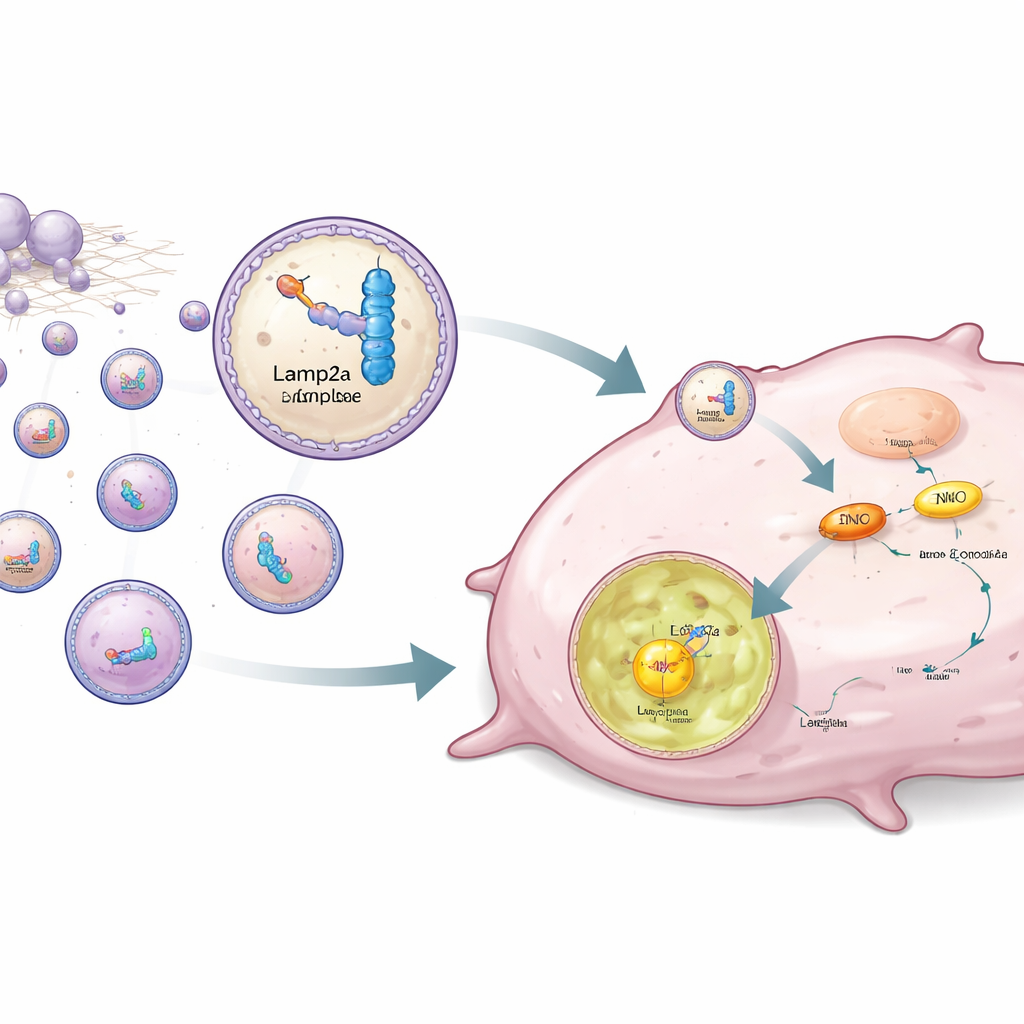
作者没有仅仅阻断ENO1,而是设计了一种选择性去除癌细胞中ENO1的策略。ENO1同时具备RNA结合蛋白的功能,能识别特定短RNA序列。研究团队工程化合成了能强烈结合ENO1的RNA片段,并将其与参与定向蛋白降解的溶酶体膜蛋白Lamp2a连接。将造成人类脂肪来源的干细胞进行基因改造,使其产生这一RNA–Lamp2a组合并将其封装进名为外泌体的小囊泡中。当这些工程化外泌体加入三阴性细胞时,RNA部分紧密结合ENO1,而Lamp2a部分将整个复合物引导至溶酶体,使ENO1即便带有稳定性的乳酰化标记也被降解。
在动物体内测试定向降解策略
为使这一想法更接近实际疗法,研究者将改造后的干细胞种植在可降解支架上,并将该构建体植入小鼠皮下,靠近三阴性肿瘤。从该位置,干细胞持续释放携带ENO1靶向复合物的外泌体。与对照动物相比,这些小鼠的肿瘤显示出明显降低的ENO1蛋白水平、糖酵解减少、分裂细胞减少以及更多细胞死亡的迹象。肿瘤生长变慢,恶性行为明显受抑,证明将ENO1引入溶酶体可有效切断肿瘤偏好的燃料通路。
这对未来治疗的可能意义
对非专业读者来说,核心信息是:这项工作同时揭示了三阴性乳腺癌的一个脆弱点和一种潜在的新治疗途径。脆弱点是肿瘤对围绕ENO1和乳酸构成的自我强化能量回路的依赖,尤其在低氧区域。治疗角度是利用定制RNA和干细胞来源外泌体的定向蛋白降解系统,将ENO1拖入细胞的处理装置。尽管距离临床应用尚远,但这一方法展示了深入理解癌症代谢如何启发精确疗法,其目标是解除而非简单毒杀恶性细胞。
引用: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
关键词: 三阴性乳腺癌, 癌症代谢, 乳酸信号, 定向蛋白降解, ENO1酶