Clear Sky Science · zh
Shp1 磷酸酶调节 CXCR2 蛋白稳定性及 IL8 介导的乳腺癌侵袭性
这项研究为何对乳腺癌重要
乳腺癌仍然是女性癌症死亡的主要原因之一,部分原因在于一些肿瘤会变得具有侵袭性并转移到远端器官。本研究解析了肿瘤中一种常见的炎性信号 IL8 如何与乳腺癌细胞对话,以及名为 Shp1 的分子“刹车”如何决定这些细胞是保持原位还是变得更具攻击性。理解这种分子上的拉锯战,可能为减缓或阻止难治性乳腺癌(尤其是三阴性病变)扩散提供新的思路。
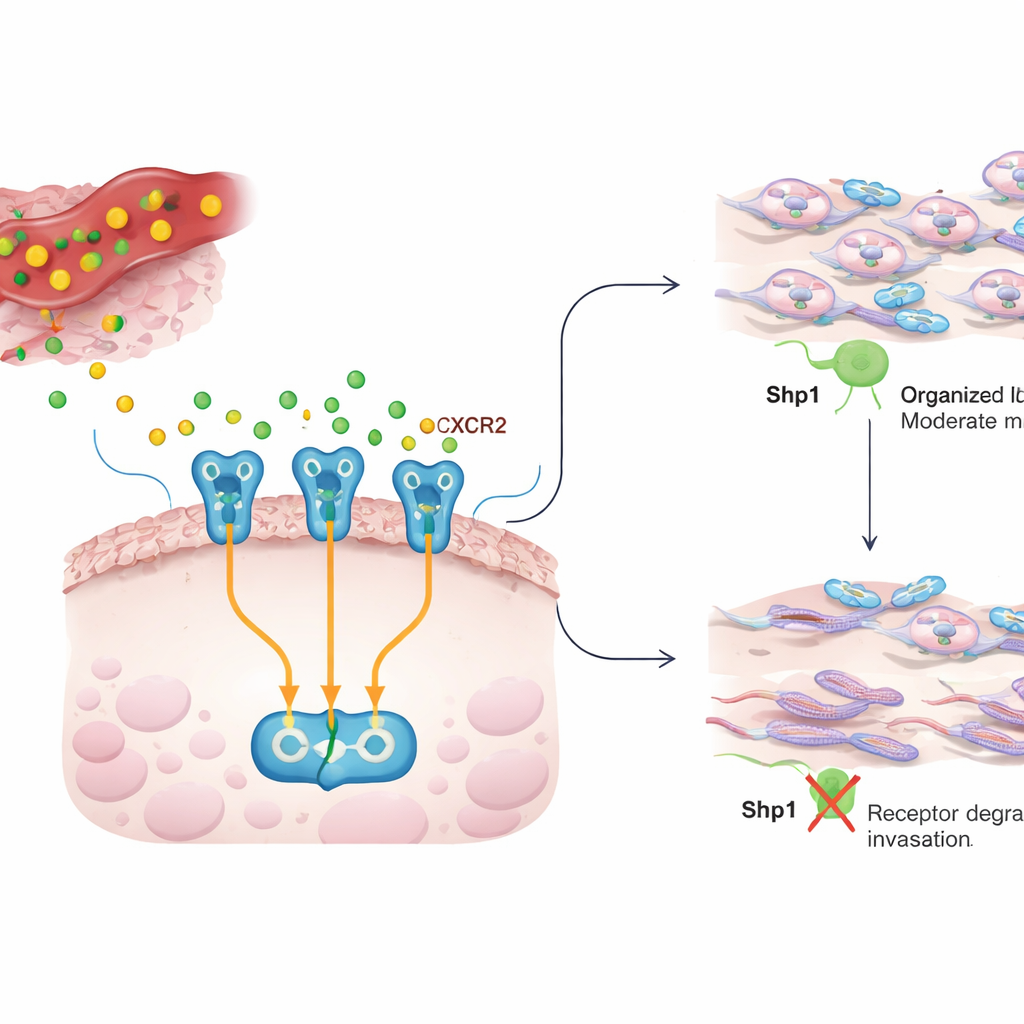
炎症与癌细胞之间的对话
在肿瘤内部,癌细胞被释放化学信使(细胞因子)的免疫细胞和支持细胞所包围。IL8 是这些信使之一,常在多种癌症中高表达,促进肿瘤增长、血管生成以及癌细胞的迁移和侵袭能力。IL8 通过癌细胞表面的受体 CXCR2 传递信号。IL8 与 CXCR2 结合时,会启动多个内部通路,重组细胞骨架,帮助细胞在组织中爬行并扩散。本研究探讨了 IL8–CXCR2 对话如何被控制,以及通常被视为对生长信号有抑制作用的酶 Shp1 是否也塑造了这种侵袭行为。
Shp1 在细胞运动中的隐性作用
研究者首先在一种常用的腔型乳腺癌细胞系(MCF7)中去除或化学抑制 Shp1,并测量细胞迁移和通过模拟组织的凝胶侵袭能力。缺失 Shp1 时,癌细胞愈合伤口更快,通过凝胶的效率提高了两到三倍,表明 Shp1 正常情况下抑制细胞运动。通过对患者数据的分析,他们还发现肿瘤中 Shp1 表达较低的女性预后更差且复发间隔更短。综合这些结果表明,Shp1 限制乳腺癌细胞的侵袭性行为,失去这一“刹车”与较差的临床结局相关。
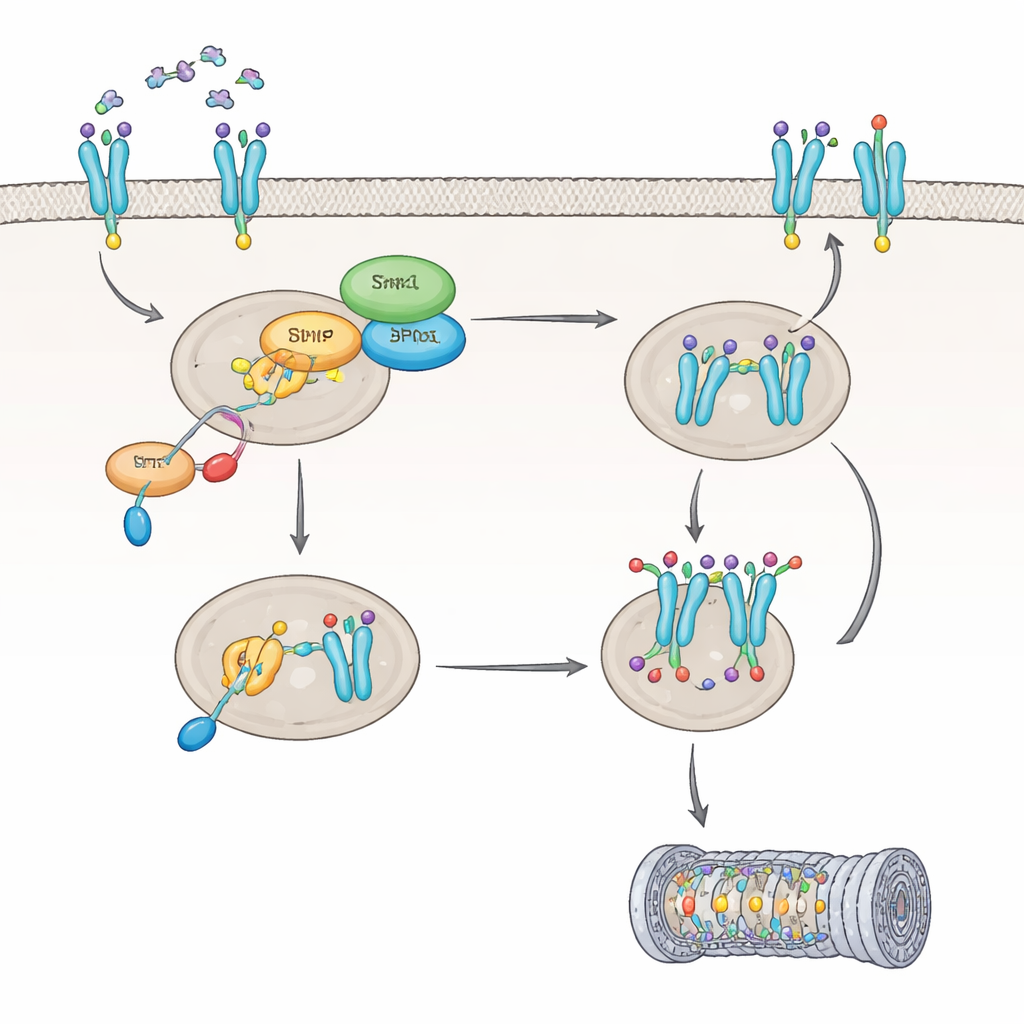
IL8 如何切换 Shp1 并重编程关键受体
接着,团队研究了 IL8 对 Shp1 本身的影响。他们发现 IL8 激活一种叫 PKC 的蛋白,PKC 在 Shp1 的特定位点发生标记,使其酶活性下降约 60%。当 Shp1 被这样抑制时,另一种酶 PP2A 的活性随之降低,CXCR2 受体保持在高度修饰的状态,从而改变其在细胞内的命运。CXCR2 不再被清理并回收至细胞表面,而是被标记为降解目标,主要通过细胞的蛋白降解机制——蛋白酶体来处理。CXCR2 上位于名为 Ser347 的氨基酸处的特定修饰对附加这些降解标签至关重要。在缺乏 Shp1 的细胞中,CXCR2 被更大量地标记并更快被分解,导致细胞表面受体数量减少,随时间对 IL8 的反应减弱。
不同乳腺癌类型,不同的信号连接
乳腺癌并非单一疾病;根据受体模式,肿瘤被分为腔型、HER2 阳性和三阴性亚型。研究团队在代表各亚型的多种细胞系中测试了 IL8–CXCR2–Shp1 回路。在腔型和三阴性细胞中,IL8 激活了 Shp1–PP2A–CXCR2 级联反应,抑制 Shp1 会既提升基础侵袭性,也消除了 IL8 通常的促侵袭作用。相反,HER2 阳性细胞仍对 IL8 有响应,但抑制 Shp1 对其行为影响甚微,提示在这些肿瘤中 Shp1 可能被与 HER2 等其他信号通路耦合,较少参与调节 CXCR2。大规模基因表达分析支持这一图景:三阴性细胞系往往 Shp1 较低、GPCR 相关信号改变且 IL8 升高,与更具侵袭性、由炎症驱动的表型一致。
这对未来治疗意味着什么
对非专业读者而言,核心信息是酶 Shp1 像交通指挥一样控制 IL8 受体 CXCR2,决定受体是被重复利用还是被销毁,进而影响乳腺癌细胞对炎性信号的响应强度。在腔型和三阴性乳腺癌中,这一控制点尤其重要:当 Shp1 水平低或其活性受阻时,细胞变得更具侵袭性,患者结局更差。由于现有某些药物可以增强或调节 Shp1,针对 Shp1–CXCR2 轴(可能联合 IL8 或 CXCR2 抑制剂)或许能为限制侵袭和减少易感乳腺癌亚型的转移提供新策略。
引用: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
关键词: 乳腺癌侵袭, IL8 信号, CXCR2 受体, Shp1 磷酸酶, 三阴性乳腺癌