Clear Sky Science · zh
利用共培养类器官研究癌症相关成纤维细胞与肿瘤细胞间串话的研究进展
为何肿瘤“邻里”很重要
癌症不仅仅是一团失控的细胞;它在一个由支持细胞、支架、血管和免疫护卫组成的繁忙“邻里”中生长。在这些邻居中,一类称为癌症相关成纤维细胞(CAFs)的细胞,默默地塑造着肿瘤的起始、扩散和对治疗的反应。本文综述说明了科学家如何使用与CAFs共培养的微型三维“类器官”,去揭示这场隐秘对话,并设计更智能、更精确的治疗方案。
培养皿里的微型肿瘤
传统癌症研究常依赖于塑料培养皿中的二维细胞层或动物模型,但这些方法只能部分反映真实疾病。类器官改变了这一局面。它们是由患者来源的肿瘤细胞形成的三维簇,保留了原始肿瘤的大部分结构、基因特征和行为。当这些类器官与CAFs共同培养时,它们开始模仿真实实体瘤,包括对化疗和放疗的响应。已经开发出多种共培养方案:简单的基于凝胶的系统中肿瘤细胞与CAFs共处同一基质;先形成致密球体的混合“悬滴”法;以及用于高通量药物筛选、能控制流体流动和类器官尺寸的微流控芯片。每种方法在逼真度、成本和技术难度之间取得不同的平衡。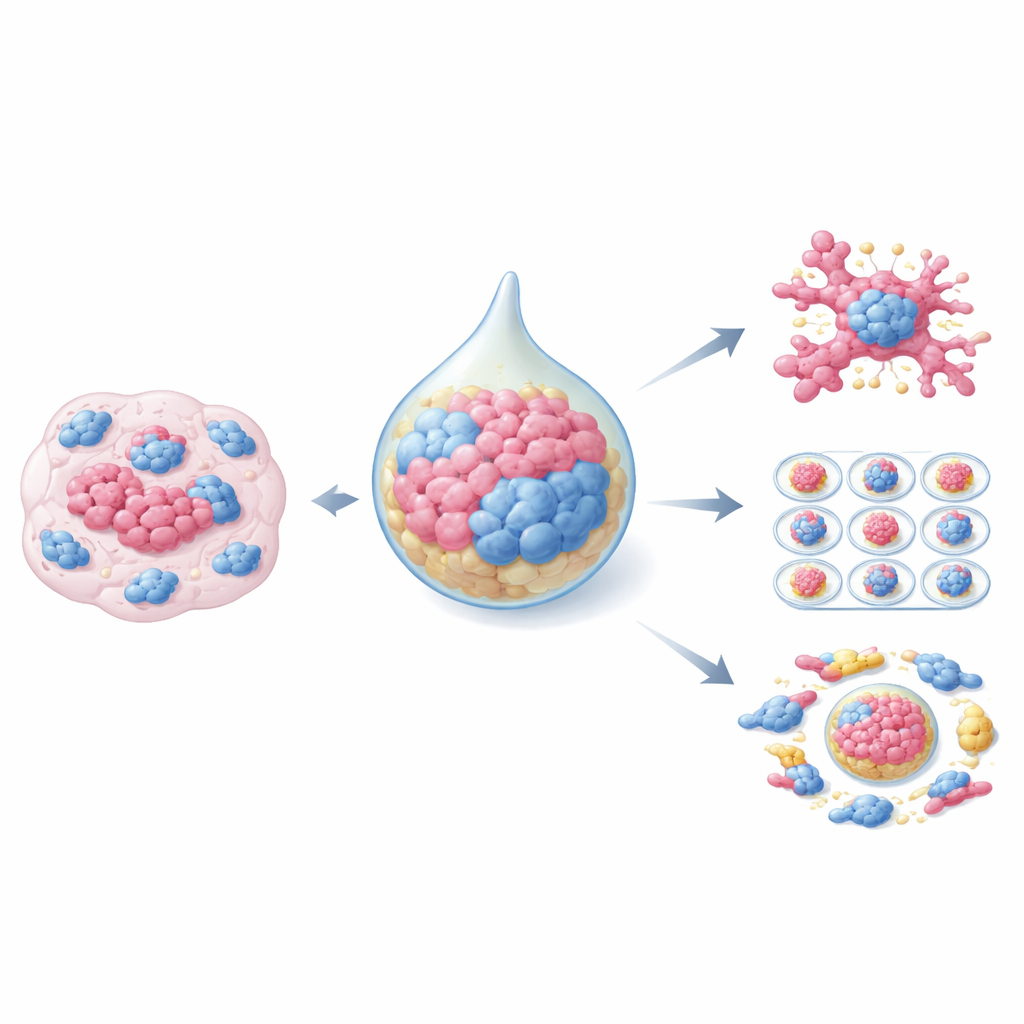
支持细胞如何帮助肿瘤繁荣
CAFs并非单一均质的细胞类型;它们有多种亚型,各自承担不同功能。在共培养类器官中,CAFs帮助构建并重塑癌细胞周围的纤维性基质,通过改变组织刚性与结构来促进肿瘤生长和侵袭。它们释放信号混合物,刺激癌细胞增殖、迁移并侵入邻近组织,甚至可诱导普通细胞获得类干细胞特性,播下新肿瘤的种子。CAFs还重塑癌细胞的能量代谢,通过营养物质互换使双方在压力下存活。在许多模型中,CAFs使肿瘤对化疗和靶向药物更具耐受性,例如通过将癌细胞包裹在致密胶原中提供屏蔽、激活生存通路,或通过发送装载RNA的小囊泡来增强DNA修复能力。
免疫逃逸与血液供应
除了为癌细胞提供养分和庇护,CAFs对机体防御也有强大影响。共培养类器官和类器官芯片系统显示,CAFs可以排斥杀伤性免疫细胞、吸引免疫抑制伙伴,并将免疫细胞推入无法攻击的状态。有些CAFs亚群会让自然杀伤细胞承受过量铁负荷并促使其发生一种死亡形式,而另一些则召唤支持肿瘤的巨噬细胞。与此同时,CAFs通过分泌促血管生成因子,鼓励新血管生长,促使血管形成细胞发芽并构建通道,确保肿瘤获得持续的氧气和营养供给。然而,这个故事并非单向:某些罕见的CAFs亚型实际上可以通过帮助激活T细胞或将其他免疫细胞重编程为更有益的状态来支持抗肿瘤免疫。
与肿瘤细胞的双向对话
CAFs与癌细胞之间的关系是一个反馈回路。肿瘤细胞发出信号,将邻近的正常成纤维细胞转化为CAFs,并进一步将它们雕塑为不同亚群,例如收缩性、产生基质的细胞或分泌大量细胞因子的炎症驱动型细胞。通过可溶性因子和微小囊泡,癌细胞能推动CAFs朝向使组织变得僵硬、促进侵袭并驱动药物耐受的状态。共培养类器官揭示了特定信号通路如何像旋钮一样调节CAFs的身份,使肿瘤得以适应不断变化的环境或治疗。理解这种来回互动至关重要,因为仅仅试图全部消除CAFs的粗暴方法,在一些动物研究和临床试验中,反而出人意料地加速了肿瘤生长。
靶向肿瘤“邻里”的新策略
借助保留CAFs–肿瘤串话的类器官模型,研究者正在探索更精细的治疗策略。与其消灭所有成纤维细胞,不如旨在阻断CAFs与癌细胞间的有害信号,破坏它们共享的代谢,或温和地“再教育”CAFs,使其转变为更良性或甚至抑制肿瘤的状态。实验性策略包括改变CAFs信号通路的小分子、软化或削薄肿瘤纤维外壳的药物,以及诸如旨在识别并攻击特定CAFs亚群的工程化免疫细胞等先进细胞疗法。基于类器官的平台使在实验室中对患者来源组织测试这些想法成为可能,为个体化组合疗法铺路,这些疗法既针对癌细胞也针对支持它们的“邻里”。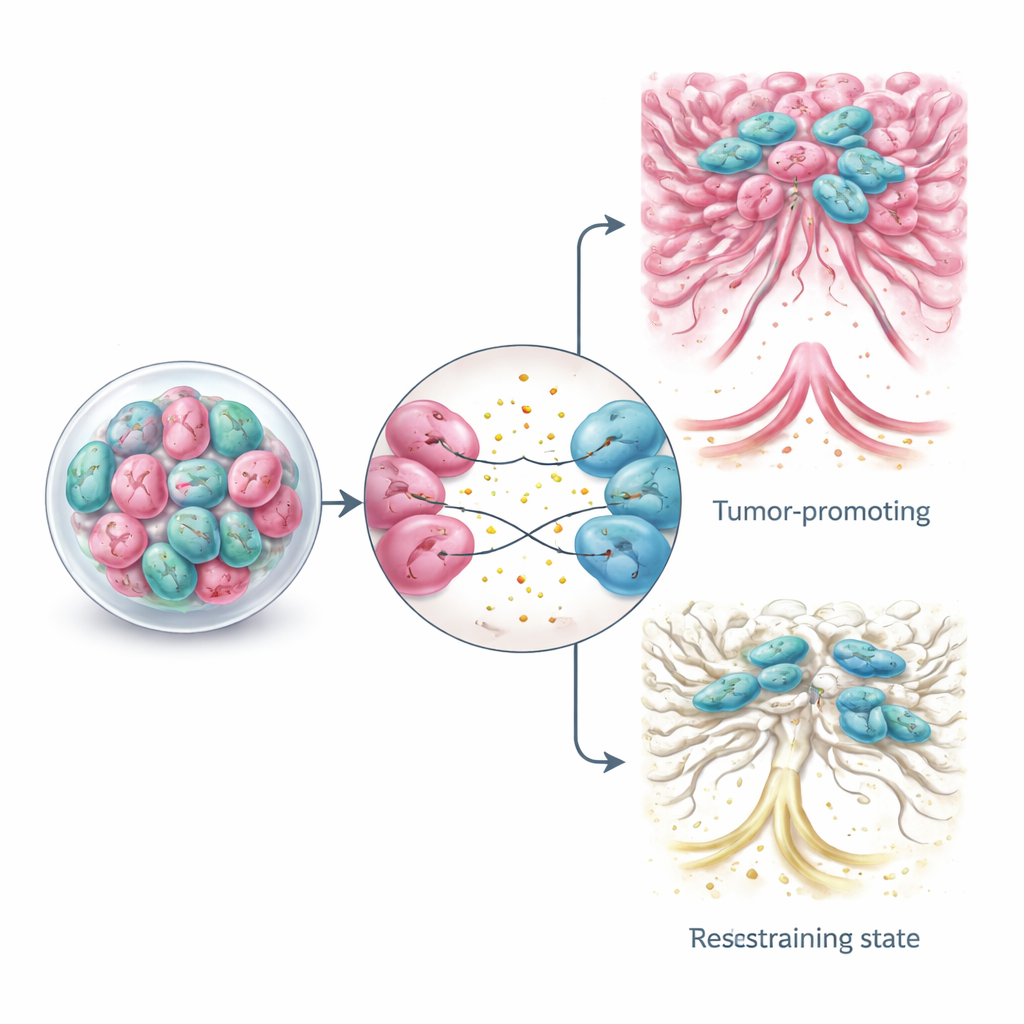
这对未来癌症护理意味着什么
本文综述认为,CAFs既是强大的助力者,有时也是癌症的潜在对手。它们的多样性和可塑性解释了为何简单的“清除CAFs”疗法常常失败甚至带来危害。通过将共培养类器官作为现实的试验台,科学家现在可以区分有益与有害的CAFs行为,绘制将其与肿瘤细胞相连的信号图谱,并设计选择性阻断促肿瘤角色同时保留或增强保护性作用的疗法。对患者而言,这项工作为更精确的药物测试和联合治疗奠定基础,这些治疗不仅攻击肿瘤本身,还重塑使其得以繁荣的“邻里”。
引用: Wang, M., Ding, X., Chen, L. et al. The research advances of crosstalk between cancer-associated fibroblasts and tumor cells using co-culture organoids. Cell Death Dis 17, 267 (2026). https://doi.org/10.1038/s41419-026-08512-8
关键词: 癌症相关成纤维细胞, 肿瘤类器官, 肿瘤微环境, 治疗耐药, 三维共培养模型